
การเปลี่ยนแปลงทางเคมีคือการเปลี่ยนแปลงของสสารที่เปลี่ยนโครงสร้างทางเคมี กล่าวคือ มันเปลี่ยนคุณสมบัติ ไม่ใช่แค่รูปร่างเท่านั้น ซึ่งหมายความว่าการเปลี่ยนแปลงทางเคมีหรือที่เรียกว่าปฏิกิริยาเคมีหรือปรากฏการณ์ทางเคมีเกี่ยวข้องกับการแตกและสร้างพันธะเคมีในสารหรือสารประกอบหนึ่งเพื่อสร้างสารหรือสารประกอบใหม่ มีมากมาย การเปลี่ยนแปลงทางเคมี ในโลกนี้
ด้วยเหตุผลนี้ เราจะอุทิศบทความนี้เพื่อบอกคุณว่าการเปลี่ยนแปลงทางเคมีหลักที่มีอยู่คืออะไร และตัวอย่างของพวกเขา
การเปลี่ยนแปลงทางเคมีคืออะไร?

เมื่อสารตั้งแต่ XNUMX ชนิดขึ้นไป (เรียกว่าสารตั้งต้นหรือสารตั้งต้น ผ่านปฏิกิริยาทางเคมีทำให้โครงสร้างทางเคมีเปลี่ยนไปในกระบวนการผลิตและสามารถบริโภคได้ (ปฏิกิริยาดูดความร้อน) หรือปล่อย (ปฏิกิริยาคายความร้อน) พลังงาน ผลิตสารตั้งแต่ XNUMX ชนิดขึ้นไป (เรียกว่าผลิตภัณฑ์) ปฏิกิริยาเคมีบางอย่างเป็นอันตรายต่อมนุษย์เนื่องจากอาจเกี่ยวข้องหรือก่อให้เกิดสารประกอบที่เป็นพิษหรือมีฤทธิ์กัดกร่อน ปฏิกิริยาอื่นๆ เช่น ปฏิกิริยาคายความร้อนสามารถทำให้เกิดการระเบิดได้
ในอุตสาหกรรมเคมี วัสดุจำนวนมากที่เราใช้ในชีวิตประจำวันผลิตขึ้นผ่านปฏิกิริยาเคมีที่มีการควบคุม ปฏิกิริยาบางอย่างเกิดขึ้นเองตามธรรมชาติ ปฏิกิริยาอื่นๆ ต้องเกิดจากมนุษย์ในโรงงานหรือห้องปฏิบัติการเคมี ปฏิกิริยาเคมีต้องใช้เวลาในการเกิด ขึ้นอยู่กับลักษณะของสารตั้งต้นและสภาวะที่เกิดปฏิกิริยา
ดังนั้นปัจจัยที่ส่งผลต่ออัตราการเกิดปฏิกิริยาเคมีโดยทั่วไป ได้แก่
- อุณหภูมิจะสูงขึ้น อุณหภูมิที่เพิ่มขึ้นมีแนวโน้มที่จะเพิ่มอัตราการเกิดปฏิกิริยาเคมี
- ความดันเพิ่มขึ้น. การเพิ่มความดันจะเพิ่มอัตราการเกิดปฏิกิริยาเคมี สิ่งนี้มักเกิดขึ้นเมื่อสารที่ไวต่อการเปลี่ยนแปลงความดัน เช่น ก๊าซ ทำปฏิกิริยา ในกรณีของของเหลวและของแข็ง การเปลี่ยนแปลงความดันจะไม่ทำให้เกิดการเปลี่ยนแปลงในอัตราการเกิดปฏิกิริยาอย่างมีนัยสำคัญ
- สถานะการรวมตัวของรีเอเจนต์. โดยทั่วไปของแข็งจะทำปฏิกิริยาได้ช้ากว่าของเหลวหรือก๊าซ แม้ว่าความเร็วจะขึ้นอยู่กับปฏิกิริยาของสารแต่ละชนิดด้วย
- การใช้ตัวเร่งปฏิกิริยา เป็นสารที่ใช้เพื่อเพิ่มความเร็วของปฏิกิริยาเคมี สารเหล่านี้ไม่รบกวนปฏิกิริยา แต่เพียงควบคุมอัตราการเกิดปฏิกิริยา นอกจากนี้ยังมีสารที่เรียกว่าสารยับยั้งซึ่งใช้ในลักษณะเดียวกันแต่ให้ผลตรงกันข้าม คือทำให้ปฏิกิริยาช้าลง
- พลังงานแสง. ปฏิกิริยาเคมีบางอย่างเร็วขึ้นเมื่อแสงตกกระทบ
- ความเข้มข้นของรีเอเจนต์ ปฏิกิริยาเคมีส่วนใหญ่จะเกิดขึ้นเร็วขึ้นหากความเข้มข้นของสารตั้งต้นสูง
ตัวอย่างของการเปลี่ยนแปลงทางเคมี
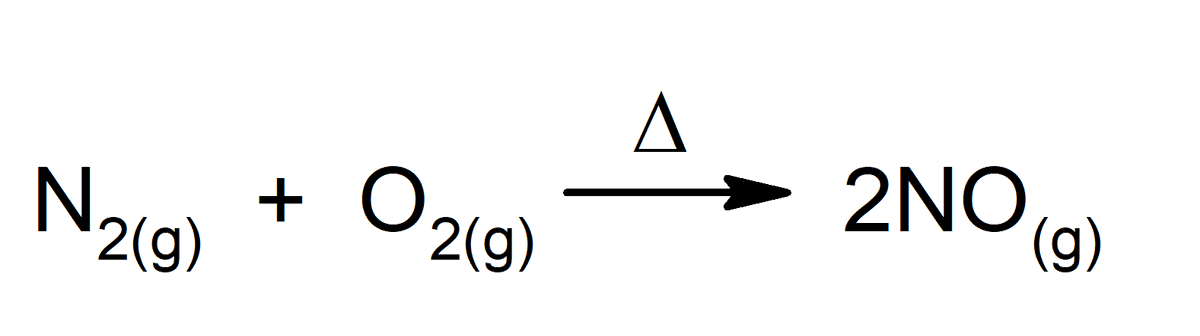
ปฏิกิริยาเคมีใดๆ ก็ตามเป็นตัวอย่างที่สมบูรณ์แบบของการเปลี่ยนแปลงทางเคมี แม้กระทั่งที่เกิดขึ้นภายในร่างกายของเรา ตัวอย่างบางส่วนคือ:
- การหายใจ นี่คือกระบวนการทางชีวภาพที่มีการเปลี่ยนแปลงทางเคมีซึ่งออกซิเจนถูกดึงมาจากอากาศและใช้ทำปฏิกิริยากับน้ำตาลกลูโคสที่เราได้รับจากอาหารทำให้เกิดพลังงานเคมี (ATP) ในระดับสูงและคาร์บอนไดออกไซด์ (CO2) จำนวนมาก ซึ่งจะต้อง ขับออกมา
- ฝนกรด. เกิดขึ้นในสภาพแวดล้อมที่มีมลพิษทางอากาศรุนแรง โดยปกติแล้วเป็นผลมาจากการเปลี่ยนแปลงทางเคมีระหว่างน้ำที่กักเก็บในเมฆและก๊าซอื่นๆ ที่กระจายตัวในอากาศ ซึ่งปริมาณซัลเฟอร์ออกไซด์หรือไนโตรเจนออกไซด์จะสร้างกรดซัลฟิวริกหรือกรดไนตริกที่ตกมาพร้อมกับน้ำฝนเพื่อก่อตัวเป็นเกลือ ปฏิกิริยาที่เกิดขึ้นภายในแบตเตอรี่อยู่ระหว่างกรดกับโลหะ ตัวอย่างเช่น แบตเตอรี่ที่ใช้ตะกั่วและกรดซัลฟิวริกจะทำให้เกิดตะกั่ว(II) ซัลเฟต ซึ่งเป็นเกลือสีขาว การสลายตัวของโอโซน โมเลกุลของโอโซนแตกตัวเป็นโมเลกุลออกซิเจนภายใต้การกระทำของแสงบางชนิด
การเปลี่ยนแปลงทางเคมีและการเปลี่ยนแปลงทางกายภาพ

การเปลี่ยนแปลงทางกายภาพของสารจะไม่เปลี่ยนองค์ประกอบของสาร กล่าวคือ ไม่ได้เปลี่ยนโครงสร้างทางเคมีของสาร ดังนั้นสารจึงไม่สามารถแตกตัวหรือก่อตัวขึ้นจากการเปลี่ยนแปลงทางกายภาพได้ การเปลี่ยนแปลงทางกายภาพเพียงแค่เปลี่ยนคุณสมบัติทางกายภาพของสสาร เช่น รูปร่าง ความหนาแน่น และสถานะของการรวมตัว (ของแข็ง ของเหลว ก๊าซ) การเปลี่ยนแปลงทางร่างกาย ในทางกลับกัน พวกมันมักจะย้อนกลับได้เพราะมันเปลี่ยนรูปร่างหรือสถานะของสสาร แต่ไม่ใช่องค์ประกอบของมัน
ตัวอย่างเช่น เมื่อน้ำเดือด เราสามารถเปลี่ยนของเหลวให้กลายเป็นก๊าซได้ แต่ไอที่เกิดขึ้นนั้นยังคงประกอบขึ้นจากโมเลกุลของน้ำ ในทางกลับกัน ถ้าเราแช่แข็งน้ำ น้ำจะกลายเป็นของแข็ง แต่ยังคงสภาพเป็นสสารเดียวกัน
อีกตัวอย่างหนึ่งคือ ก๊าซเหลวที่เราใช้ในที่จุดบุหรี่ โดยปกติจะเป็นบิวเทน (C4H10) หรือโพรเพน (C3H8) ซึ่งจะเปลี่ยนเป็นของเหลวเมื่อใช้แรงดันสูง แต่ไม่เปลี่ยนองค์ประกอบทางเคมี
การเปลี่ยนแปลงทางเคมีทำให้การจัดเรียงตัวและพันธะของอะตอมในสารเปลี่ยนไป ทำให้เกิดการรวมตัวกันในลักษณะที่ต่างออกไป ทำให้เกิดสารที่ต่างไปจากเดิม เมื่อเกิดการเปลี่ยนแปลงทางเคมี คุณจะลงเอยด้วยสารในปริมาณเท่าเดิมเสมอ แม้ว่าจะมีอัตราส่วนที่ต่างกันก็ตาม เพราะสสารไม่สามารถสร้างหรือทำลายได้ มีเพียงการแปรสภาพเท่านั้น
ตัวอย่างเช่น หากเราทำปฏิกิริยากับน้ำ (H2O) และโพแทสเซียม (K) เราจะได้สารใหม่ 2 ชนิด ได้แก่ โพแทสเซียมไฮดรอกไซด์ (KOH) และก๊าซไฮโดรเจน (HXNUMX) นี่เป็นปฏิกิริยาที่โดยทั่วไปจะปล่อยพลังงานจำนวนมากออกมา ดังนั้นจึงเป็นอันตรายมาก
ตัวอย่างการเปลี่ยนแปลงทางเคมีของสสาร
การอบคุกกี้หรือเค้ก
ของทั่วไปเช่น คุกกี้ เค้ก คัพเค้ก ฯลฯ ซ่อนปฏิกิริยาทางเคมีที่เรียกว่าการหมักซึ่ง แป้งขึ้นเนื่องจากก๊าซที่ผลิตโดยยีสต์. ในการทำขนมปัง ยีสต์จะเปลี่ยนแป้งเป็นกลูโคส
การย่อยอาหาร
การย่อยอาหารเป็นตัวอย่างที่ชัดเจนของการเปลี่ยนแปลงทางเคมีของสสารผ่านการไฮโดรไลซิส (การสลายสารอินทรีย์โดยการกระทำของน้ำ) อาหารที่เรากินในรูปของผัก ผลไม้ เนื้อสัตว์ ฯลฯ ผ่านกระบวนการผสมกับน้ำย่อยเพื่อให้ดูดซึมสารอาหารได้ดีขึ้น และเปลี่ยนเป็นสารต่างๆตามความต้องการของสิ่งมีชีวิต
ในกระบวนการเดียวกัน ธาตุหรือสารพิษส่วนเกินจะถูกกำจัดออกจากร่างกายด้วยวิธีที่แตกต่างจากของเดิม ในรูปของอุจจาระ ปัสสาวะ เหงื่อ เป็นต้น
พัลก์
การหมักเป็นกระบวนการเร่งปฏิกิริยาที่โมเลกุลกลูโคสแตกตัวเนื่องจากขาดออกซิเจน เครื่องดื่มแอลกอฮอล์บางชนิดที่ได้จากกระบวนการหมัก ได้แก่ ไซเดอร์ เบียร์ และไวน์ชนิดอ่อน ซึ่งอย่างหลังนี้เป็นหนึ่งในเครื่องดื่มที่รู้จักกันน้อยที่สุดในโลก Pulque ได้มาจากต้น Agave ผ่านกระบวนการของช่างฝีมือl ซึ่งการสุกของสารเป็นกุญแจสำคัญเพื่อให้ได้ผลิตภัณฑ์ขั้นสุดท้าย ซึ่งมีสีขาว เปรี้ยว และหนืด โดยมีรสชาติเฉพาะที่ไม่เหมาะกับรสนิยมใดๆ
การหมักยังเกิดขึ้นระหว่างการทำขนมปัง โยเกิร์ต ชีส เป็นต้น
ขนม
คาราเมลเป็นตัวอย่างพื้นฐานของการเปลี่ยนแปลงทางเคมีของสาร เช่น น้ำตาลทรายขาวที่เป็นของแข็งเมื่อให้ความร้อนไม่กี่นาทีจะกลายเป็นสารที่หนาสีเหลืองอำพันที่มีกลิ่นหอม กล่าวอีกนัยหนึ่งคือผลิตภัณฑ์ที่แตกต่างไปจากเดิมอย่างสิ้นเชิง
ฉันหวังว่าด้วยข้อมูลนี้ คุณสามารถเรียนรู้เพิ่มเติมเกี่ยวกับการเปลี่ยนแปลงทางเคมีและตัวอย่างได้