Në fushën e fizikës, ekziston një degë përgjegjëse për studimin e transformimeve të prodhuara nga nxehtësia dhe puna në sistem. Bëhet fjalë për termodinamikën. Shtë një degë e fizikës që është përgjegjëse për studimin e të gjitha kalimeve, të cilat janë vetëm rezultat i një procesi që përfshin ndryshime në ndryshoret e gjendjes së temperaturës dhe energjisë në nivelin makro. Ka disa parimet e termodinamikës të cilat janë themelore për shumë aspekte të fizikës.
Prandaj, ne do t'ju tregojmë në këtë artikull se cilat janë parimet e termodinamikës dhe cila është rëndësia e saj.
Karakteristikat e termodinamikës
Nëse analizojmë termodinamikën klasike, do të zbulojmë se bazohet në konceptin e sistemeve makroskopike. Ky sistem është vetëm një pjesë e cilësisë fizike ose konceptuale të ndarjes nga mjedisi i jashtëm. Për të studiuar më mirë sistemin termodinamik, gjithmonë supozohet se është një masë fizike që nuk shqetësohet nga shkëmbimi i energjisë me ekosistemin e jashtëm.
Gjendja e një sistemi makroskopik në ekuilibër përcaktohet nga sasitë e quajtura ndryshore termodinamike. Ne i dimë të gjitha këto ndryshore: temperatura, presioni, vëllimi dhe përbërja kimike. Të gjitha këto ndryshore përcaktojnë sistemin dhe ekuilibrin e tij. Falë aleancës ndërkombëtare të aplikacioneve, simbolet kryesore të termodinamikës kimike janë vendosur. Përdorimi i këtyre njësive mund të funksionojë më mirë dhe të shpjegojë parimet e termodinamikës.
Megjithatë, ekziston një degë e termodinamikës që nuk studion ekuilibrin, Përkundrazi, ata janë përgjegjës për analizimin e proceseve termodinamike që kryesisht karakterizohen nga mungesa e aftësisë për të arritur kushtet e ekuilibrit në mënyrë të qëndrueshme.
Parimet e termodinamikës
Ekzistojnë 4 parime të termodinamikës, të listuara nga zero në tre pika, këto ligje ndihmojnë për të kuptuar të gjitha ligjet e fizikës në universin tonë dhe është e pamundur të shihen fenomene të caktuara në botën tonë. Ato njihen gjithashtu me emrin e ligjeve të termodinamikës. Këto ligje kanë origjinë të ndryshme. Disa janë formuluar nga formula të mëparshme. Ligji i fundit i njohur i termodinamikës është ligji zero. Këto ligje janë të përhershme në të gjitha hetimet dhe hetimet e kryera në laborator. Ato janë thelbësore për të kuptuar se si funksionon universi ynë. Ne do të përshkruajmë parimet e termodinamikës një nga një.
Parimi i parë
Ky ligj thotë se energjia nuk mund të krijohet ose shkatërrohet, ajo vetëm mund të transformohet. Ky njihet edhe si ligji i ruajtjes së energjisë. Në fakt, kjo do të thotë që në çdo sistem fizik të izoluar nga mjedisi i tij, e gjithë energjia e tij do të jetë gjithmonë e njëjtë. Megjithëse energjia mund të shndërrohet në lloje të tjera të energjisë në një formë ose në një tjetër, shuma e të gjitha këtyre energjive është gjithmonë e njëjtë.
Ne do të japim një shembull për ta kuptuar më mirë. Duke ndjekur këtë parim, nëse kontribuojmë një sasi të caktuar energjie në një sistem fizik në formën e nxehtësisë, ne mund të llogarisim energjinë totale duke gjetur ndryshimin midis rritjes së energjisë së brendshme dhe punës së bërë nga sistemi dhe rrethina e tij. Kjo do të thotë, ndryshimi midis energjisë që ka sistemi në atë moment dhe punës që ka bërë do të jetë energjia termike e lëshuar.
Parimi i dytë
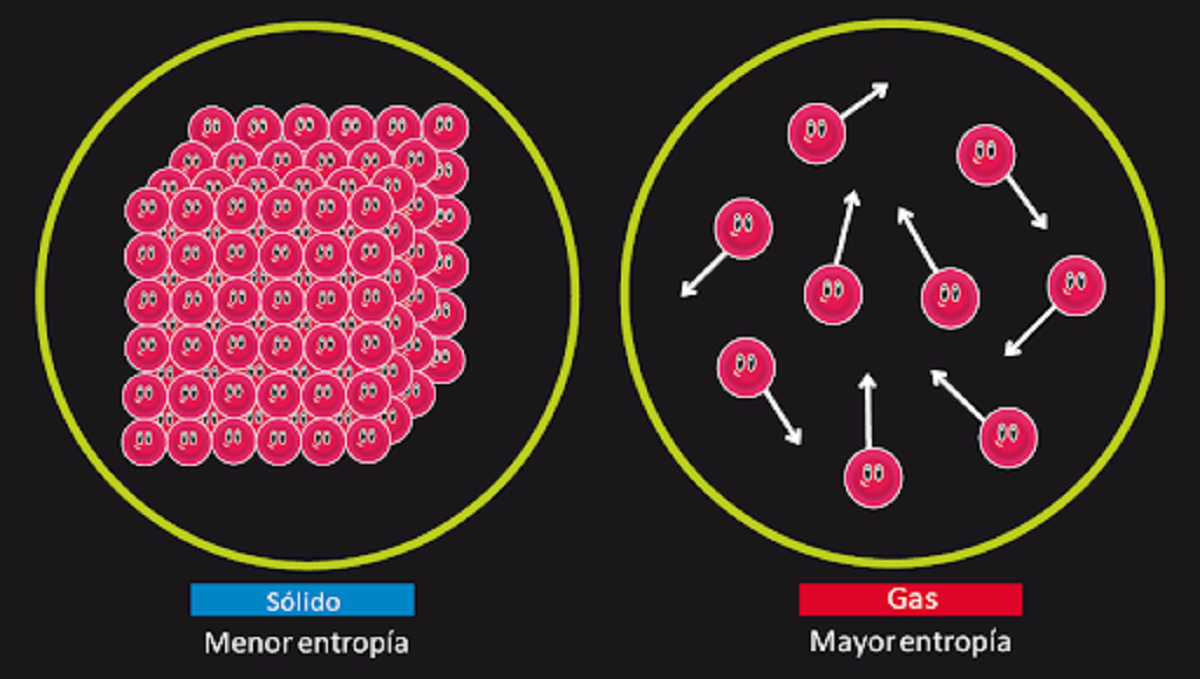
Nëse ka kohë të mjaftueshme, të gjitha sistemet përfundimisht do të humbasin ekuilibrin e tyre. Ky parim quhet edhe ligji i entropisë. Mund të përmblidhet si më poshtë. Sasia e entropisë në univers do të rritet me kalimin e kohës. Entropia e sistemit është një indeks për të matur shkallën e çrregullimit. Me fjale te tjera, Parimi i dytë i termodinamikës na thotë se sapo sistemi të arrijë një pikë ekuilibri, do të rrisë shkallën e çrregullimit në sistem. Kjo mund të nënkuptojë që nëse i japim një sistemi kohë të mjaftueshme, ai përfundimisht do të bëhet i pabalancuar.
Ky është ligji që është përgjegjës për të shpjeguar pakthyeshmërinë e disa fenomeneve fizike. Për shembull, na ndihmon të shpjegojmë pse një letër një letër e djegur nuk mund të kthehet në formën e saj origjinale. Në këtë sistem të njohur si letër dhe zjarr, çrregullimi është rritur në një masë të tillë që nuk është e mundur të kthehet në origjinë. Ky ligj prezanton funksionin e gjendjes entropi, i cili në rastin e sistemeve fizike është përgjegjës për përfaqësimin e shkallës së çrregullimit dhe humbjen e pashmangshme të energjisë.
Për të kuptuar parimin e dytë të termodinamikës ne do të japim një shembull. Nëse djegim një sasi të caktuar lënde dhe e vendosim topin së bashku me hirin që rezulton, mund të shohim se ka më pak lëndë sesa në gjendjen fillestare. Kjo ndodh sepse materia është kthyer në gaze që Ata nuk mund të shërohen dhe duhet të shpërndahen dhe të rrëmujë. Kështu e shohim që në gjendjen e parë kishte të paktën entropi sesa në gjendjen e dytë.
Parimi i tretë
Kur arrihet zero absolute, procesi i sistemit fizik ndalet. Zero absolute është temperatura më e ulët që mund të arrijmë. Në këtë rast, ne matim temperaturën në gradë Kelvin. Në këtë mënyrë, mund të thuhet se temperatura dhe ftohja bëjnë që entropia e sistemit të jetë zero. Në këto raste, është më shumë si një konstante e caktuar. Kur arrin në zero absolute, procesi i sistemit fizik ndalet. Prandaj, entropia do të ketë një vlerë minimale por konstante.
Arritja në zero absolute ose jo është një detyrë e lehtë. Vlera zero absolute e shkallës Kelvin është zero, por nëse e përdorim atë në Matja e shkallës së temperaturës Celsius, është -273,15 gradë.
Ligji zero
Ky ligj është ky i fundit supozoi dhe thotë se nëse A = C dhe B = C, atëherë A = B. Kjo përcakton rregullat themelore dhe themelore të tre ligjeve të tjera të termodinamikës. Shtë një emër që merr ligjin e ekuilibrit termik. Me fjalë të tjera, nëse sistemi dhe sistemet e tjera janë në mënyrë të pavarur në ekuilibrin termik, ato duhet të jenë në ekuilibër termik. Ky ligj lejon krijimin e parimeve të temperaturës. Ky parim përdoret për të krahasuar energjinë termike të dy objekteve të ndryshme në një gjendje ekuilibri termik. Nëse këto dy objekte janë në ekuilibër termik, ato do të jenë të panevojshme në të njëjtën temperaturë. Nga ana tjetër, nëse të dy ndryshojnë ekuilibrin termik të sistemit të tretë, ato gjithashtu do të ndikojnë tek njëri -tjetri.
Shpresoj që me këtë informacion mund të mësoni më shumë rreth parimeve të termodinamikës së karakteristikave të tij.