
ભૌતિકશાસ્ત્ર અને રસાયણશાસ્ત્ર બંનેમાં શરીરમાં રહેલી measureર્જાને માપવા માટે એક ખ્યાલ વપરાય છે. અમે વિશે વાત કરી રહ્યા છીએ મોહક. તે એક પ્રકારનું માપન છે જે શરીર અથવા સિસ્ટમમાં સમાયેલી energyર્જાની માત્રા સૂચવે છે જેનું ચોક્કસ વોલ્યુમ હોય છે, જે દબાણમાં હોય છે અને પર્યાવરણ સાથે બદલી શકાય છે. સિસ્ટમની એન્થાલ્પી એચ અક્ષર દ્વારા રજૂ થાય છે અને theર્જા મૂલ્યો સૂચવવા માટે તેની સાથે સંકળાયેલ ભૌતિક એકમ જૌલે છે.
આ લેખમાં અમે તમને એન્થાલ્પીની બધી લાક્ષણિકતાઓ અને મહત્વ જણાવવા જઈ રહ્યા છીએ.
મુખ્ય લાક્ષણિકતાઓ
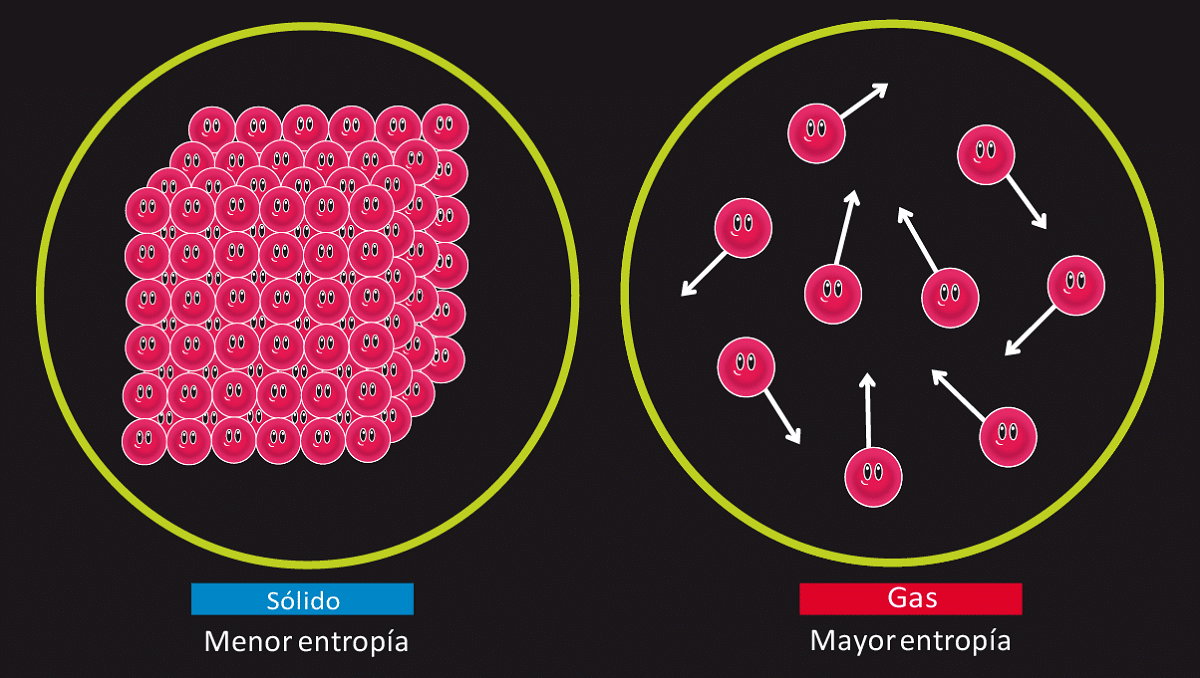
આપણે કહી શકીએ છીએ કે એન્થેલ્પી સિસ્ટમ એ આંતરિક energyર્જા જેટલી છે જે સમાન સિસ્ટમના દબાણના ગુણ ઉપરાંત છે. જ્યારે આપણે જોઈએ છીએ કે સિસ્ટમની energyર્જા, દબાણ અને વોલ્યુમ એ રાજ્યના કાર્યો છે, તો એન્થાલ્પી પણ છે. આનો અર્થ એ છે કે, જ્યારે સમય આવે છે, ત્યારે તે અમુક અંતિમ પ્રારંભિક પરિસ્થિતિઓમાં આવી શકે છે જેથી ચલ સમગ્ર સિસ્ટમનો અભ્યાસ કરવામાં મદદ કરી શકે.
પ્રથમ વસ્તુ એ જાણવાની છે કે રચનાની એન્થાલ્પી શું છે. તે વિશે જ્યારે સામાન્ય સ્થિતિમાં તત્વોમાંથી 1 પદાર્થ પદાર્થનું ઉત્પાદન થાય છે ત્યારે સિસ્ટમ દ્વારા ભૂલી ગયેલી ગરમી. આ રાજ્યો નક્કર, પ્રવાહી અથવા વાયુયુક્ત અથવા સોલ્યુશનના કિસ્સામાં હોઈ શકે છે. એલોટ્રોપિક રાજ્ય સૌથી સ્થિર રાજ્ય છે. ઉદાહરણ તરીકે, કાર્બન ધરાવે છે તે સૌથી સ્થિર એલોટ્રોપિક રાજ્ય એ સામાન્ય સ્થિતિમાં હોવા ઉપરાંત, ડિપ્રેસન મૂલ્યો છે. 1 વાતાવરણ અને તાપમાન 25 ડિગ્રી છે.
અમે ભારપૂર્વક જણાવીએ છીએ કે આપણે જે નિર્ધારિત કર્યું છે તે મુજબ રચનાની મોહક રચનાઓ ઉત્પાદિત સંયોજનના 1 છછુંદર માટે છે. આ રીતે, હાલના રીએજન્ટ ઉત્પાદનોની માત્રાને આધારે, પ્રતિક્રિયાને અપૂર્ણાંક ગુણાંક સાથે સંતુલિત કરવી પડશે.
રચના એન્થેલ્પી

આપણે જાણીએ છીએ કે કોઈપણ રાસાયણિક પ્રક્રિયામાં, રચનાની એન્થાલ્પી હકારાત્મક અને નકારાત્મક બંને હોઈ શકે છે. જ્યારે પ્રતિક્રિયા એન્ડોથર્મિક હોય ત્યારે આ એન્થાલ્પી હકારાત્મક છે. રાસાયણિક પ્રતિક્રિયા એ એન્ડોથર્મિક એટલે કે તે માધ્યમની ગરમીને શોષી શકે છે. બીજી બાજુ, જ્યારે પ્રતિક્રિયા એક્ઝોર્થેમિક હોય ત્યારે આપણી પાસે નકારાત્મક એન્થાલ્પી હોય છે. રાસાયણિક પ્રતિક્રિયા એ એક્ઝોર્ડેમિક છે તેનો અર્થ એ છે કે તે સિસ્ટમમાંથી બહારની તરફ ગરમી ઉત્તેજિત કરે છે.
એક્ઝોસ્ટરમિક પ્રતિક્રિયા થાય તે માટે, રિએક્ટન્ટ્સમાં ઉત્પાદનો કરતાં thanંચી .ર્જા હોવી આવશ્યક છે. તેનાથી .લટું, એન્ડોથર્મિક પ્રતિક્રિયા લેવા માટે રિએક્ટન્ટ્સમાં ઉત્પાદનો કરતા ઓછી energyર્જા હોવી આવશ્યક છે. જેથી આ બધાનું રાસાયણિક સમીકરણ સારી રીતે લખી શકાય, પદાર્થના સંરક્ષણના કાયદાનું પાલન કરવું જરૂરી છે. એટલે કે, રાસાયણિક સમીકરણમાં રીએક્ટન્ટ્સ અને ઉત્પાદનોની શારીરિક સ્થિતિ વિશેની માહિતી હોવી આવશ્યક છે. આ એકત્રીકરણ રાજ્ય તરીકે ઓળખાય છે
તમારે એ પણ ધ્યાનમાં રાખવું પડશે શુદ્ધ પદાર્થો શૂન્ય બરાબર રચનાની મુગ્ધતા ધરાવે છે. આ એન્થાલ્પી મૂલ્યો પ્રમાણભૂત શરતો હેઠળ મેળવવામાં આવે છે, જેમ કે ઉપર જણાવેલ, અને તેમના સૌથી સ્થિર સ્વરૂપમાં. રાસાયણિક પ્રણાલીમાં જ્યાં રિએક્ટન્ટ્સ અને ઉત્પાદનો હોય છે, પ્રતિક્રિયાની એન્થાલ્પી ધોરણની શરતો હેઠળ રચનાની એન્થાલ્પી સમાન છે.
આપણે જાણીએ છીએ કે કેટલાક અકાર્બનિક અને કાર્બનિક રાસાયણિક સંયોજનોના નિર્માણના મૂલ્યોની લંબાઈ 1 દબાણના વાતાવરણ અને 25 ડિગ્રી તાપમાનની સ્થિતિમાં સ્થાપિત થાય છે.
પ્રતિક્રિયાની એન્થેલ્પી
આપણે રચનાનો લ્હાવો શું છે તે પહેલાથી જ ઉલ્લેખ કર્યો છે. હવે અમે વર્ણવવા જઈ રહ્યા છીએ પ્રતિક્રિયાની લઘુતા શું છે. તે થર્મોોડાયનેમિક ફંક્શન છે જે મદદ કરે છે પ્રાપ્ત કરેલ ગરમી અથવા રાસાયણિક પ્રતિક્રિયા દરમ્યાન આપવામાં આવેલી ગરમીની ગણતરી કરો. ટ્રેનર સંતુલન રીજેન્ટ્સ અને ઉત્પાદનો બંને માંગવામાં આવે છે, રહે છે અથવા પ્રાપ્ત કરે છે. પ્રતિક્રિયાની એન્થાલ્પીની ગણતરી કરવા માટે એક પાસા જે પરિપૂર્ણ થવું જોઈએ તે છે કે પ્રતિક્રિયા પોતે જ સતત દબાણ પર થવી આવશ્યક છે. બીજા શબ્દોમાં કહીએ તો, રાસાયણિક પ્રતિક્રિયા થવા માટેના આખા સમય દરમિયાન, દબાણ સતત રાખવું આવશ્યક છે.
આપણે જાણીએ છીએ કે એન્થેલ્પીમાં energyર્જાના પરિમાણો હોય છે અને તેથી જ તે જ્યુલ્સમાં માપવામાં આવે છે. રાસાયણિક પ્રતિક્રિયા દરમિયાન આદાનપ્રદાન કરવામાં આવે છે તે ગરમી સાથે લલચાવનારા સંબંધને સમજવા માટે થર્મોોડાયનેમિક્સના પહેલા કાયદામાં જવું જરૂરી છે. અને તે છે કે આ પ્રથમ કાયદો અમને જણાવે છે કે થર્મોોડાયનેમિક પ્રક્રિયામાં જે ગરમીનો વિનિમય થાય છે તે પદાર્થની આંતરિક energyર્જા અથવા પ્રક્રિયામાં સામેલ પદાર્થોની વત્તા અને પ્રક્રિયા દરમિયાન જણાવ્યું હતું કે પદાર્થો દ્વારા કરવામાં આવેલ કાર્ય સમાન છે.
આપણે જાણીએ છીએ કે બધી રાસાયણિક પ્રતિક્રિયાઓ વિવિધ દબાણયુક્ત પ્રક્રિયાઓ કરતા કંઇક અલગ થર્મોોડાયનેમિક પ્રક્રિયાઓ કરતાં વધુ નથી. સૌથી સામાન્ય દબાણ મૂલ્યો વાતાવરણીય દબાણની માનક પરિસ્થિતિઓમાં આપવામાં આવે છે. તેથી, આ રીતે થનારી બધી થર્મોોડાયનેમિક પ્રક્રિયાઓને આઇસોબેરિક કહેવામાં આવે છે, કારણ કે તે સતત દબાણમાં થાય છે.
એન્થેલ્પી હીટ કહેવું ખૂબ સામાન્ય છે. જો કે, તે ખૂબ જ સ્પષ્ટ હોવું જોઈએ કે તે ગરમી જેવું જ નથી, પરંતુ હીટ એક્સચેંજ છે. તે છે, તે તે ગરમી નથી જે પાઠ આપી શકે છે અથવા રીએક્ટન્ટ્સ અને ઉત્પાદનોની આંતરિક ગરમી આપે છે. તે ગરમી છે જેનો બદલાવ રાસાયણિક પ્રતિક્રિયા પ્રક્રિયા દરમિયાન થાય છે.
તાપ સાથે સંબંધ
આપણે પહેલા જે વાત કરી છે તેનાથી વિપરીત, એન્થેલ્પી એ એક રાજ્ય કાર્ય છે. જ્યારે આપણે એન્થાલ્પી પરિવર્તનની ગણતરી કરીએ છીએ, ત્યારે આપણે ખરેખર બે કાર્યોના તફાવતની ગણતરી કરીએ છીએ. આ કાર્યો સામાન્ય રીતે સિસ્ટમની સ્થિતિ પર આધારિત છે. સિસ્ટમની આ સ્થિતિ આંતરિક energyર્જા અને સિસ્ટમના જ વોલ્યુમના આધારે બદલાય છે. કેમ કે આપણે જાણીએ છીએ કે આવૃત્તિ રાસાયણિક પ્રતિક્રિયા દરમિયાન સતત રહે છે, પ્રતિક્રિયાની એન્થાલ્પી એ રાજ્યના કાર્ય કરતા વધુ કંઈ નથી જે આંતરિક internalર્જા અને વોલ્યુમ બંને પર આધારિત છે.
તેથી, અમે રાસાયણિક પ્રતિક્રિયામાં રિએક્ટન્ટ્સના એન્થેલ્પીને તે દરેકના સરવાળો તરીકે વ્યાખ્યાયિત કરી શકીએ છીએ. બીજી બાજુ, અમે તે જ વસ્તુને વ્યાખ્યાયિત કરીએ છીએ પરંતુ ઉત્પાદનોમાં બધા ઉત્પાદનોની એન્થાલ્પીનો સરવાળો.
હું આશા રાખું છું કે આ માહિતીની મદદથી તમે એન્થાલ્પી અને તેની વિશેષતાઓ વિશે વધુ શીખી શકો છો.
