
La Batas ni Boyle ito ay natuklasan ni Robert Boyle noong ika-XNUMX siglo at inilatag ang mga pundasyon upang ipaliwanag ang kaugnayan sa pagitan ng presyon at dami na nasa mga gas. Sa pamamagitan ng isang serye ng mga eksperimento, pinamamahalaang niyang ipakita na kung pare-pareho ang temperatura, binabawasan ng isang gas ang volume nito kapag napailalim ito sa mas maraming presyon, at tumataas ang volume kung nabawasan ang presyon.
Sa artikulong ito, sasabihin namin sa iyo ang lahat ng kailangan mong malaman tungkol sa batas ni Boyle, ang mga katangian at kahalagahan nito.
pangunahing katangian
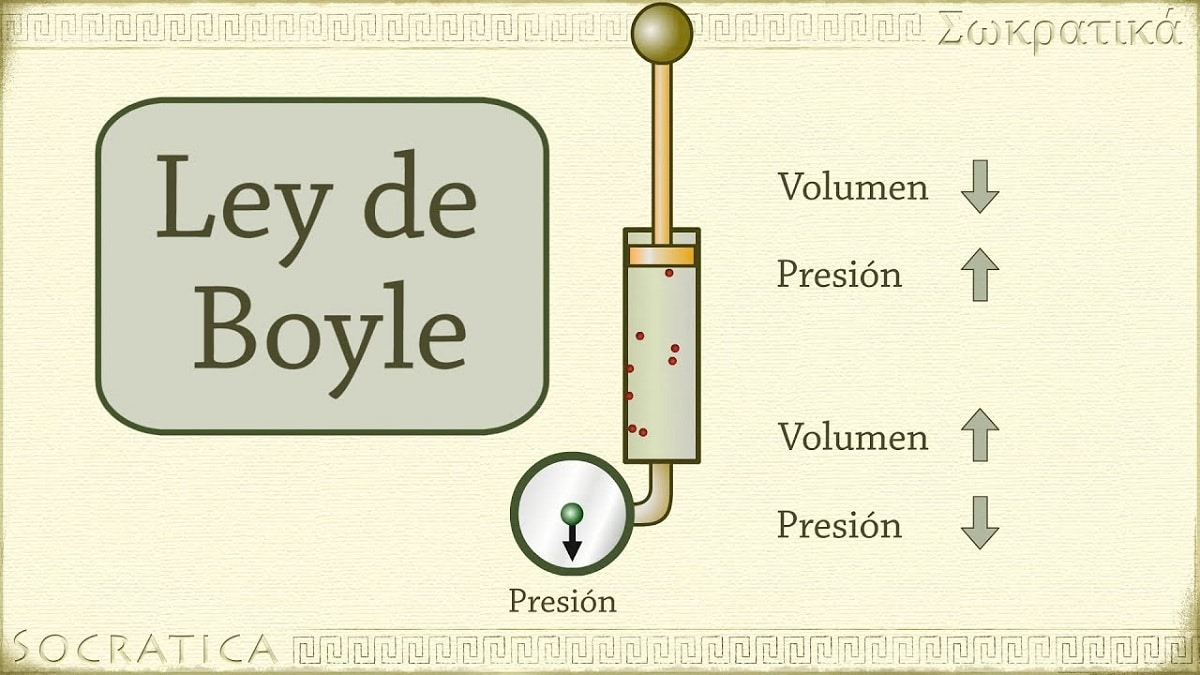
Noong 1662, natuklasan ni Robert Boyle na ang presyon na ibinibigay sa isang gas ay inversely proportional sa dami at bilang ng mga moles nito sa pare-parehong temperatura. Sa madaling salita, kung ang presyon na inilapat sa isang gas ay nadoble, ang parehong gas ay i-compress at ang dami nito ay magiging kalahati.
Habang tumataas ang volume ng lalagyan na naglalaman ng gas, tumataas din ang distansya ng mga particle bago bumangga sa mga dingding ng lalagyan. Ang pagtaas ng distansya na ito ay nagbibigay-daan sa dalas ng mga shocks na bumaba, kaya ang presyon sa pader ay mas mababa kaysa dati kapag ang volume ay mas maliit.
Ang Batas ni Boyle ay unang natuklasan noong 1662 ni Robert Boyle. Si Edme Mariotte ay isa pang siyentipiko na nag-isip at dumating sa parehong mga konklusyon bilang Boyle, gayunpaman, hindi isinapubliko ni Mariotte ang kanyang trabaho hanggang 1676. Kaya naman sa maraming aklat ay makikita natin ang batas na ito na tinatawag na Boyle and Mariot's Law Boyle-Mariot's Law, na kilala rin bilang Mattut's Law, na binuo ng British physicist at chemist na si Robert Ito ay nabuo. nang nakapag-iisa ni Boyle at ng French physicist at botanist na si Edmé Mattout.
Ito ay tumutukoy sa isa sa mga batas na nag-uugnay sa dami at presyon ng isang gas sa isang tiyak na halaga ng gas na pinananatili sa isang pare-parehong temperatura. Ang Batas ni Boyle ay nagsasaad ng mga sumusunod: Ang presyur na ginagawa ng isang puwersa ay pisikal na kabaligtaran na proporsyonal sa dami ng gaseous matter hangga't ang temperatura nito ay nananatiling pare-pareho. O mas simple, maaari nating bigyang-kahulugan ito bilang: sa isang mas mataas na pare-parehong temperatura, ang dami ng isang nakapirming masa ng gas ay inversely proporsyonal sa pare-parehong presyon na ibinibigay nito.
Mga eksperimento at aplikasyon ng batas ni Boyle

Upang patunayan ang teorya ng Batas ni Boyle, si Mariot ang namamahala sa pagpasok ng gas sa isang silindro na may piston at nagawang i-verify ang iba't ibang mga pressure na nalikha habang bumababa ang piston. Nahihinuha mula sa eksperimentong ito na habang tumataas ang volume, bumababa ang presyon.
Maraming aplikasyon ang batas ni Boyle sa makabagong buhay, bukod dito ay maaari nating banggitin halimbawa ang pagsisid, ito ay dahil ang maninisid ay kailangang ilabas ang hangin mula sa kanyang mga baga kapag umaakyat dahil ito ay lumalawak kapag bumaba ang presyon, kung hindi ito gagawin ay maaaring magdulot ng pagkasira ng tissue.
Ito ay matatagpuan sa lahat ng kagamitan na gumagamit o pinapagana ng pneumatic power, tulad ng mga robotic arm na gumagamit ng mga bahagi gaya ng mga pneumatic piston, actuator, pressure regulator, at pressure relief valve.
Ginagamit din ng mga makina ng gasolina, gas o diesel ang batas ni Boyle sa panahon ng panloob na pagkasunog, dahil sa unang pagkakataon na ang hangin ay pumasok sa silindro na may volume at presyon, sa pangalawang pagkakataon ay binabawasan nito ang volume sa pamamagitan ng pagtaas ng presyon.
Ang mga sasakyan ay may mga airbag system na gumagana sa pamamagitan ng pagpapalabas ng isang tiyak na dami ng hangin o gas mula sa isang silid na umaabot sa labas ng airbag, kung saan bumababa ang presyon at tumataas ang volume na nagpapanatili ng pare-parehong temperatura.
Napakahalaga ngayon ng Batas ni Boyle dahil ito ang batas na nagsasalita sa atin at nagpapaliwanag sa pag-uugali ng mga gas. Tiyak na ipinapaliwanag nito na ang presyon at dami ng isang gas ay inversely proportional sa bawat isa. Samakatuwid, kapag ang presyon ay inilapat sa isang gas, ang dami nito ay bumababa at ang presyon nito ay tumataas.
perpektong modelo ng gas

Nalalapat ang batas ng Boyle-Mariotte sa tinatawag na mga ideal na gas, isang teoretikal na modelo na lubos na nagpapasimple sa pag-uugali ng anumang gas, sa pag-aakalang:
- mga molekula ng gas ang mga ito ay napakaliit na hindi na kailangang isipin ang kanilang sukat, lalo na kung isasaalang-alang na ito ay mas maliit kaysa sa layo ng kanilang paglalakbay.
- Bukod dito, halos hindi nakikipag-ugnayan ang mga molekula, maliban kapag sila ay nagbanggaan nang napakaikling, at kapag nangyari ito, ang banggaan ay nababanat, kaya ang parehong momentum at kinetic na enerhiya ay natipid.
- Sa wakas, ipagpalagay na ang kinetic energy na ito ay proporsyonal sa temperatura ng gaseous sample, iyon ay, mas nabalisa ang mga particle, mas mataas ang temperatura.
Ang mga magaan na gas, anuman ang kanilang pagkakakilanlan, ay sumusunod sa mga alituntuning ito nang napakahigpit sa ilalim ng karaniwang mga kondisyon ng temperatura at presyon (ibig sabihin: 0ºC at atmospheric pressure (1 atmosphere). Para sa mga gas na ito, ang batas ng Boyle-Mariotte ay naglalarawan ng kanilang pag-uugali nang tumpak. .
Dahil ang P∙V ay pare-pareho sa isang naibigay na temperatura, kung ang presyon ng gas ay nagbabago, ang volume ay nagbabago upang ang produkto ay mananatiling pareho, kaya sa dalawang magkaibang estado 1 at 2, ang pagkakapantay-pantay ay maaaring ipahayag bilang mga sumusunod:
P1∙V1 = P2∙V2
Pagkatapos ay alam mo ang isang estado, kasama ang isang variable mula sa kabilang estado, malalaman mo ang nawawalang variable sa pamamagitan ng pag-alis nito sa batas ng Boyle-Mariot.
Kasaysayan ng Batas ni Boyle
British chemist. Pioneer ng mga eksperimento sa larangan ng kimika, lalo na sa mga katangian ng mga gas,
Ang thesis ni Robert Boyle sa pag-uugali ng bagay sa antas ng particle ay isang pasimula sa modernong teorya ng mga elemento ng kemikal. Siya rin ay isang founding member ng Royal Society of London.
Si Robert Boyle ay isinilang sa isang marangal na pamilya sa Ireland at nag-aral sa pinakamahusay na Ingles at European na mga paaralan. Mula 1656 hanggang 1668 nagsilbi siya bilang katulong ni Robert Hooke sa Oxford University, nakipagtulungan sa kanya sa isang serye ng mga eksperimento na tumutukoy sa mga pisikal na katangian ng hangin at kung paano ito nasusunog, humihinga, at nagpapadala ng tunog.
Ang mga resulta ng mga kontribusyon na ito ay nakolekta sa kanilang "Mga bagong pisikal-mekanikal na eksperimento sa pagkalastiko ng hangin at mga epekto nito» (1660). Sa ikalawang edisyon ng gawaing ito (1662), inihayag niya ang tanyag na pag-aari ng mga gas, ang batas ng Boyle-Mariotte, na nagsasaad na ang dami na inookupahan ng isang gas sa pare-parehong temperatura ay inversely proporsyonal sa presyon nito. Ngayon ay kilala na ang batas na ito ay natutupad lamang kapag ang teoretikal na ideal na pag-uugali ng mga gas ay tinanggap.
Umaasa ako na sa impormasyong ito maaari kang matuto nang higit pa tungkol sa batas ni Boyle, ang mga katangian at aplikasyon nito sa mundo ng agham.