இயற்பியல் உலகில் வெப்பம் மற்றும் ஒரு அமைப்பில் வேலை செய்யும் உருமாற்றங்களைப் படிப்பதற்கு ஒரு கிளை உள்ளது. இது பற்றி வெப்ப இயக்கவியல். இது இயற்பியலின் ஒரு கிளையாகும், இது மேக்ரோஸ்கோபிக் மட்டத்தில் வெப்பநிலை மற்றும் ஆற்றல் இரண்டின் நிலை மாறிகளில் மாற்றங்களை உள்ளடக்கிய செயல்முறைகளின் விளைவாக மட்டுமே ஏற்படும் அனைத்து மாற்றங்களையும் ஆய்வு செய்ய பொறுப்பாகும்.
இந்த கட்டுரையில் வெப்ப இயக்கவியல் மற்றும் வெப்ப இயக்கவியல் கொள்கைகளைப் பற்றி நீங்கள் தெரிந்து கொள்ள வேண்டிய அனைத்தையும் நாங்கள் உங்களுக்கு சொல்லப்போகிறோம்.
முக்கிய பண்புகள்
கிளாசிக்கல் வெப்ப இயக்கவியலைப் பகுப்பாய்வு செய்தால், அது மேக்ரோஸ்கோபிக் அமைப்பின் கருத்தை அடிப்படையாகக் கொண்டது என்பதைக் காண்கிறோம். இந்த அமைப்பு வெளிப்புற சூழலில் இருந்து பிரிக்கப்பட்ட உடல் அல்லது கருத்தியல் வெகுஜனத்தின் ஒரு பகுதியைத் தவிர வேறில்லை. வெப்ப இயக்கவியல் அமைப்புகளை சிறப்பாகப் படிப்பதற்காக, இது வெளிப்புற சுற்றுச்சூழல் அமைப்புடன் ஆற்றல் பரிமாற்றத்தால் தொந்தரவு செய்யப்படாத ஒரு உடல் நிறை என்று எப்போதும் கருதப்படுகிறது.
ஒரு மேக்ரோஸ்கோபிக் அமைப்பின் நிலை என்ன சமநிலை நிலைமைகளின் கீழ் இது வெப்ப இயக்கவியல் மாறிகள் எனப்படும் அளவுகளால் குறிப்பிடப்படுகிறது. இந்த மாறிகள் அனைத்தும் எங்களுக்குத் தெரியும், அவை வெப்பநிலை, அழுத்தம், அளவு மற்றும் வேதியியல் கலவை. இந்த மாறிகள் அனைத்தும் அமைப்புகளையும் அவற்றின் சமநிலையையும் வரையறுக்கின்றன. வேதியியல் வெப்ப இயக்கவியலில் உள்ள முக்கிய குறிப்புகள் பயன்படுத்தப்பட்ட சர்வதேச தொழிற்சங்கத்திற்கு நன்றி. இந்த அலகுகள் மூலம் வெப்ப இயக்கவியலின் சட்டத்தை சிறப்பாகச் செயல்படுத்தவும் விளக்கவும் முடியும்.
இருப்பினும், வெப்ப இயக்கவியலின் ஒரு கிளை உள்ளது, அது சமநிலையைப் படிக்கவில்லை, ஆனால் முக்கியமாக வகைப்படுத்தப்படும் வெப்ப இயக்கவியல் செயல்முறைகளை பகுப்பாய்வு செய்வதற்கான பொறுப்பு ஒரு நிலையான வழியில் சமநிலை நிலைமைகளை அடைவதற்கான திறன் இல்லை.
சட்டங்கள்
XNUMX ஆம் நூற்றாண்டில் ஈசா அந்த கொள்கைகளை கண்டனம் செய்தார் அனைத்து மாற்றங்களையும் ஒழுங்குபடுத்துவதற்கும் அவற்றின் முன்னேற்றத்திற்கும் அவர்கள் பொறுப்பாவார்கள். உண்மையான கருத்தாக்கத்தைப் பெறுவதற்கு உண்மையான வரம்புகள் என்ன என்பதையும் அவை பகுப்பாய்வு செய்கின்றன. அவை நிரூபிக்க முடியாத ஆனால் அனுபவத்தின் அடிப்படையில் நிரூபிக்க முடியாத கோட்பாடுகள். வெப்ப இயக்கவியலின் ஒவ்வொரு கோட்பாடும் இந்த கொள்கைகளை அடிப்படையாகக் கொண்டது. நாம் 3 அடிப்படைக் கோட்பாடுகளையும் கொள்கையையும் வேறுபடுத்திப் பார்க்க முடியும், ஆனால் அதுதான் வெப்பநிலையை வரையறுக்கிறது, மற்ற 3 கொள்கைகளில் இது மறைமுகமாக உள்ளது.
பூஜ்ஜிய சட்டம்
இந்த பூஜ்ஜிய சட்டம் என்ன என்பதை நாம் விவரிக்கப் போகிறோம், இது மீதமுள்ள கொள்கைகளில் உள்ளார்ந்த வெப்பநிலையை முதலில் விவரிக்கிறது. இரண்டு அமைப்புகள் ஒருவருக்கொருவர் தொடர்புகொண்டு வெப்ப சமநிலையில் இருக்கும்போது அவை சில பண்புகளைப் பகிர்ந்து கொள்கின்றன. அவர்கள் ஒருவருக்கொருவர் பகிர்ந்து கொள்ளும் இந்த பண்புகளை அளவிடலாம் மற்றும் ஒரு எண் மதிப்பைக் கொடுக்கலாம். இதன் விளைவாக, இரண்டு அமைப்புகளும் மூன்றில் ஒரு பகுதியுடன் சமநிலையில் இருந்தால், அவை ஒருவருக்கொருவர் சமநிலையில் இருக்கும் மற்றும் பகிரப்படும் சொத்து வெப்பநிலை.
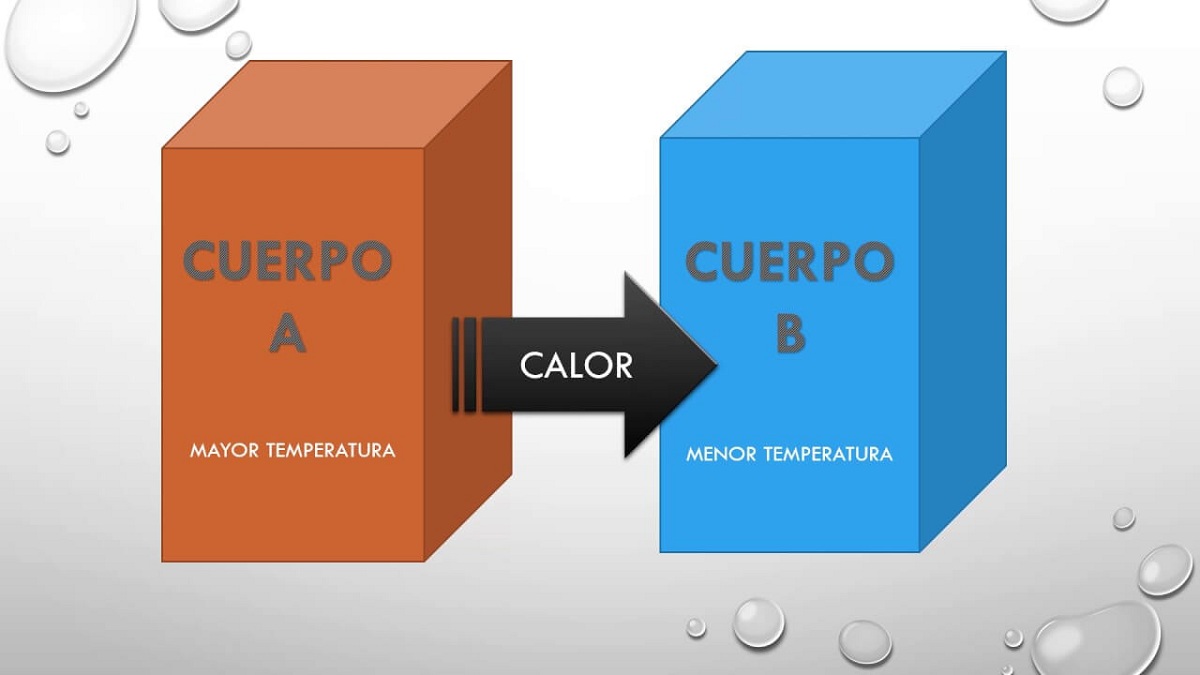
எனவே, இந்த கொள்கை ஆனால் வெறுமனே என்று கூறுகிறது ஒரு உடல் A உடல் B உடன் சமநிலையில் இருந்தது, இந்த உடல் B ஒரு உடல் C உடன் வெப்ப சமநிலையில் இருக்கும், பின்னர் A மற்றும் C உடல்களும் சமநிலையில் இருக்கும் வெப்ப. வெவ்வேறு வெப்பநிலையில் உள்ள இரண்டு உடல்கள் ஒருவருக்கொருவர் வெப்பத்தை பரிமாறிக் கொள்ளலாம் என்ற உண்மையை இந்த கொள்கை விளக்குகிறது. விரைவில் அல்லது பின்னர் இரு உடல்களும் ஒரே வெப்பநிலையை அடைகின்றன, எனவே அவை மொத்த சமநிலையில் உள்ளன.
வெப்ப இயக்கவியலின் முதல் விதி
ஒரு உடல் குளிர்ச்சியான உடலுடன் தொடர்பு கொள்ளும்போது, ஒரு மாற்றம் நிகழ்கிறது, அது சமநிலையின் நிலைக்கு இட்டுச் செல்கிறது. குளிர்ந்த உடலுக்கான சூடான உடலுக்கு இடையில் ஆற்றல் பரிமாற்றம் மேம்படுத்தப்படுவதால் இரு உடல்களின் வெப்பநிலை சமமாக இருக்கும் என்ற உண்மையை அடிப்படையாகக் கொண்டது இந்த சமநிலை நிலை. இந்த நிகழ்வை விளக்கும் பொருட்டு, விஞ்ஞானிகள் அதிக அளவு இருக்கும் ஒரு சூடான பொருள், குளிர்ந்த உடலைக் கடந்து சென்றதாக கருதினர். வெப்பத்தை பரிமாறிக்கொள்ள வெகுஜன வழியாக நகரக்கூடிய ஒரு திரவம் என்று கருதப்பட்டது.
வெப்பத்தை ஆற்றலின் வடிவமாக அடையாளம் காண இந்த கொள்கை பொறுப்பாகும். இது ஒரு பொருள் பொருள் அல்ல. இந்த வழியில், கலோரிகளிலும் வேலைகளிலும் அளவிடப்படும் வெப்பம், ஜூல்களில் அளவிடப்படுகிறது என்பதைக் காட்டலாம். எனவே, அது இன்று நமக்குத் தெரியும் 1 கலோரி சுமார் 4,186 ஜூல்கள் ஆகும்.
வெப்ப இயக்கவியலின் முதல் கொள்கை ஆற்றலைப் பாதுகாப்பதற்கான ஒரு கொள்கை என்று கூறலாம். ஒரு வெப்ப இயந்திரத்தில் உள்ள ஆற்றலின் அளவு வேலையாக மாற்றப்படுகிறது மற்றும் ஆற்றலை நுகராமல் அத்தகைய வேலையை உருவாக்கக்கூடிய எந்திரத்தால் பார்க்க முடியும். இந்த முதல் கொள்கையை நாம் இவ்வாறு நிறுவலாம்: ஒரு மூடிய வெப்ப இயக்கவியல் அமைப்பின் உள் ஆற்றலின் மாறுபாடு அமைப்புக்கு வழங்கப்படும் வெப்பத்திற்கும் சூழலில் கூறப்பட்ட அமைப்பால் செய்யப்படும் வேலைக்கும் இடையிலான வேறுபாட்டிற்கு சமம்.
வெப்ப இயக்கவியலின் இரண்டாவது விதி
குளிர்ந்த உடலில் இருந்து வெப்பமான உடலுக்கு வெப்பத்தை மாற்றுவதன் மூலம் மட்டுமே சுழற்சி இயந்திரத்தை உருவாக்க முடியாது என்று இது ஆரம்பத்தில் கூறுகிறது. ஒரு உருமாற்றம் செய்ய இயலாது என்று நாம் கூறலாம், அதன் முடிவு மட்டுமே இருக்கும் ஒரு மூலத்திலிருந்து நாம் பிரித்தெடுத்த வெப்பத்தை இயந்திர வேலைகளாக மாற்றுவது.
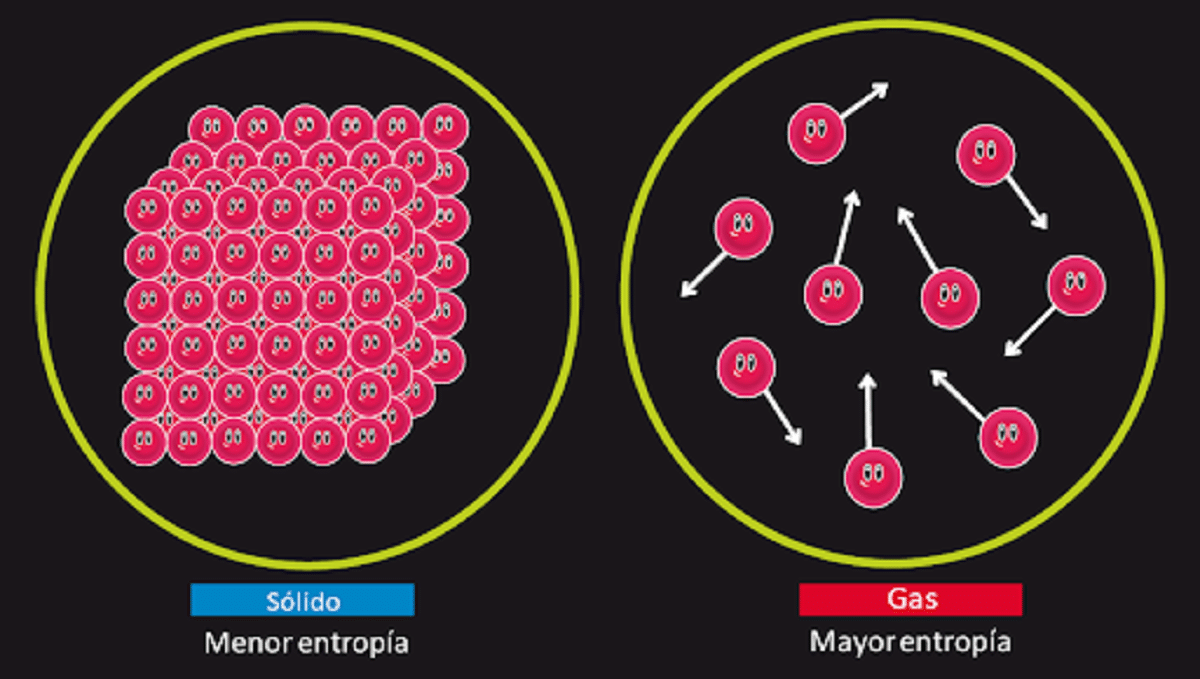
இரண்டாவது இனத்தின் நன்கு அறியப்பட்ட நிரந்தர இயக்கம் இருப்பதற்கான வாய்ப்பை மறுப்பதற்கு இந்த கொள்கை காரணமாகும். என்று எங்களுக்குத் தெரியும் என்ட்ரோபி மீளக்கூடிய மாற்றம் நிகழும்போது ஒரு அமைப்பின் மாற்றமின்றி தனிமைப்படுத்தப்படுகிறது. மீளமுடியாத மாற்றம் நிகழும்போது அது அதிகரிக்கிறது என்பதையும் நாங்கள் அறிவோம்.
வெப்ப இயக்கவியலின் மூன்றாவது விதி
இந்த கடைசி கொள்கை இரண்டாவதாக நெருக்கமாக தொடர்புடையது மற்றும் அதன் விளைவாக கருதப்படுகிறது. இந்த கோட்பாடு ஒரு முழுமையான எண்ணிக்கையிலான மாற்றங்களுடன் நிறத்தில் அடைய முடியாது என்பதை உறுதிப்படுத்துகிறது. முழுமையான பூஜ்ஜியம் இருப்பதை நாம் அறிவோம், அடையக்கூடிய குறைந்தபட்ச வெப்பநிலையை விட அதிகமாக இல்லை. அலகுகளில் கெல்வின் அது 0 என்று நமக்குத் தெரியும், ஆனால் டிகிரி செல்சியஸில் -273.15 டிகிரி மதிப்பு உள்ளது.
0 கெல்வின் வெப்பநிலையுடன் ஒரு படிகமாக இருக்கும் ஒரு திடத்திற்கான என்ட்ரோபி 0 க்கு சமம் என்றும் இது கூறுகிறது. இதன் பொருள் எந்த என்ட்ரோபியும் இருக்காது, எனவே கணினி முற்றிலும் நிலையானதாக இருக்கும். 0 கெல்வின் வெப்பநிலையில் அதை உருவாக்கும் துகள்களின் விடுதலை, மொழிபெயர்ப்பு மற்றும் சுழற்சியின் ஆற்றல் எதுவும் இருக்காது.
இந்த தகவலுடன் நீங்கள் வெப்ப இயக்கவியல் மற்றும் அடிப்படைக் கொள்கைகளைப் பற்றி மேலும் அறியலாம் என்று நம்புகிறேன்.