
После познанства Тхомсон-ов атомски модел, који је сматрао да се електрони налазе у позитивно наелектрисаном медијуму, напреднијем моделу познатом као Рутхерфорд-ов атомски модел. Научник задужен за овај нови напредак у науци био је Ернест Рутхерфорд. Рођен је 20. августа 1871. године, а умро 19. октобра 1937. Током свог живота дао је велики допринос хемији и свету науке уопште.
Стога ћемо посветити овај чланак да бисмо вам испричали све што треба да знате о Рутхерфордовом атомском моделу.
Експеримент са златним лишћем
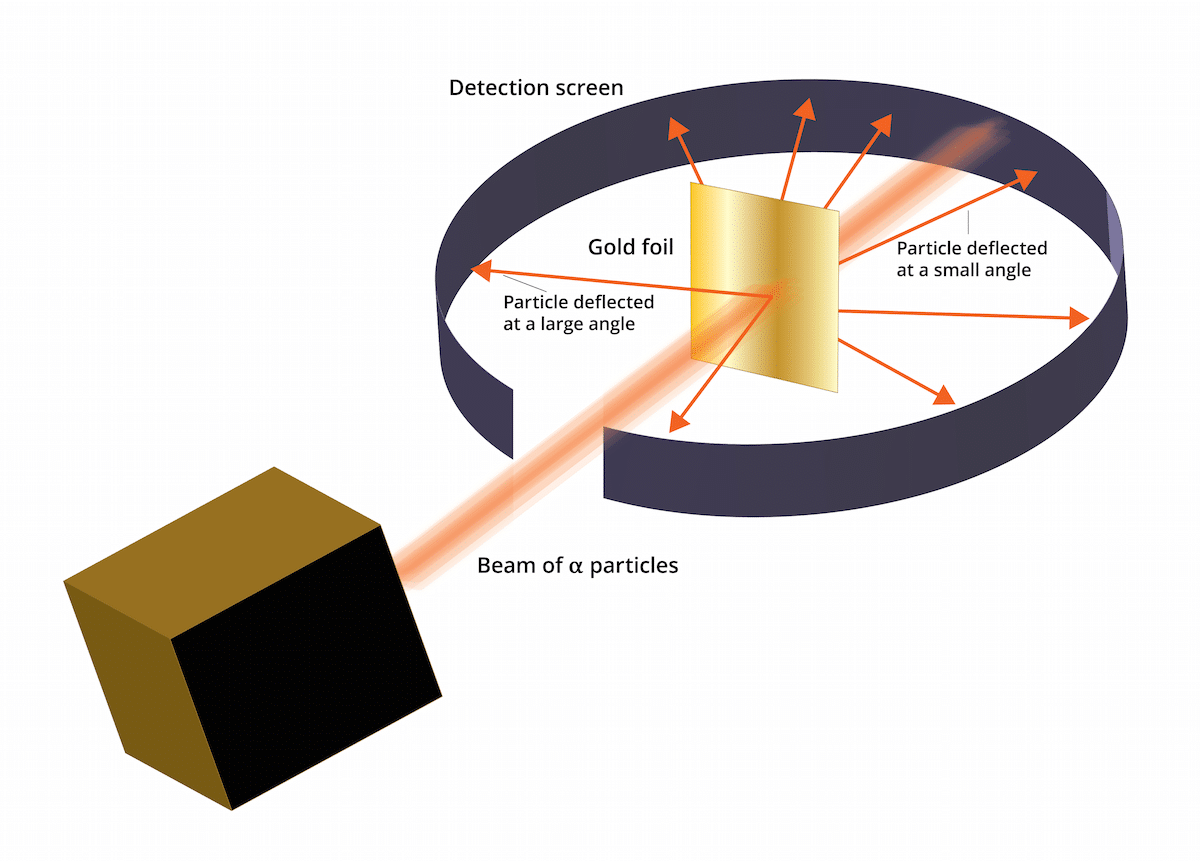
Стари Томсонов модел рекао је да су се електрони налазили у позитивно наелектрисаном медијуму. 1909. године Ернест Рутхерфорд, у пратњи два помоћника по имену Геигер и Марсден, урадио је студију познату као експеримент Златног лишћа где су могли да провере да ли Томсонов добро познати „пудинг од грожђица“ је погрешио. И управо је тај нови експеримент успео да покаже да је атом имао структуру са јаким позитивним наелектрисањем. Овај експеримент није могао да помогне да се поново успоставе неки закључци који су на крају представљени као Рутхерфордов атомски модел 1911. године.
Експеримент познат као Златни лист није био јединствен, али је спроведен између 1909. и 1913. За ово су користили физичке лабораторије Универзитета у Манчестеру. Ови експерименти су били од велике важности, јер су се на основу њихових резултата могли успоставити нови закључци, што је довело до револуционарног атомског модела.
Овај експеримент се састојао од следећег: танки лим злата дебео само 100 нм морао је бити бомбардиран великом количином алфа честица. Те алфа честице су биле и јони. Односно, атоми који немају електроне, па су имали само протоне и неутроне. Имајући неутроне и протоне, укупан набој атома био је позитиван. Циљ овог експеримента је углавном био да потврди да ли је Томсонов модел тачан. Ако је овај модел био у праву, алфа честице су морале да пролазе кроз атоме злата у правој линији.
Да би се проучило отклон узрокован алфа честицама, око фине златне фолије морао се поставити флуоресцентни филтер цинк сулфида. Резултат овог експеримента је да је примећено да су неке честице могле да пролазе кроз златне атоме лима у правој линији. Међутим, неке од ових алфа честица биле су скренуте у случајним правцима.
Закључци експеримента са златним листом

С обзиром на ову чињеницу, није било могуће поткрепити оно што се сматрало претходним атомским моделима. А управо су ови атомски модели истакли да је позитивно наелектрисање равномерно распоређено у атомима и то би олакшало његово прелазак, јер његово наелектрисање у одређеном тренутку не би било толико јако.
Резултати овог експеримента са златним листом били су потпуно неочекивани. То је натерало Рутхерфорда да помисли да атом има центар са јаким позитивним набојем који ствара алфа честицу покушајте да је издате одбачене од централне структуре. Да би се утврдио поузданији извор, узете су у обзир честице које су се одбијале и оне које нису. Захваљујући овом одабиру честица, било је могуће одредити величину језгра у поређењу са орбитом електрона око њега. Такође би се могло закључити да је већи део простора атома празан.
Могло се видети, неке алфа честице су биле скренуте златном фолијом. Неки од њих су одступали само под врло малим угловима. Ово је помогло да се закључи да позитивно наелектрисање на атому није равномерно распоређено. Односно, позитивно наелектрисање се налази на атому концентрисано у врло малој запремини простора.
Веома мало алфа честица се вратило уназад. Ово одступање указује на следеће да су се поменуте честице могле одскочити. Захваљујући свим овим новим разматрањима, Рутхерфордов атомски модел могао би се успоставити новим идејама.
Рутхерфорд-ов атомски модел

Проучићемо који су принципи Рутхерфордовог атомског модела:
- Честице које имају позитивно наелектрисање унутар атома распоређени су у врло малој запремини ако је упоредимо са укупном запремином поменутог атома.
- Готово сва маса коју има атом налази се у тој малој поменутој запремини. Ова унутрашња маса названа је језгро.
- Електрони који имају негативне наелектрисања налазе се ротирајући око језгра.
- Електрони се окрећу великом брзином када су око језгра и то кружно. Те путање називале су се орбите. Касније хоћу познате су као орбитале.
- И они електрони који су били негативно наелектрисани и језгро самог позитивно наелектрисаног атома увек се држе заједно захваљујући електростатичкој привлачној сили.
Прихватање и ограничења Рутхерфордовог атомског модела
Као што се и очекивало, овај нови модел је замислио потпуно нову панораму атома у научном свету. Захваљујући овом атомском моделу, многи каснији научници могли су да проуче и утврде број електрона који има сваки елемент у периодном систему. Поред тога, могла би се доћи до нових открића која помажу на најједноставнији начин објаснити функционисање атома.
Међутим, овај модел такође има одређена ограничења и грешке. Иако је то био пробој у свету физике, они нису били ни савршени ни потпуни модел. И да ли је то од према Њутновим законима и важном аспекту Максвелових закона, овај модел није могао објаснити одређене ствари:
- Није могао да објасни како су негативни набоји могли да се држе заједно у језгру. Према електронској тибији, позитивни набоји морају да се одбијају.
- Друга контрадикција била је према основним законима електродинамике. Ако се сматрало да се електрони са позитивним наелектрисањем ротирају око језгра, они би требало да емитују електромагнетно зрачење. Емитовањем овог зрачења троши се енергија да се електрони сруше у језгру. Према томе, пругасти атомски модел не може објаснити стабилност атома.
Надам се да ћете са овим информацијама сазнати више о Рутхерфордовом атомском моделу.