
У науци је било много научника који су направили разлику када је реч о сазнању како ствари функционишу. Знање о честицама, атомима и електронима пружило је много напретка у науци. Стога ћемо овај чланак посветити Тхомсон-ов атомски модел. Такође је био познат и као модел пудинга од сувог грожђа.
У овом чланку можете научити све везано за Тхомсонов атомски модел, које су његове карактеристике и колико је то било важно за науку.
Шта је Тхомсон-ов атомски модел

Ово је модел који је развијен 1904. године и можда је откривена прва субатомска честица. Откривач је био британски научник Џозеф Џон Томсон. Овај човек је успео да открије негативно наелектрисане честице експериментом у којем је користио катодне цеви 1897. године.
Последица овог открића била је прилично огромна, јер није било доказа да атом може имати језгро. Овај научник нас наводи на помисао да су електрони уроњени у неку врсту позитивно наелектрисане супстанце која се супротставља негативном наелектрисању електрона. Због тога су атоми имали неутрални набој.
Објаснити их на разумљив начин је попут стављања желеа са грожђицама које лебде унутра. Отуда име модела пудинг са сувим грожђем. У овом моделу, Тхомсон био задужен за називање електронских телесних целица и сматрао је да су они распоређени на не случајан начин. Данас је познато да су они у некој врсти ротирајућих прстенова и да сваки прстен има другачији ниво енергије. Када електрон изгуби енергију, прелази на виши ниво, односно удаљава се од језгра атома.
Експеримент са златном фолијом

Томпсон је мислио да позитивни део атома увек остаје на неодређено време. Овај модел који је створио 1904. године није имао широко прихваћено академско прихватање. Пет година касније Геигер и Марсден могли су да изведу експеримент са златном фолијом због чега Тхомсонова открића нису била толико ефикасна. У овом експерименту су прошли сноп честица хелијум алфа кроз златну фолију. Алфа честице нису ништа друго до лавови елемента, односно језгра која немају електроне и зато имају позитиван набој.
Резултат експеримента је био да се овај сноп расејао пролазећи кроз златну фолију. Овим би се могло закључити да мора постојати језгро са извором позитивног наелектрисања одговорно за одбијање снопа светлости. С друге стране, у Томсоновом атомском моделу имали смо да је позитивно наелектрисање распоређено дуж онога што је речено као желатина и који садржи електроне. То значи да би сноп јона могао проћи кроз атом тог модела.
Када се у следећем експерименту показало супротно, овај модел би могао бити негиран атомска.
Откриће електрона такође је дошло из дела другог атомског модела, али из Далтона. У том моделу, атом се сматрао потпуно недељивим. То је оно што је подстакло Тхомсона да размисли о свом моделу пудинга од сувог грожђа.
Карактеристике Тхомсоновог атомског модела
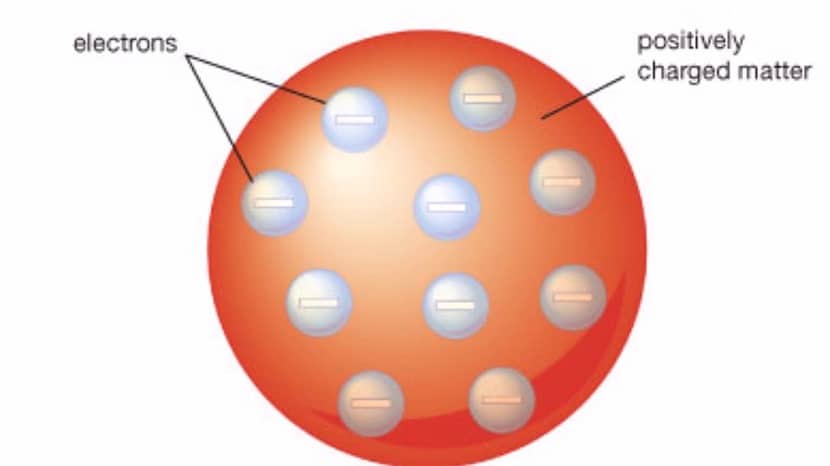
Међу главним карактеристикама овог модела сумирамо следеће:
- Атом који овај модел представља подсећа на сферу која има позитивно наелектрисан материјал са електронима који су негативно набијени. И електрони и позитивно наелектрисана материја присутни су унутар сфере.
- Позитивни и негативни набој имају исту величину. То значи да читав атом нема наелектрисање, већ је електрично неутралан.
- Тако да атом уопште може имати неутрално наелектрисање електрони треба да буду уроњени у супстанцу која има позитиван набој. То је оно што је поменуто са сувим грожђем као делом електрона, а остатак желатине је део са позитивним наелектрисањем.
- Иако то није експлицитно објашњено, може се закључити да у овом моделу атомско језгро није постојало.
Када је Тхомсон створио овај модел, напустио је претходну хипотезу о небуларном атому. Ова хипотеза се заснивала на чињеници да су атоми састављени од нематеријалних вртлога. Будући да је био успешан научник, желео је да створи свој атомски модел заснован на експерименталним доказима који су били познати у његово време.
Упркос чињеници да овај модел није био сасвим тачан, успео је да помогне у постављању фиксних темеља како би каснији модели могли бити успешнији. Захваљујући овом моделу било је могуће изводити различите експерименте који су довели до нових закључака и тако се наука коју данас познајемо развијала све више и више.
Ограничења и грешке Тхомсоновог атомског модела
Анализираћемо која су то питања у којима овај модел није постигао циљ и због тога није могао да иде напред. Прва ствар је да није могао да објасни како се наелектрисања држе на електронима унутар атома. Не могавши то да објасни, такође није могао да реши ништа о стабилности атома.
У својој теорији није поменуо ништа о атому који поседује језгро. Да смо данас знали да се атом састоји од језгро састављено од протона и неутрона и електрона ротира око себе на различитим нивоима енергије.
Протони и неутрони још увек не би били откривени. Томпсон је свој модел покушао да заснива на објашњењу са елементима који су у то време били научно доказани. Када је експеримент са златном фолијом верификован, брзо је одбачен. У овом експерименту је показано да унутар атома мора постојати нешто због чега би имао позитиван набој и већу масу. За ово се већ зна да је језгро атома.
Надам се да ћете са овим информацијама сазнати више о Томсоновом атомском моделу.