
當然,您曾經看過 玻爾原子模型。 這是這位科學家為科學特別是電磁學和電化學學做出的重要發現。 以前有盧瑟福的模型,該模型具有革命性並且非常成功,但是與其他原子定律(例如麥克斯韋定律和牛頓定律)存在一些衝突。
在本文中,我們將告訴您有關玻爾原子模型需要了解的所有信息,以及其詳細信息,以澄清對該主題的任何疑問。
它幫助解決的問題
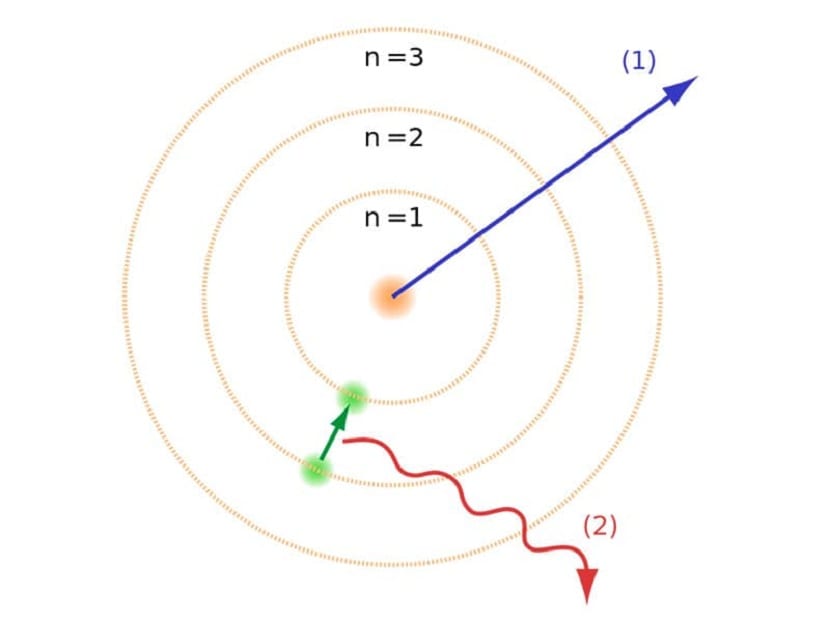
正如我們在本文開頭提到的那樣,此原子模型有助於解決與其他原子定律存在的某些衝突。 在以前的盧瑟福模型中,我們不得不 帶負電荷運動的電子必鬚髮出一種電磁輻射。 由於外面的電磁定律,應該做到這一點。 能量的損失導致電子通過向中心盤旋而減少到其軌道。 當他們到達中心時,他們崩潰了,與核心碰撞。
這在理論上產生了一個問題,因為它無法隨原子核崩潰,但電子的軌跡必須不同。 這是通過玻爾原子模型解決的。 它解釋說 電子圍繞原子核在某些允許的軌道上運動,並具有特定的能量。 能量與普朗克常數成正比。
我們已經提到的這些軌道在電子移動的地方被稱為能量層或能級。 即,電子具有的能量並不總是相同,而是被量化的。 量子能級是發現原子的不同軌道。 根據在任何給定時刻它所處的軌道,它將具有或多或少的能量。 靠近原子核的軌道具有更大的能量。 另一方面,離原子核越遠,能量越少。
能級模型
這個玻爾原子模型暗示電子只能從一個軌道跳到另一個軌道而獲得或失去能量,這有助於解決盧瑟福模型提出的崩潰。 當從一個能級移動到另一個能級時,它會吸收或發射電磁輻射。 也就是說,當您從電量較高的電量躍升至電量較低的電量時,您會釋放多餘的電量。 相反,當它從低能級變為高能級時,它會吸收電磁輻射。
由於此原子模型是對盧瑟福模型的修改,因此保留了小的中心核的特徵以及大部分原子的質量。 儘管電子的軌道並不像行星的軌道那樣平坦,但可以說這些電子繞其原子核旋轉的方式與行星繞太陽旋轉的方式類似。
玻爾的原子模型原理

現在,我們將分析此原子模型的原理。 關於所述模型及其操作的詳細說明。
- 帶正電的粒子 與原子的總體積相比,它們的濃度低。
- 帶有負電荷的電子是被發現圍繞核以圓形能量軌道旋轉的電子。
- 電子在軌道上存在能級循環。 它們也具有設定的大小,因此在軌道之間沒有中間狀態。 他們只是從一個級別轉到另一個級別。
- 每個軌道擁有的能量與其大小有關。 軌道離原子核越遠,它擁有的能量就越多。
- 能級具有不同數量的電子。 能級越低,它包含的電子越少。 例如,如果我們處於第2級,則最多會有兩個電子。 在第8級,最多可以有XNUMX個電子,依此類推。
- 當電子從一個軌道移動到另一個軌道時,它們吸收或釋放電磁能。 如果您從一個以上的能量水平降低到另一個以下的能量水平,則會釋放剩餘的能量,反之亦然。
該模型是革命性的,試圖為以前的模型所沒有的材料賦予穩定性。 該原子模型還解釋了氣體的離散發射光譜和吸收光譜。 它是第一個引入量化或量化概念的模型。 這使玻爾的原子模型成為介於經典力學和量子力學之間的模型。 儘管它也有缺點,但它是薛定ding和其他科學家後來的量子力學的先驅模型。
玻爾原子模型的局限性和錯誤
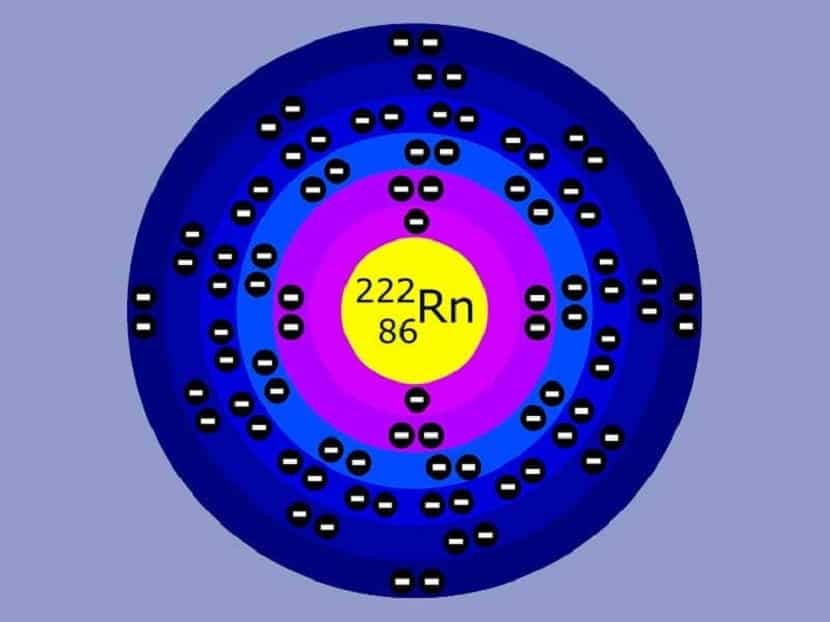
正如我們已經提到的,該模型還存在某些缺點和錯誤。 首先,它沒有解釋或給出為什麼電子應僅限於特定軌道的原因。 它直接假設電子具有已知的半徑和軌道。 但是,事實並非如此。 十年後 海森堡的不確定性原理反駁了這一點。
儘管此原子模型能夠模擬氫原子中電子的行為,但涉及到具有更高電子數的元素時,它並不是那麼精確。 這是一個模型 難以解釋塞曼效應。 當在外部磁場和靜態磁場的作用下將譜線分成兩個或多個時,可以看到這種效果。
該模型的另一個錯誤和局限性是,它為基態軌道的角動量提供了不正確的值。 提到的所有這些錯誤和限制導致玻爾的原子模型在數年後被量子理論所取代。
我希望通過本文,您可以了解有關玻爾原子模型及其在科學中的應用的更多信息。