
你见过 玻尔原子模型。 这是这位科学家为科学特别是电磁学和电化学学做出的重要发现。 以前有卢瑟福(Rutherford)模型,它非常具有革命性并且非常成功,但是与其他原子定律(例如麦克斯韦定律和牛顿定律)存在一些冲突。
在本文中,我们将告诉您有关玻尔原子模型需要了解的所有信息,以及其细节,以澄清对该主题的任何疑问。
它帮助解决的问题
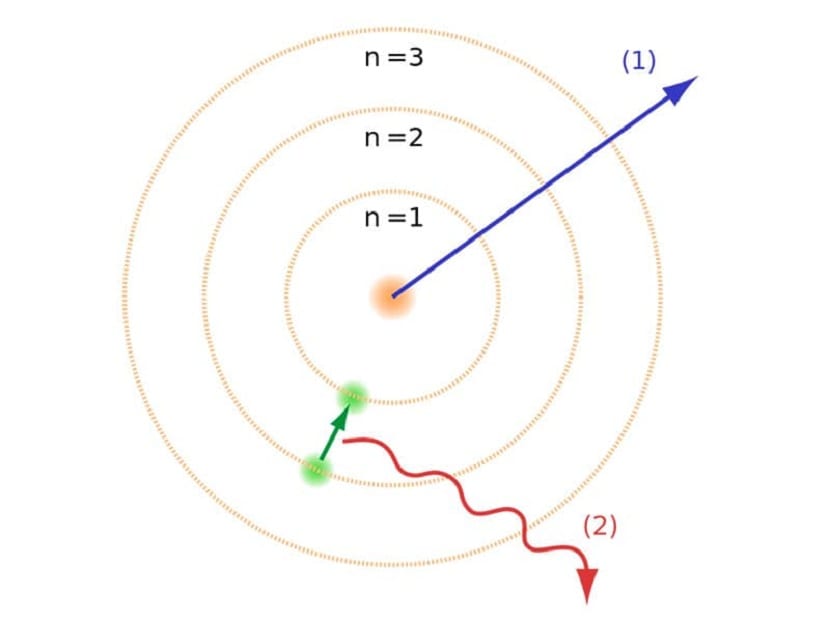
正如我们在本文开头提到的那样,此原子模型有助于解决与其他原子定律存在的某些冲突。 在以前的卢瑟福模型中,我们不得不 带负电荷运动的电子必须发出一种电磁辐射。 由于外面的电磁定律,应该做到这一点。 能量的损失导致电子通过向中心盘旋而减少到其轨道。 当他们到达中心时,他们崩溃了,与核心碰撞。
这在理论上产生了一个问题,因为它无法随原子核崩溃,但电子的轨迹必须不同。 这是通过玻尔原子模型解决的。 它解释说 电子以允许的且具有特定能量的某些轨道围绕核运动。 能量与普朗克常数成正比。
我们已经提到的这些轨道在电子移动的地方被称为能量层或能级。 即,电子具有的能量并不总是相同,而是被量化的。 量子能级是原子所处的不同轨道。 根据在任何给定时刻它所处的轨道,它将具有或多或少的能量。 靠近原子核的轨道具有更大的能量。 另一方面,它们越远离核,能量就越少。
能级模型
这个玻尔原子模型暗示电子只能从一个轨道跳到另一个轨道而获得或失去能量,这有助于解决卢瑟福模型提出的崩溃。 当从一个能级移动到另一个能级时,它会吸收或发射电磁辐射。 也就是说,当您从电量较高的电量跃升至电量较低的电量时,您会释放多余的电量。 相反,当它从低能级变为高能级时,它会吸收电磁辐射。
由于此原子模型是对卢瑟福模型的修改,因此保留了小的中心核的特征以及大部分原子的质量。 尽管电子的轨道并不像行星的轨道那样平坦,但是可以说这些电子绕其原子核旋转的方式与行星绕太阳旋转的方式类似。
玻尔的原子模型原理

现在,我们将分析此原子模型的原理。 关于所述模型及其操作的详细说明。
- 带正电的粒子 与原子的总体积相比,它们的浓度低。
- 带有负电荷的电子是被发现围绕核以圆形能量轨道旋转的电子。
- 电子在轨道上存在能级循环。 它们也具有设定的大小,因此在轨道之间没有中间状态。 他们只是从一个级别转到另一个级别。
- 每个轨道拥有的能量与其大小有关。 轨道离原子核越远,它拥有的能量就越多。
- 能级具有不同数量的电子。 能级越低,它包含的电子越少。 例如,如果我们处于第2级,则最多会有两个电子。 在第8级,最多可以有XNUMX个电子,依此类推。
- 当电子从一个轨道移动到另一个轨道时,它们吸收或释放电磁能。 如果您从一个更高的能量水平降低到另一个,则释放过多的能量,反之亦然。
该模型是革命性的,试图为以前的模型所没有的材料赋予稳定性。 该原子模型还解释了气体的离散发射光谱和吸收光谱。 它是第一个引入量化或量化概念的模型。 这使玻尔的原子模型成为介于经典力学和量子力学之间的模型。 尽管它也有缺点,但它是薛定ding和其他科学家后来的量子力学的先驱模型。
玻尔原子模型的局限性和错误
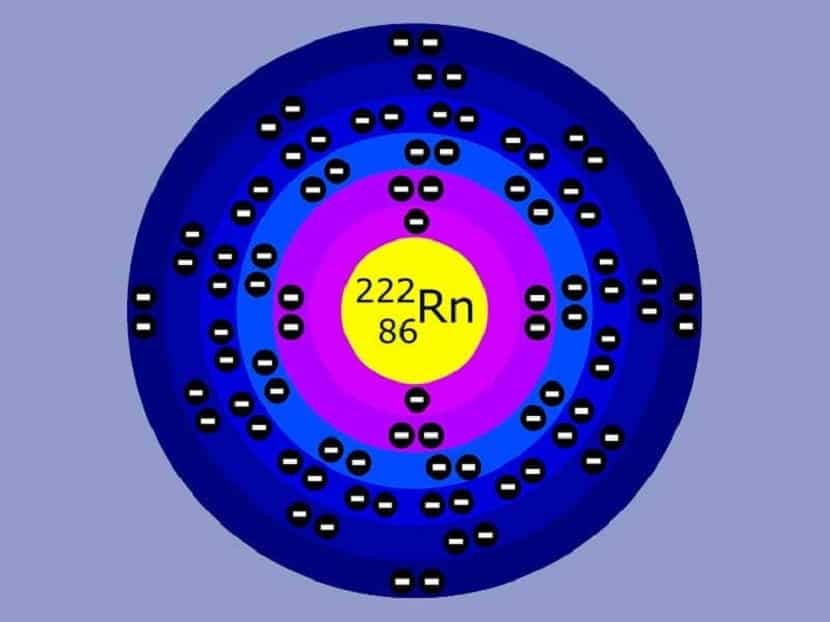
正如我们已经提到的,该模型还存在某些缺点和错误。 首先,它没有解释或给出为什么电子应仅限于特定轨道的原因。 它直接假设电子具有已知的半径和轨道。 但是,事实并非如此。 十年后 海森堡的不确定性原理反驳了这一点。
尽管此原子模型能够模拟氢原子中电子的行为,但涉及到具有更高电子数的元素时,它并不是那么精确。 这是一个模型 难以解释塞曼效应。 当在外部磁场和静态磁场的作用下将谱线分成两个或多个时,可以看到这种效果。
该模型的另一个错误和局限性是,它为基态轨道的角动量提供了不正确的值。 提到的所有这些错误和限制导致玻尔的原子模型在数年后被量子理论所取代。
我希望通过本文,您可以了解有关玻尔原子模型及其在科学中的应用的更多信息。