Fizik alanında, sistemde ısı ve iş tarafından üretilen dönüşümleri incelemekle görevli bir dal vardır. Termodinamikle ilgili. Sadece makro düzeyde sıcaklık ve enerji durum değişkenlerindeki değişiklikleri içeren bir sürecin sonucu olan tüm geçişlerin incelenmesinden sorumlu olan bir fizik dalıdır. Bir kaç tane var termodinamiğin ilkeleri fiziğin birçok yönü için temel olan.
Bu nedenle bu yazımızda sizlere termodinamiğin ilkelerini ve önemini anlatacağız.
Termodinamiğin özellikleri
Klasik termodinamiği analiz edersek, onun makroskopik sistemler kavramına dayandığını görürüz. Bu sistem, dış çevreden ayrılmanın fiziksel veya kavramsal niteliğinin yalnızca bir parçasıdır. Termodinamik sistemi daha iyi incelemek için her zaman fiziksel bir kütle olduğu varsayılır. dış ekosistem ile enerji alışverişinden rahatsız olmaz.
Makroskopik bir sistemin dengedeki durumu, termodinamik değişkenler adı verilen niceliklerle belirlenir. Tüm bu değişkenleri biliyoruz: sıcaklık, basınç, hacim ve kimyasal bileşim. Bütün bu değişkenler sistemi ve onun dengesini tanımlar. Uluslararası uygulama ittifakı sayesinde, kimyasal termodinamiğin ana sembolleri oluşturulmuştur. Bu birimleri kullanmak daha iyi çalışabilir ve termodinamiğin ilkelerini açıklayabilir.
Sin ambargo, dengeyi incelemeyen bir termodinamik dalı vardır, Aksine, esas olarak denge koşullarını kararlı bir şekilde elde etme kabiliyetine sahip olmama ile karakterize edilen termodinamik süreçleri analiz etmekten sorumludurlar.
termodinamiğin ilkeleri
Termodinamiğin sıfırdan üçe kadar sıralanmış 4 ilkesi vardır, bu yasalar evrenimizdeki tüm fizik yasalarını anlamamıza yardımcı olur ve dünyamızda belirli fenomenleri görmek imkansızdır. Ayrıca termodinamik yasaları adıyla da bilinirler. Bu kanunların farklı kökenleri vardır. Bazıları önceki formüllerden formüle edilmiştir. Termodinamiğin bilinen son yasası sıfır yasasıdır. Laboratuvarda yapılan tüm araştırma ve incelemelerde bu yasalar kalıcıdır. Evrenimizin nasıl çalıştığını anlamak için gereklidirler. Termodinamiğin ilkelerini tek tek anlatacağız.
İlk ilke
Bu yasa, enerjinin yaratılamayacağını veya yok edilemeyeceğini, yalnızca dönüştürülebileceğini söylüyor. Bu aynı zamanda enerjinin korunumu yasası olarak da bilinir. Aslında, bu, çevresinden izole edilmiş herhangi bir fiziksel sistemde, tüm enerjisinin her zaman aynı olacağı anlamına gelir. Enerji şu veya bu şekilde başka enerji türlerine dönüştürülebilmesine rağmen, tüm bu enerjilerin toplamı her zaman aynıdır.
Daha iyi anlamak için bir örnek vereceğiz. Bu ilkeye göre, fiziksel bir sisteme ısı şeklinde belirli bir miktarda enerji katarsak, iç enerjideki artış ile sistem ve çevresinin yaptığı iş arasındaki farkı bularak toplam enerjiyi hesaplayabiliriz. Yani sistemin o anda sahip olduğu enerji ile yaptığı iş arasındaki fark açığa çıkan ısı enerjisi olacaktır.
İkinci ilke
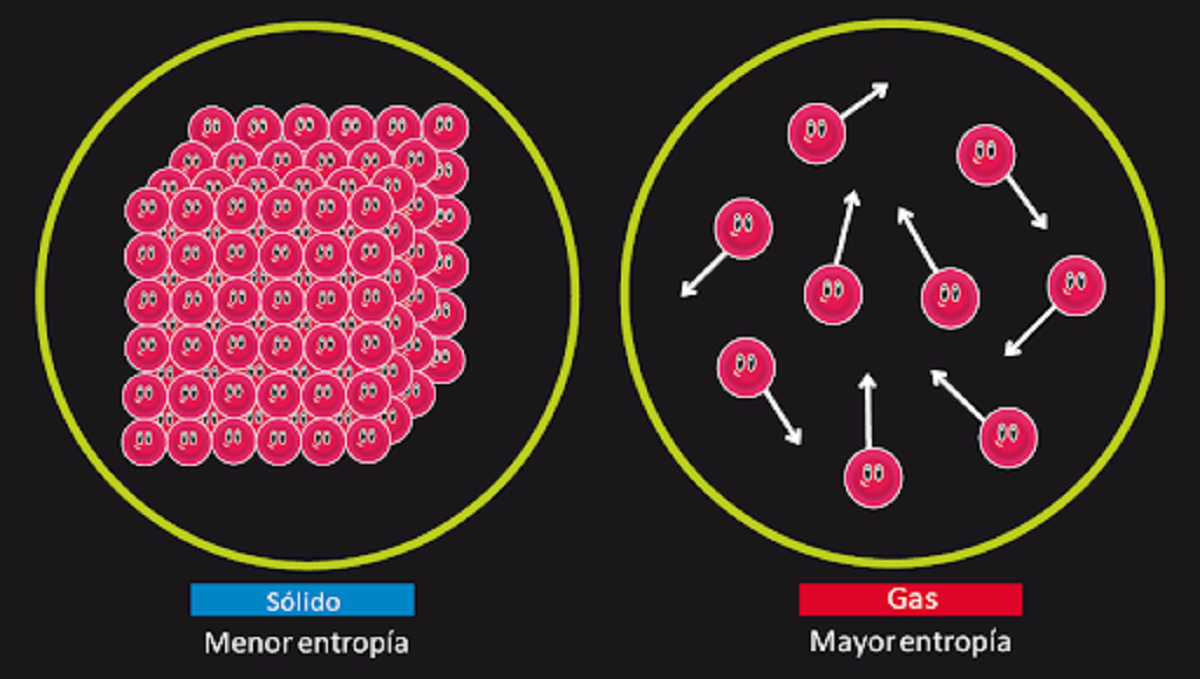
Yeterli zaman varsa, tüm sistemler sonunda dengesini kaybeder. Bu ilkeye entropi yasası da denir. Aşağıdaki gibi özetlenebilir. Evrendeki entropi miktarı zamanla artacaktır. Sistemin entropisi, düzensizliğin derecesini ölçmek için bir indekstir. Diğer bir deyişle, Termodinamiğin ikinci ilkesi bize, sistem bir kez denge noktasına ulaştığında, sistemdeki düzensizlik derecesini artıracaktır. Bu, bir sisteme yeterince zaman verirsek, sonunda dengesizleşeceği anlamına gelebilir.
Bu, bazı fiziksel olayların tersinmezliğini açıklamadan sorumlu olan yasadır. Örneğin, bir makalenin nedenini açıklamamıza yardımcı olur. bir kağıt yanmış orijinal şekline dönemez. Kağıt ve ateş olarak bilinen bu sistemde düzensizlik o kadar artmıştır ki, kökenine dönmek mümkün değildir. Bu yasa, fiziksel sistemler durumunda düzensizliğin derecesini ve kaçınılmaz enerji kaybını temsil etmekten sorumlu olan entropi durumu işlevini ortaya koymaktadır.
Termodinamiğin ikinci ilkesini anlamak için bir örnek vereceğiz. Belli bir miktar maddeyi yakıp, ortaya çıkan külle birlikte topun yanına koyarsak, başlangıçtaki halinden daha az madde olduğunu görebiliriz. Bunun nedeni, maddenin gaza dönüşmesidir. Geri alınamazlar ve dağılmaları ve dağınık olmaları gerekir. Bu şekilde, birinci durumda, ikinci durumda olduğundan daha az entropi olduğunu görüyoruz.
Üçüncü ilke
Mutlak sıfıra ulaşıldığında, fiziksel sistem süreci durur. Mutlak sıfır, ulaşabileceğimiz en düşük sıcaklıktır. Bu durumda sıcaklığı Kelvin cinsinden ölçüyoruz. Bu şekilde sıcaklığın ve soğumanın sistemin entropisinin sıfır olmasına neden olduğu söylenebilir. Bu durumlarda, daha çok kesin bir sabit gibidir. Mutlak sıfıra ulaştığında fiziksel sistem süreci durur. Bu nedenle, entropi minimum fakat sabit bir değere sahip olacaktır.
Mutlak sıfıra ulaşmak ya da ulaşmamak kolay bir iştir. Kelvin derecesinin mutlak sıfır değeri sıfırdır, ancak Santigrat sıcaklık ölçeği ölçümü, -273,15 derecedir.
Sıfır kanun
Bu yasa ikincisi varsaydı ve eğer A = C ve B = C ise, o zaman A = B olduğunu söylüyor. Bu, termodinamiğin diğer üç yasasının temel ve temel kurallarını belirler. Termal denge yasasını varsayan bir isimdir. Başka bir deyişle, sistem ve diğer sistemler birbirinden bağımsız olarak ısıl dengedeyse, ısıl dengede olmaları gerekir. Bu yasa, sıcaklık ilkelerinin oluşturulmasına izin verir. Bu ilke, bir termal denge durumunda iki farklı nesnenin termal enerjisini karşılaştırmak için kullanılır. Bu iki nesne termal dengedeyse, gereksiz yere aynı sıcaklıkta olacaklardır. Öte yandan her ikisi de üçüncü sistemin ısıl dengesini değiştirirse birbirlerini de etkilerler.
Umarım bu bilgilerle, termodinamiğin karakteristiklerinin ilkeleri hakkında daha fazla bilgi edinebilirsiniz.