Bugün nükleer enerji üretmek için kullanılan bir izotoptan bahsedeceğiz. Hakkında döteryum. Hidrojenin izotop türlerinden biridir ve D sembolü ile temsil edilir veya 2H. Yaygın olarak ağır hidrojen adı verilmiştir çünkü kütle protonun iki katıdır. Bir izotop, aynı kimyasal elementten gelen ancak farklı bir kütle numarasına sahip bir türden başka bir şey değildir. Döteryum çeşitli amaçlar için kullanılır.
Bu nedenle, bu makaleyi döteryumun tüm özelliklerini, yapısını, özelliklerini ve kullanımlarını anlatmaya adayacağız.
temel özellikleri
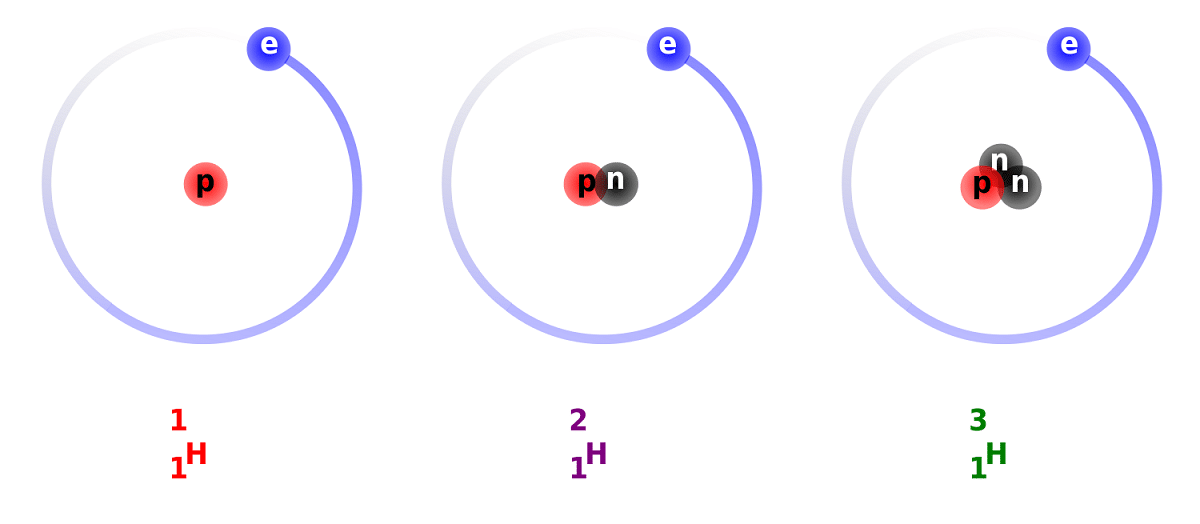
Döteryum ve hidrojen arasındaki fark, sahip olduğu nötron sayısındaki farktan kaynaklanmaktadır. Bu nedenle döteryum, kararlı bir izotop olarak kabul edilir ve tamamen doğal kaynaklı hidrojenin oluşturduğu bileşiklerde bulunabilir. Doğal kökenli olmalarına rağmen küçük bir oranda meydana geldikleri dikkate alınmalıdır. Sıradan hidrojene çok benzeyen özellikleri göz önüne alındığında, katıldığı reaksiyonlarda bütünüyle değiştirebilir. Bu şekilde muadil maddelere dönüştürülebilir.
Bu ve diğer nedenlerden dolayı döteryumun bilimin farklı alanlarında çok sayıda uygulaması vardır. Yıllar geçtikçe, teknoloji ve bilgi alanındaki araştırma ve gelişmeler için en önemli unsurlardan biri haline geldi.
Bu izotopun ana yapısı, bir proton ve bir nötron içeren bir çekirdekten oluşur. Yaklaşık 2,014 gram atom ağırlığına sahiptir. Bu izotop, Amerika Birleşik Devletleri'nden bir kimyager olan Harold C. Urey ve işbirlikçileri Ferdinand Brickwedde ve George Murphy sayesinde 1931'de keşfedildi. Döteryum'u saf haliyle karşılama hazırlıkları ilk kez 1933'te başarıyla gerçekleştirildi. Lityum döterid olarak bilinen, büyük stabilite sergileyen katı bir fazın kullanılmaya başlandığı 50'lerde zaten. Bu madde, çok sayıda kimyasal reaksiyonda döteryum ve trityumun yerini alabilir.
Bilimdeki gelişmeler, ürünlerin üretimi için kimyasal reaksiyonları kolaylaştırabilecek bir madde bulunduğunda ortaya çıkar. Bu anlamda, belirli şeyleri gözlemleyebilmek için bu izotopun bolluğunu incelediyseniz. Suda döteryum oranının numunenin alındığı alana bağlı olarak biraz değiştiği bilinmektedir. Bazı spektroskopi çalışmaları vardır. galaksimizdeki diğer gezegenlerde bu izotopun varlığını belirledik. Bu, diğer gök cisimlerinin bileşimini incelemek için büyük önem taşıyabilir.
Döteryumun yapısı ve kökeni

Döteryum hakkında bazı gerçekleri öğreneceğiz. Daha önce de belirttiğimiz gibi, hidrojen izotopları arasındaki temel fark yapılarında yatmaktadır. Ve hidrojen, döteryum ve trityum farklı miktarlarda proton ve nötron içerdiğinden, farklı kimyasal özelliklere sahip olmalarıdır. Ayrıca, diğer yıldız cisimlerinin içinde var olan döteryumun, ortaya çıktığından daha büyük bir hızla ortadan kaldırıldığını da hesaba katmalıyım. Yıldız cisimlerindeki döteryumun varlığını incelemenin bu kadar zor olmasının nedenlerinden biri budur.
Doğanın diğer fenomenlerinin küçük bir miktar döteryum oluşturduğu düşünülmektedir, bu nedenle üretimi günümüzde hatırı sayılır bir ilgi yaratmaya devam etmektedir. Doğada döteryum varlığından daha önce bahsettiğimiz yüzdeden, % 0.02'ye varmaz. Bir dizi bilimsel araştırma, döteryumdan oluşan atomların büyük çoğunluğunun doğal olarak evrenin kökenine neden olan patlamadan kaynaklandığını ortaya çıkarmıştır. Büyük patlama. Bunlar döteryumun Jüpiter gibi büyük gezegenlerde var olduğunun düşünülmesinin ana nedenlerinden biridir.
Bu izotopu doğal olarak elde etmenin en yaygın yolu, hidrojen ile birleştirilmeleridir. Bu olduğunda, protium şeklinde birleştirilecektir. Bilim adamları, oranı arasında kurulan ilişkiyi bilmekle ilgileniyorlar. döteryum ve hidrojen biliminin farklı alanlarında. Astronomi veya klimatoloji gibi bilim dallarında yaygın olarak incelenir. Bu dallarda, evreni ve atmosferimizi bilmek ve anlamak için bazı pratik araçlara sahiptir.
Döteryumun özellikleri

Hidrojene ait bu izotopun sahip olduğu temel özelliklerin neler olduğunu öğreneceğiz. Yapılacak ilk şey, radyoaktif özelliklerden yoksun bir izotopun ne olduğunu bilmektir. Bu, doğada oldukça kararlı olduğu anlamına gelir. Çeşitli kimyasal reaksiyonlarda hidrojenin yerini almak için kullanılabilir. Doğal olarak büyük bir istikrara sahip olarak, sıradan hidrojenden farklı bir davranış gösterir. Bu, biyokimyasal yapıya sahip tüm reaksiyonlarda olur. İkame etmeden önce, kimyasal reaksiyonlarda döteryum ile hidrojenin değiştirilmesiyle ulaşılabilse de, farklı bir davranışa sahip olacaklarının bilinmesi gerekir.
Sudaki iki hidrojen atomunu değiştirdiğinizde, ağır su olarak bilinen bir bileşik elde edebilirsiniz. Okyanusta bulunan ve döteryum şeklinde olan hidrojen protium ile ilgili olarak sadece% 0,016'lık bir oran sunar. Evrende, bu izotop, helyuma yol açmak için daha hızlı kaynaşma eğilimindedir. Döteryumu atomik oksijenle birleştirirsek, onun toksik bir tür haline geldiğini görürüz. Buna ve kimyasal özelliklerine veya hidrojeninkilere çok benzer olmasına rağmen.
Bu izotopun bir diğer özelliği de döteryum atomlarının yüksek sıcaklıklarda nükleer füzyon işlemine tabi tutulması durumunda büyük miktarlarda enerji açığa çıkabilmesidir. Gezegenimizin nükleer füzyonunu uygulayabilmek için çalıştınız bu göç. Kaynama noktası, buharlaşma ısısı, üçlü nokta ve yoğunluk gibi bazı fiziksel özellikler hidrojenden daha büyük büyüklüklere sahiptir.
Umarım bu bilgilerle döteryum ve özellikleri hakkında daha fazla bilgi edinebilirsiniz.