Сегодня мы поговорим об изотопе, который используется для производства ядерной энергии. Это о дейтерий. Это один из изотопов водорода и обозначается символом D или 2H. Он получил общее название тяжелый водород, потому что масса в два раза больше массы протона. Изотоп - это не что иное, как разновидность одного и того же химического элемента, но имеющая другое массовое число. Дейтерий используется для различных целей.
Поэтому мы собираемся посвятить эту статью, чтобы рассказать вам обо всех характеристиках, структуре, свойствах и использовании дейтерия.
Características principales
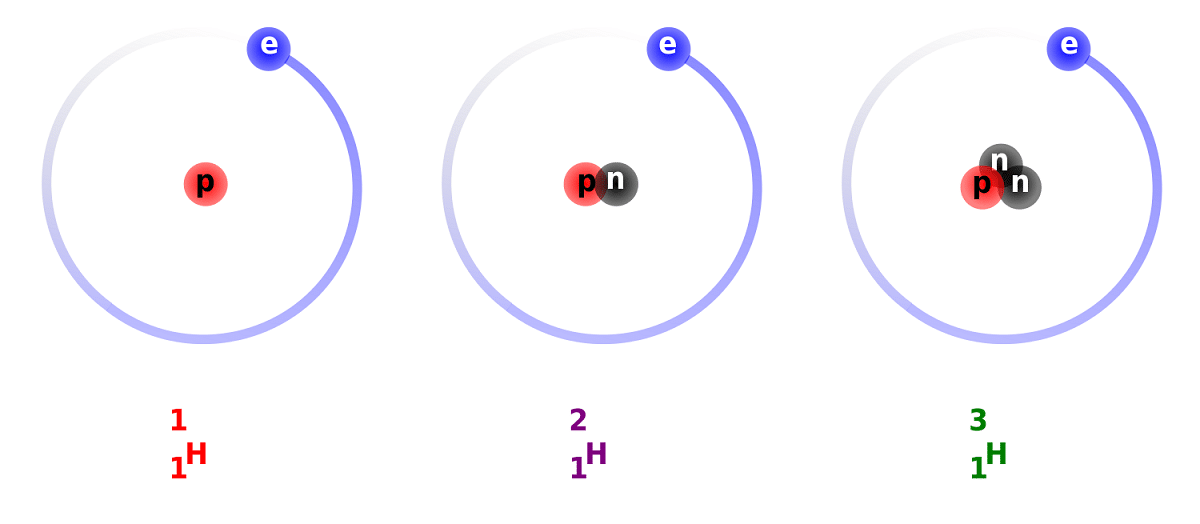
Различие между дейтерием и водородом связано с разницей в количестве нейтронов, которые у него есть. По этой причине дейтерий считается стабильным изотопом и может быть найден в соединениях, образованных водородом полностью природного происхождения. Необходимо учитывать, что хотя они и естественного происхождения, но встречаются в небольшой пропорции. Учитывая свойства, которые он так похож на обычный водород, может полностью заменить его в реакциях, в которых он участвует. Таким образом, его можно превратить в эквивалентные вещества.
По этой и другим причинам дейтерий имеет большое количество применений в различных областях науки. С годами он стал одним из важнейших элементов исследований и достижений в области технологий и информации.
Основная структура этого изотопа состоит из ядра, в котором есть протон и нейтрон. Его атомный вес составляет около 2,014 граммов. Этот изотоп был открыт в 1931 году благодаря Гарольду К. Юри, химику из Соединенных Штатов, и его сотрудникам Фердинанду Брикведде и Джорджу Мерфи. Подготовка к встрече с дейтерием в чистом виде была впервые успешно проведена в 1933 году. Уже в 50-х годах начали использовать твердую фазу, которая продемонстрировала высокую стабильность, известную как дейтерид лития. Это вещество могло заменить дейтерий и тритий в большом количестве химических реакций.
Успехи в науке достигаются, когда обнаруживается вещество, которое может способствовать химическим реакциям с образованием продуктов. В этом смысле, если вы изучите распространенность этого изотопа, вы сможете наблюдать определенные вещи. Известно, что доля дейтерия в воде незначительно меняется в зависимости от области, где отбирается проба. Есть некоторые спектроскопические исследования, которые определили существование этого изотопа на других планетах нашей галактики. Это может иметь большое значение для изучения состава других небесных тел.
Структура и происхождение дейтерия

Мы собираемся узнать некоторые факты о дейтерии. Как мы уже упоминали ранее, основное различие между изотопами водорода заключается в их структуре. И в том, что водород, дейтерий и тритий имеют разное количество протонов и нейтронов, поэтому они имеют разные химические свойства. Я также должен принять во внимание, что дейтерий, который существует внутри других звездных тел, удаляется с большей скоростью, чем он возникает. Это одна из причин, почему так сложно изучить присутствие дейтерия в звездных телах.
Считается, что другие явления природы образуют небольшое количество дейтерия, поэтому его производство по-прежнему вызывает значительный интерес. Исходя из упомянутого ранее процента присутствия дейтерия в природе, он не составляет 0.02%. Серия научных исследований показала, что подавляющее большинство атомов, образованных из дейтерия, естественным образом возникло в результате взрыва, который дал начало Вселенной, известной как Большой взрыв. Это одна из основных причин, почему считается, что дейтерий присутствует на больших планетах, таких как Юпитер.
Самый распространенный способ получить этот изотоп естественным путем - соединить его с водородом. Когда это произойдет, он будет объединен в виде протия. Ученым интересно знать взаимосвязь, установленную между долей дейтерий и водород в разных областях науки. Он широко изучается в таких областях науки, как астрономия или климатология. В этих отраслях у него есть некоторые практические полезности, чтобы знать и понимать Вселенную и нашу атмосферу.
Свойства дейтерия

Мы узнаем, каковы основные свойства этого изотопа, принадлежащего водороду. Первое, что нужно сделать, - это узнать, что такое изотоп, лишенный радиоактивных свойств. Это означает, что он довольно устойчив по своей природе. Его можно использовать для замены водорода в различных химических реакциях. Естественно, имея большую стабильность, показывает другое поведение по сравнению с обычным водородом. Это происходит во всех реакциях, имеющих биохимическую природу. Перед заменой необходимо знать, что, хотя этого можно достичь путем обмена водорода на дейтерий в химических реакциях, необходимо знать, что они будут вести себя иначе.
Когда вы заменяете два атома водорода в воде, вы можете получить соединение, известное как тяжелая вода. Водород, который присутствует в океане и находится в форме дейтерия. он составляет всего 0,016% по отношению к протию. Во Вселенной этот изотоп имеет тенденцию быстрее плавиться с образованием гелия. Если мы объединим дейтерий с атомарным кислородом, мы увидим, что он становится токсичным. Несмотря на это, и по химическим свойствам он очень похож на водород.
Еще одно свойство этого изотопа состоит в том, что когда атомы дейтерия подвергаются процессу ядерного синтеза при высоких температурах, может выделяться большое количество энергии. Это исход, который вы изучали, чтобы реализовать ядерный синтез на нашей планете. Некоторые физические свойства, такие как точка кипения, теплота испарения, тройная точка и плотность. обладают большими величинами, чем водород.
Я надеюсь, что с помощью этой информации вы сможете больше узнать о дейтерии и его характеристиках.