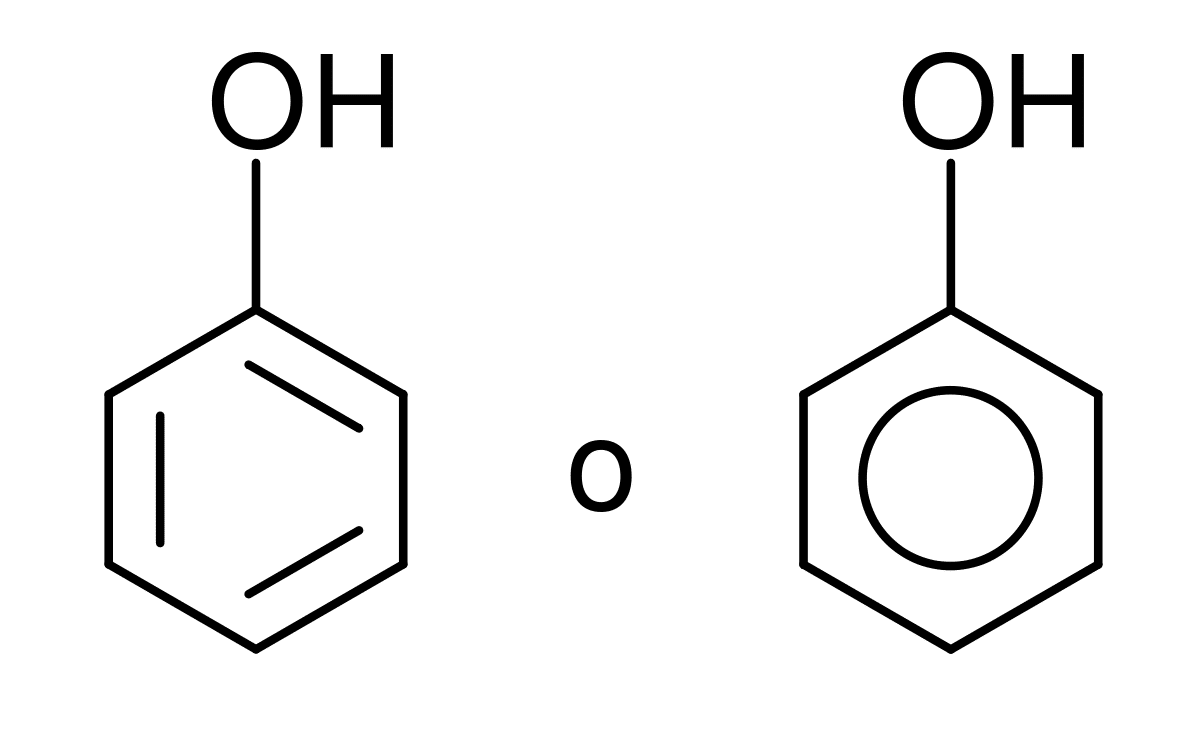
Группа гидроксил Он состоит из атома кислорода и атома водорода и напоминает молекулу воды. Его можно найти в различных химических формах, таких как группа, ион или радикал. Для всех тех, кто изучает органическую химию, знание реакций и важности этой группы атомов является фундаментальным. И он способен образовывать существенные связи с атомом углерода, хотя он также может образовывать связи с серой и фосфором.
В этой статье мы расскажем вам о характеристиках гидроксильной группы и ее важности в органической химии.
Características principales
Когда мы анализируем гидроксильную группу с точки зрения неорганической химии, мы видим, что она больше участвует в качестве иона. Другими словами, тип шнурка, который существует между ним и металлами, не ковалентный, а ионный. Из-за этого гидроксильная группа стала важным элементом, который помогает определять свойства и превращения многих соединений.
Гидроксильная группа присоединена к радикалу, который определяется cбуквой R, если он алкил, или буквой Ar, если он ароматический. Больше всего я знаю в науке то, что вносит гидроксильную группу в молекулу, в которой она связывается. Лучший ответ можно найти при изучении его протонов. И в том, что протоны могут захватываться сильными основаниями с образованием солей. Это также может взаимодействовать с другими окружающими группами, которые связаны друг с другом водородными связями. Кроме того, наиболее важным аспектом гидроксильной группы является то, что где бы она ни находилась, она может представлять потенциальную область для образования воды.
Строение гидроксильной группы

Гидроксильная группа стала довольно интересной молекулой с точки зрения органической химии. Молекула воды имеет угловатую форму и похожа на бумеранг. Если мы отрежем один из его концов, что означает то же самое, что и удаление протона, могут возникнуть различные ситуации. Молекула воды превращается в гидроксильный радикал или гидроксильный ион. Однако оба имеют линейную молекулярную геометрию и не являются электронными.
Все эти связи связаны с тем, что они ориентированы на два атома, чтобы всегда оставаться выровненными. То же самое с гибридными орбиталями. Ключ для гидроксильной группы, позволяющий различным молекулам смешиваться друг с другом, требует водородных связей. Эти водородные связи не являются прочными сами по себе, но по мере увеличения количества источников и количества гидроксильных групп в структуре эффекты множатся. Это увеличение количества водородных связей также отражается на физических свойствах соединения.
Водородные связи требуют, чтобы атомы располагались друг напротив друга. Некоторые атомы кислорода одной гидроксильной группы должны быть расположены так, чтобы образовалась прямая линия с водородом второй группы. Это несколько сложнее, но случается часто. Таким образом, возникают довольно специфические пространственные устройства, такие как что происходит в структуре молекулы ДНК. Это происходит между азотистыми основаниями, составляющими ДНК.
Мы можем назвать количество гидроксильных групп структурой, прямо пропорциональной сродству воды к молекуле. Мы собираемся привести пример, чтобы лучше понять это. Сахар, хотя и имеет гидрофобную углеродную структуру, так как имеет большое количество гидроксильных групп, делает его очень растворимым в воде.
Ионы и их функции
Гидроксильная группа и ион очень похожи, но имеют разные химические свойства. Ион гидроксила является чрезвычайно сильным основанием и работает, улавливая протоны. Если мы его заставим, он превратится в воду. А это неполная молекула воды, которая заряжена отрицательно и для завершения ей нужен протон. С другой стороны, поскольку гидроксильная группа ему не нужно захватывать протоны, чтобы завершить его работу как чрезвычайно слабое основание. Он способен отдавать протоны, хотя делает это только против очень сильных оснований.
Положительные ядра - это атомы в молекуле, которые страдают от недостатка электроники из-за их электроотрицательного окружения.
Гидроксильная группа и метеорология

Мы знаем, что в воздухе он действует как моющее средство, которое расщепляет другие газы. Мы знаем, что гидроксильная группа является основным регулятором концентрации метана. Метан - это парниковый газ, концентрация которого превосходит диоксид углерода в его вкладе в глобальное потепление. Хотя метан в меньшей степени содержится в атмосфере, он способен удерживать большее количество тепла, чем диоксид углерода.
Есть новое исследование, проведенное научным сотрудником НАСА, которое показало, что гидроксильные радикалы перерабатывают сами себя и способны поддерживать постоянную атмосферную концентрацию. Эта концентрация сохраняется с течением времени, даже если выбросы метана увеличиваются. Следовательно, понимание роли гидроксила необходимо для понимания срока службы метана и атмосферы.
Ученые указали, что увеличение концентрации и выбросов метана может привести к истощению количества гидроксильных радикалов в глобальном масштабе. Таким образом, полезный срок службы метана будет продлен, а это усугубит глобальное потепление. Увеличив продолжительность жизни метана, нам нечем было бы очищать атмосферу. Были изучены основные источники гидроксила и метана и то, как они реагируют. Рециркуляция этой группы происходит после разложения метана, а затем его преобразования в присутствии других газов.. Концентрации гидроксила со временем довольно стабильны. Они не обязательно должны исчезать при реакции с метаном.
Я надеюсь, что с этой информацией вы сможете узнать больше о гидроксильной группе и всей ее важности.