
O átomo é a unidade básica da matéria e é a menor fração que pode identificar um elemento químico. Consiste em um núcleo atômico que contém nêutrons e prótons, e elétrons ao redor do núcleo. O termo átomo é derivado do grego e significa indivisível. No entanto, muitas pessoas não sabem bem o que é um átomo nem quais são suas características.
Por isso, vamos dedicar este artigo para contar o que é um átomo, suas características e importância.
o que é um átomo

Os átomos consistem em uma parte central chamada núcleo, na qual residem os prótons (partículas carregadas positivamente) e os nêutrons (partículas eletricamente neutras). A região ao redor do núcleo é ocupada por elétrons (partículas com carga negativa); esta região é chamada de camada elétrica. A casca elétrica (carregada negativamente) e o núcleo (carregado positivamente) são mantidos juntos por atração elétrica.
O diâmetro médio de um átomo é de cerca de 10 a 10 metros, e o diâmetro médio de um núcleo é de cerca de 10 a 15 metros; por tanto, um átomo tem um diâmetro de 10.000 a 100.000 vezes maior que seu núcleo. Por exemplo, se um átomo tiver o tamanho de um campo de futebol, o núcleo terá o mesmo tamanho da bola no centro do campo. Se um átomo tem 100 metros de diâmetro, seu núcleo tem 1 centímetro de diâmetro.
Um pouco de história

O filósofo grego Aristóteles (384 aC – 322 aC) tentou explicar a composição de toda a matéria a partir dos elementos: terra, ar, fogo e água. Demócrito (546 aC – 460 aC) foi um cientista e matemático grego que propôs a ideia de que havia um limite para o tamanho das partículas. Essas partículas se tornam tão pequenas que não podem mais ser divididas, disse ele. Ele chamou essas partículas de "átomos".
Durante a maior parte do século XIX, foi o modelo atômico do cientista britânico Dalton quem propôs a teoria atômica, que estava muito além do pensamento dos antigos da época.
Esta teoria diz que Toda a matéria é composta de minúsculas partículas indivisíveis chamadas átomos. Pesquisas recentes descobriram que os átomos são compostos de outras pequenas partículas chamadas partículas subatômicas.
Historicamente, diferentes teorias atômicas sobre a composição da matéria foram desenvolvidas antes que o conhecimento atual sobre a estrutura atômica fosse obtido. Com base na teoria atômica, Os cientistas têm demonstrado modelos de átomos que evoluem gradualmente.
O primeiro modelo proposto por John Dalton desenvolveu-se no modelo do átomo de Niels Bohr. Bohr propôs um modelo muito semelhante ao modelo atual de elétrons orbitando o núcleo.
estrutura de um átomo
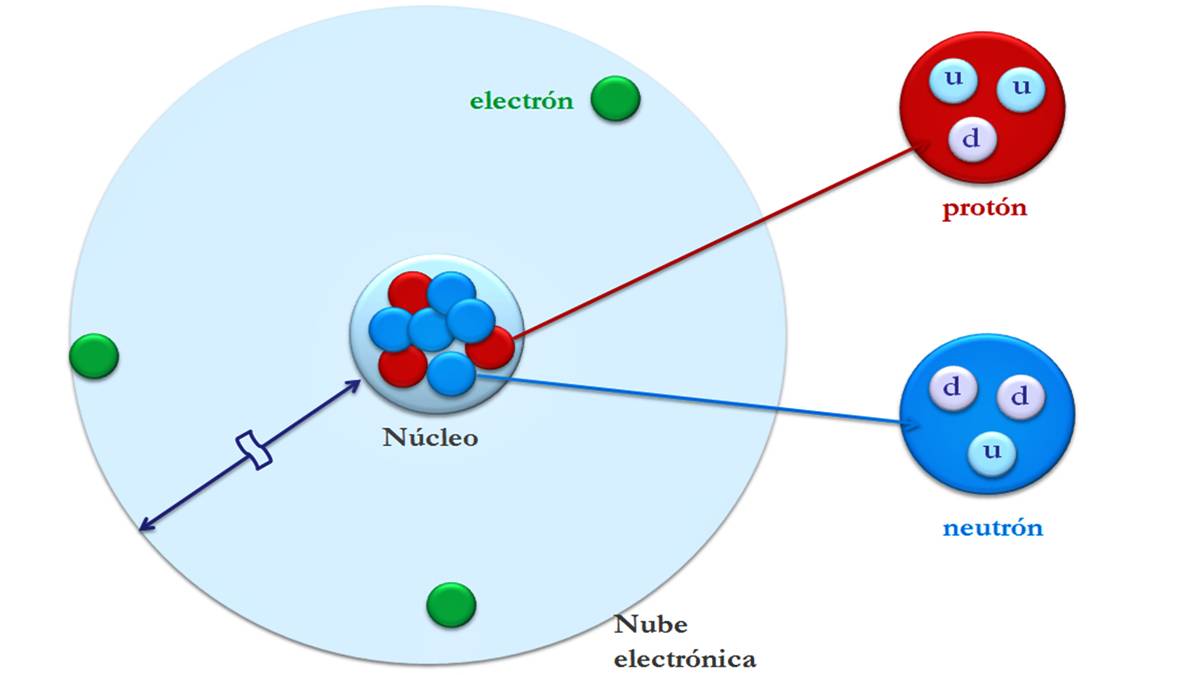
Os átomos são compostos de pequenas partículas chamadas partículas subatômicas: elétrons, prótons e nêutrons. A maior parte da massa de um átomo está concentrada no núcleo. E seu maior volume está no invólucro elétrico onde se encontram os elétrons.
Elétrons, prótons e nêutrons
Os elétrons são carregados negativamente e quase não têm massa. Sua massa é cerca de 1840 vezes a do núcleo atômico.. São partículas minúsculas que giram em torno do núcleo central de um átomo. Além disso, eles se movem rapidamente ao redor do núcleo gerando um campo eletromagnético.
Um próton tem a mesma carga positiva que a carga de um elétron em valor absoluto, então prótons e elétrons tendem a se atrair. Estes constituem a unidade de massa e junto com os nêutrons formam o núcleo do átomo.
Os nêutrons não têm carga, ou seja, têm carga neutra. Junto com os prótons, forma o núcleo e representa quase toda a massa (99,9%) do átomo. Os nêutrons fornecem estabilidade ao núcleo.
Os átomos têm níveis de energia, sete camadas ao redor do núcleo nas quais existem elétrons orbitando o núcleo. As camadas são denominadas K, L, M, N, O, P e Q. Cada camada pode conter um número finito de elétrons: oito elétrons por camada. A camada mais externa é sempre a mais dinâmica. Apenas o átomo de hidrogênio não possui nêutrons e apenas um elétron orbita ao redor do próton.
características químicas
Na química, os átomos são as unidades fundamentais que geralmente mantêm suas propriedades originais em todas as reações. Eles não são destruídos ou criados, eles são simplesmente organizados de maneiras diferentes com diferentes conexões entre eles.
Os átomos se agrupam para criar moléculas e outros tipos de materiais. As ligações criadas nas reações químicas têm uma certa composição que distingue os diferentes elementos químicos. Esses elementos são aqueles que aparecem na tabela periódica dos elementos.
Cada um desses elementos tem muitos prótons no núcleo. Esse número é chamado de número atômico e é indicado pela letra Z. Todos os átomos com o mesmo número de prótons pertencem ao mesmo elemento e têm as mesmas propriedades químicas, embora sejam elementos químicos diferentes.
Além disso, encontramos o número de massa, denotado pela letra A. Este número refere-se ao número de nucleons presentes no átomo. Outro tipo de átomo que podemos encontrar, e sobre o qual sabemos melhor, é um isótopo. Esses átomos têm o mesmo número de prótons, mas diferentes números de nêutrons. Eles têm as mesmas propriedades químicas, embora suas propriedades físicas sejam diferentes umas das outras.
Como observamos anteriormente, os isótopos são muito importantes. E são vitais para a energia nuclear porque o enriquecimento de urânio envolve a conversão de um isótopo de urânio em outro com uma estrutura química mais instável, permitindo uma reação em cadeia.
Propriedades
As propriedades que definem um átomo são:
- Número atômico (Z) indicando o número de prótons no núcleo. Todos os átomos com o mesmo número de prótons pertencem ao mesmo elemento. Por exemplo, um átomo de hidrogênio com apenas um próton.
- O número de massa refere-se à soma de prótons e nêutrons.. Elementos com diferentes números de nêutrons são diferentes isótopos do mesmo elemento.
- eletro-negatividade É a tendência dos átomos de atrair elétrons quando formam ligações químicas.
- raio atômico Corresponde à metade da distância entre dois núcleos unidos do mesmo elemento.
- potencial de ionização É a energia necessária para remover um elétron de um elemento.
Espero que com essas informações você possa aprender mais sobre o que é um átomo e suas características.
MUITO BOM
RICARDO