
En kjemisk endring er en endring av materie som endrer dens kjemiske struktur, det vil si at den endrer egenskapene, ikke bare formen. Dette betyr at en kjemisk endring, også kjent som en kjemisk reaksjon eller kjemisk fenomen, innebærer å bryte og danne kjemiske bindinger i ett stoff eller en forbindelse for å danne en ny substans eller forbindelse. Det er mange kjemiske endringer i verden.
Av denne grunn skal vi dedikere denne artikkelen til å fortelle deg hva som er de viktigste kjemiske endringene som eksisterer og et eksempel på dem.
Hva er kjemiske endringer?

Når to eller flere stoffer (kalt reaktanter eller reaktanter) gjennomgå en kjemisk reaksjon, endre deres kjemiske struktur i prosessen og være i stand til å konsumere (endoterme reaksjoner) eller frigjør (eksoterme reaksjoner) energi, og produserer to eller flere stoffer (kalt et produkt). Noen kjemiske reaksjoner er farlige for mennesker fordi de kan involvere eller produsere giftige eller etsende forbindelser. Andre reaksjoner, for eksempel visse eksoterme reaksjoner, kan forårsake eksplosjoner.
I den kjemiske industrien produseres mange materialer som vi bruker i vårt daglige liv gjennom kontrollerte kjemiske reaksjoner. Noen reaksjoner oppstår spontant, andre må produseres av mennesker i fabrikker eller kjemiske laboratorier. En kjemisk reaksjon tar en bestemt mengde tid å finne sted. avhengig av arten av reaktantene og betingelsene som reaksjonen skjer under.
Derfor inkluderer faktorer som påvirker hastigheten på kjemiske reaksjoner generelt:
- Temperaturen stiger. En økning i temperatur har en tendens til å øke hastigheten på en kjemisk reaksjon.
- økt trykk. Å øke trykket øker generelt hastigheten på en kjemisk reaksjon. Dette skjer vanligvis når stoffer som er følsomme for trykkendringer, som gasser, reagerer. Når det gjelder væsker og faste stoffer, forårsaker ikke trykkendringer signifikante endringer i reaksjonshastighetene.
- Reagens aggregeringstilstand. Faste stoffer reagerer generelt saktere enn væsker eller gasser, selv om hastigheten også avhenger av reaktiviteten til hvert stoff.
- Bruk av katalysator. De er stoffer som brukes til å øke hastigheten på kjemiske reaksjoner. Disse stoffene forstyrrer ikke reaksjonen, de kontrollerer bare hastigheten reaksjonen skjer med. Det finnes også stoffer som kalles inhibitorer, som brukes på samme måte, men som har motsatt effekt, og bremser reaksjonen.
- lysenergi. Noen kjemiske reaksjoner går raskere når lys faller på dem.
- Reagenskonsentrasjon. De fleste kjemiske reaksjoner skjer raskere hvis konsentrasjonene av reaktantene er høye.
Eksempler på kjemiske endringer
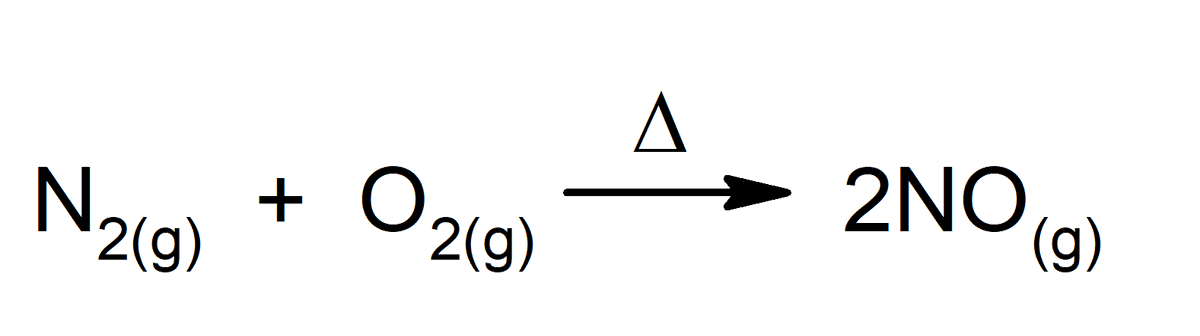
Enhver kjemisk reaksjon er et perfekt eksempel på en kjemisk endring, selv de som finner sted inne i kroppen vår. Noen eksempler er:
- Puster. Dette er en kjemisk endret biologisk prosess der oksygen tas fra luften og brukes til å reagere med glukosen vi får fra maten, og produserer høye nivåer av kjemisk energi (ATP) og store mengder avfall karbondioksid (CO2). utskilles.
- Sur nedbør. Det forekommer i miljøer med alvorlig luftforurensning. Det er vanligvis et resultat av en kjemisk endring mellom vann lagret i skyer og andre gasser spredt i luften, hvis svoveloksid- eller nitrogenoksidinnhold skaper svovelsyre eller salpetersyre som faller sammen med regnvann og danner salt. Reaksjonen som finner sted inne i batteriet er mellom syren og metallet. For eksempel produserer et batteri som bruker bly og svovelsyre bly(II)sulfat, et hvitt salt. Ozonnedbrytning. Ozonmolekyler brytes ned til oksygenmolekyler under påvirkning av en slags lys.
Kjemisk endring og fysisk endring

Fysiske endringer i et stoff endrer ikke dets sammensetning, det vil si at de ikke endrer den kjemiske strukturen til stoffet, så stoffer kan ikke brytes ned eller dannes ved fysiske endringer. Fysisk endring endrer ganske enkelt de fysiske egenskapene til materie, som form, tetthet og aggregeringstilstand (fast stoff, flytende, gass). Fysiske endringer derimot, De er vanligvis reversible fordi de endrer materiens form eller tilstand, men ikke sammensetningen.
For eksempel, når vann koker, kan vi gjøre en væske til en gass, men den resulterende dampen består fortsatt av vannmolekyler. Omvendt, hvis vi fryser vann, blir det fast, men er fortsatt kjemisk det samme stoffet.
Et annet eksempel er den flytende gassen vi bruker i sigarettennerene våre, vanligvis butan (C4H10) eller propan (C3H8) som blir flytende når det påføres høyt trykk, men som ikke endrer dens kjemiske sammensetning.
En kjemisk endring endrer arrangementet og bindingen av atomene i et stoff slik at de kombineres på en annen måte, noe som resulterer i et annet stoff enn det opprinnelige. Når det skjer en kjemisk endring ender du alltid opp med samme mengde stoff som du startet med, selv om det er i et annet forhold, fordi materie ikke kan skapes eller ødelegges, bare transformeres.
Hvis vi for eksempel reagerer vann (H2O) og kalium (K), får vi to nye stoffer: kaliumhydroksid (KOH) og hydrogengass (H2). Dette er en reaksjon som generelt frigjør mye energi og er derfor svært farlig.
Eksempler på kjemiske endringer i materie
Baking av småkaker eller kaker
Vanlige ting som informasjonskapsler, kaker, cupcakes, etc. skjule en kjemisk reaksjon kalt gjæring, der deigen hever på grunn av gassene som produseres av gjæren. Ved brødbaking omdanner gjær stivelse til glukose.
Fordøyelse
Fordøyelsen av mat er et åpenbart eksempel på den kjemiske endringen av materie gjennom hydrolyse (nedbrytning av organisk materiale ved innvirkning av vann). Maten vi spiser i form av frukt, grønnsaker, kjøtt osv. de går gjennom en prosess med å blande med magesaft for bedre å absorbere næringsstoffer og konvertere dem til forskjellige stoffer i henhold til organismens behov.
I samme prosess blir overskuddselementene eller giftstoffene eliminert fra organismen på en annen måte enn den opprinnelige; i form av avføring, urin, svette o.l.
pulque
Fermentering er en katabolsk prosess der glukosemolekyler brytes ned på grunn av mangel på oksygen. Noen av de alkoholholdige drikkene som oppnås gjennom gjæringsprosessen er cider, øl og myk vin, sistnevnte er en av de minst kjente drikkene i verden. Pulque oppnås fra agaveplanten gjennom en håndverksprosessl, der stoffets modning er nøkkelen til å oppnå sluttproduktet, som er hvitt, surt og tyktflytende, med en veldig spesifikk smak som ikke passer til noen smak.
Gjæring skjer også under fremstilling av blant annet brød, yoghurt og ost.
Caramelo
Karamell er et grunnleggende eksempel på en kjemisk endring i substans, da fast hvitt sukker, oppvarmet i noen minutter, blir til en ravfarget goo med en behagelig aroma. Det genereres med andre ord et helt annet produkt enn originalen.
Jeg håper at du med denne informasjonen kan lære mer om kjemiske endringer og deres eksempler.