
Cheminis pokytis – tai materijos pakitimas, pakeičiantis jos cheminę struktūrą, ty keičiasi jos savybės, o ne tik forma. Tai reiškia, kad cheminis pokytis, dar žinomas kaip cheminė reakcija arba cheminis reiškinys, apima cheminių jungčių nutraukimą ir formavimąsi vienoje medžiagoje ar junginyje, kad susidarytų nauja medžiaga ar junginys. Yra daugybė cheminiai pokyčiai pasaulyje.
Dėl šios priežasties šį straipsnį skirsime tam, kad papasakotume, kokie yra pagrindiniai egzistuojantys cheminiai pokyčiai ir koks jų pavyzdys.
Kas yra cheminiai pokyčiai?

Kai dvi ar daugiau medžiagų (vadinamos reagentais arba reagentais) vyksta cheminė reakcija, proceso metu keičiasi jų cheminė struktūra ir gali vartoti (endoterminės reakcijos) arba išskiria (egzoterminės reakcijos) energiją, gamindamos dvi ar daugiau medžiagų (vadinamų produktu). Kai kurios cheminės reakcijos yra pavojingos žmonėms, nes jose gali atsirasti toksiškų ar ėsdinančių junginių arba jų susidarymas. Kitos reakcijos, pvz., tam tikros egzoterminės reakcijos, gali sukelti sprogimus.
Chemijos pramonėje daugelis medžiagų, kurias naudojame kasdieniame gyvenime, gaminamos kontroliuojamų cheminių reakcijų metu. Kai kurios reakcijos vyksta spontaniškai, kitas turi sukelti žmonės gamyklose ar chemijos laboratorijose. Cheminei reakcijai įvykti reikia tam tikro laiko. priklausomai nuo reagentų pobūdžio ir reakcijos vykstančių sąlygų.
Todėl veiksniai, turintys įtakos cheminių reakcijų greičiui, paprastai apima:
- Temperatūra pakyla. Temperatūros padidėjimas linkęs padidinti cheminės reakcijos greitį.
- padidėjęs slėgis. Padidinus slėgį, paprastai padidėja cheminės reakcijos greitis. Dažniausiai tai atsitinka, kai reaguoja slėgio pokyčiams jautrios medžiagos, pavyzdžiui, dujos. Skysčių ir kietųjų medžiagų atveju slėgio pokyčiai nesukelia reikšmingų jų reakcijos greičio pokyčių.
- Reagento agregacijos būsena. Kietosios medžiagos paprastai reaguoja lėčiau nei skysčiai ar dujos, nors greitis taip pat priklauso nuo kiekvienos medžiagos reaktyvumo.
- Katalizatoriaus naudojimas. Tai medžiagos, kurios naudojamos cheminių reakcijų greičiui padidinti. Šios medžiagos netrukdo reakcijai, jos tik kontroliuoja reakcijos greitį. Taip pat yra medžiagų, vadinamų inhibitoriais, kurios naudojamos taip pat, tačiau turi priešingą poveikį – sulėtina reakciją.
- šviesos energija. Kai kurios cheminės reakcijos paspartėja, kai ant jų patenka šviesa.
- Reagento koncentracija. Dauguma cheminių reakcijų vyksta greičiau, jei reaguojančių medžiagų koncentracija yra didelė.
Cheminių pokyčių pavyzdžiai
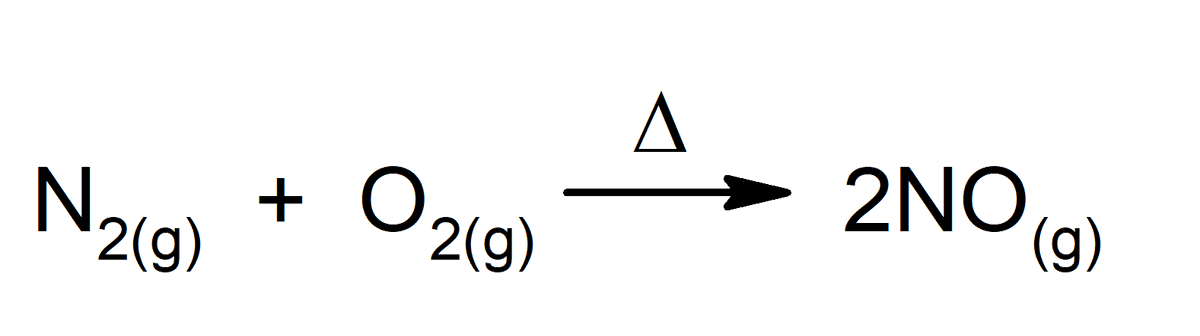
Bet kokia cheminė reakcija yra puikus cheminių pokyčių pavyzdys, net ir tie, kurie vyksta mūsų kūne. Keletas pavyzdžių:
- Kvėpavimas. Tai chemiškai pakeistas biologinis procesas, kurio metu deguonis paimamas iš oro ir naudojamas reaguoti su gliukoze, kurią gauname iš maisto, gaminant daug cheminės energijos (ATP) ir daug išmetamo anglies dioksido (CO2). išsiskiria.
- Rūgštūs lietūs. Tai atsiranda aplinkoje, kurioje yra didelė oro tarša. Paprastai tai yra cheminio pasikeitimo tarp debesyse laikomo vandens ir kitų ore pasklidusių dujų, kurių sieros oksido arba azoto oksido kiekis sukuria sieros arba azoto rūgštį, kuri kartu su lietaus vandeniu nukrenta ir susidaro druska. Reakcija, kuri vyksta akumuliatoriaus viduje, vyksta tarp rūgšties ir metalo. Pavyzdžiui, baterija, kurioje naudojamas švinas ir sieros rūgštis, gamina švino (II) sulfatą, baltą druską. Ozono skilimas. Ozono molekulės, veikiamos tam tikros šviesos, skyla į deguonies molekules.
Cheminiai pokyčiai ir fiziniai pokyčiai

Fizikiniai medžiagos pokyčiai nekeičia jos sudėties, tai yra, nepakeičia cheminės medžiagos struktūros, todėl medžiagos negali suskaidyti ar susidaryti dėl fizinių pokyčių. Fiziniai pokyčiai tiesiog pakeičia fizines medžiagos savybes, tokias kaip forma, tankis ir agregacijos būsena (kieta, skysta, dujinė). Kita vertus, fiziniai pokyčiai Paprastai jie yra grįžtami, nes keičia medžiagos formą ar būseną, bet ne jos sudėtį.
Pavyzdžiui, kai vanduo užverda, skystį galime paversti dujomis, tačiau susidarantys garai vis tiek susideda iš vandens molekulių. Ir atvirkščiai, jei užšaldome vandenį, jis tampa kietas, bet chemiškai vis tiek yra ta pati medžiaga.
Kitas pavyzdys yra suskystintos dujos, kurias naudojame savo cigarečių žiebtuvėliuose, dažniausiai butanas (C4H10) arba propanas (C3H8), kuris veikiant aukštam slėgiui virsta skystu, bet nekeičia savo cheminės sudėties.
Cheminis pokytis pakeičia atomų išsidėstymą ir ryšį medžiagoje taip, kad jie susijungia kitaip, todėl susidaro kitokia medžiaga nei pradinė. Kai įvyksta cheminis pokytis, jūs visada gaunate tą patį medžiagos kiekį, su kuriuo pradėjote, net jei jo santykis yra kitoks, nes materija negali būti sukurta ar sunaikinta, o tik transformuojama.
Pavyzdžiui, jei sureaguosime su vandeniu (H2O) ir kaliu (K), gausime dvi naujas medžiagas: kalio hidroksidą (KOH) ir vandenilio dujas (H2). Tai reakcija, kuri paprastai išskiria daug energijos ir todėl yra labai pavojinga.
Cheminių medžiagų pokyčių pavyzdžiai
Sausainių ar pyragų kepimas
Įprasti dalykai, pvz., sausainiai, pyragaičiai, keksiukai ir kt. paslėpti cheminę reakciją, vadinamą fermentacija, kurios metu tešla pakyla dėl mielių gaminamų dujų. Gaminant duoną mielės paverčia krakmolą gliukoze.
Virškinimas
Maisto virškinimas yra akivaizdus cheminės medžiagos pasikeitimo hidrolizės metu (organinių medžiagų skaidymas veikiant vandeniui) pavyzdys. Maistas, kurį valgome vaisių, daržovių, mėsos ir kt., jie pereina maišymosi su skrandžio sultimis procesą, kad geriau įsisavintų maistines medžiagas ir paverčia jas įvairiomis medžiagomis pagal organizmo poreikius.
Tuo pačiu metu elementų ar toksinų perteklius iš organizmo pašalinamas kitaip nei pirminis; išmatų, šlapimo, prakaito ir kt.
pulque
Fermentacija yra katabolinis procesas, kurio metu gliukozės molekulės suyra dėl deguonies trūkumo. Kai kurie alkoholiniai gėrimai, gaunami fermentacijos proceso metu, yra sidras, alus ir minkštasis vynas, pastarasis yra vienas mažiausiai žinomų gėrimų pasaulyje. Pulque gaunamas iš agavos augalo amatininkų būdul, kuriame medžiagos brandinimas yra labai svarbus norint gauti galutinį produktą, kuris yra baltas, rūgštus ir klampus, turintis labai specifinį skonį, kuris netinka jokiam gomuriui.
Fermentacija taip pat vyksta gaminant duoną, jogurtą ir sūrį, be kita ko.
caramelo
Karamelė yra pagrindinis cheminės medžiagos pasikeitimo pavyzdys, nes kietas baltas cukrus, pakaitintas kelias minutes, virsta gintaro spalvos gintaru, turinčiu malonų aromatą. Kitaip tariant, sukuriamas produktas, visiškai kitoks nei originalas.
Tikiuosi, kad turėdami šią informaciją galėsite daugiau sužinoti apie cheminius pokyčius ir jų pavyzdžius.