
原子は物質の基本単位であり、化学元素を識別することができる最小の部分です。 それは、中性子と陽子を含む原子核と、原子核を取り囲む電子で構成されています。 アトムという用語はギリシャ語に由来し、分割できないことを意味します。 しかし、よく知らない人も多い 原子とは また、その特徴は何ですか。
したがって、この記事を捧げて、原子とは何か、その特徴と重要性を説明します.
原子とは

原子は核と呼ばれる中心部分で構成されており、その中には陽子 (正に帯電した粒子) と中性子 (電気的に中性の粒子) が存在します。 核の周りの領域は電子 (負に帯電した粒子) で占められています。 この領域は電気層と呼ばれます。 電気シェル (負に帯電) とコア (正に帯電) は、電気的引力によって一緒に保持されます。
原子の平均直径は約 10 ~ 10 メートルで、原子核の平均直径は約 10 ~ 15 メートルです。 それで、 原子の直径は、原子核の 10.000 ~ 100.000 倍です。 たとえば、原子がサッカー場のサイズである場合、原子核はフィールドの中心にあるボールと同じサイズになります。 原子の直径が 100 メートルの場合、原子核の直径は 1 センチメートルです。
いくつかの歴史

ギリシャの哲学者アリストテレス (紀元前 384 年 - 紀元前 322 年) は、すべての物質の組成を、土、空気、火、水の要素から説明しようとしました。 デモクリトス (紀元前 546 年 - 紀元前 460 年) は、粒子のサイズに制限があるという考えを提案したギリシャの科学者および数学者でした。 これらの粒子は非常に小さくなり、分割できなくなると彼は言いました。 彼はそのような粒子を「原子」と呼んだ。
XNUMX 世紀のほとんどの期間、当時の古代人の考えをはるかに超えた原子理論を提案したのは、英国の科学者ダルトンの原子モデルでした。
この理論はそれを言います すべての物質は、原子と呼ばれる分割できない小さな粒子で構成されています。 最近の研究により、原子は亜原子粒子と呼ばれる他の小さな粒子で構成されていることがわかりました。
歴史的に、原子構造に関する現在の知識が得られる前に、物質の組成に関するさまざまな原子理論が開発されてきました。 原子論に基づいて、 科学者たちは、徐々に進化する原子のモデルを実証してきました。
ジョン・ダルトンによって提案された最初のモデルは、ニールス・ボーアの原子モデルに発展しました。 ボーアは、原子核を周回する電子の現在のモデルに非常によく似たモデルを提案しました。
原子の構造
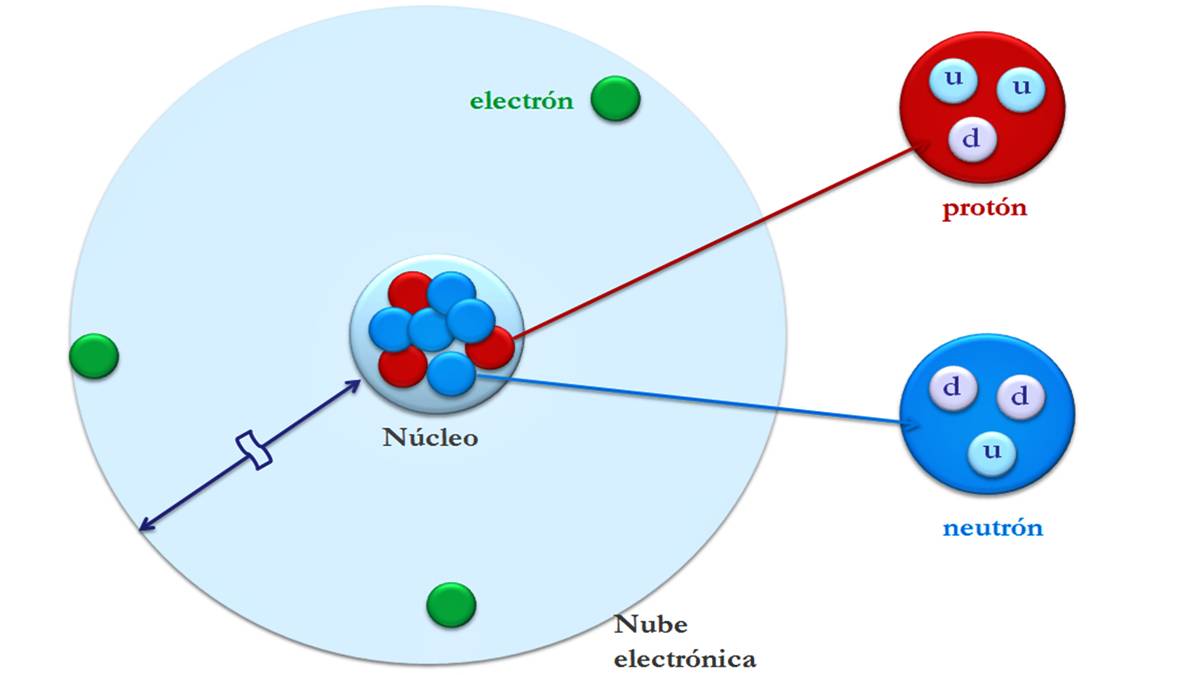
原子は、素粒子と呼ばれる小さな粒子 (電子、陽子、中性子) で構成されています。 原子の質量のほとんどは原子核に集中しています。 そして、その最大の体積は、電子が存在する電気シェルにあります。
電子、陽子、中性子
電子は負に帯電しており、質量はほとんどありません。 その質量は原子核の約 1840 倍です。. それらは、原子の中心核の周りを回転する小さな粒子です。 さらに、それらは電磁場を生成する原子核の周りを急速に移動します。
陽子は絶対値で電子の電荷と同じ正電荷を持っているため、陽子と電子は互いに引き合う傾向があります。 これらは質量の単位を構成し、中性子とともに原子核を形成します。
中性子には電荷がありません。つまり、中性の電荷を持っています。 陽子とともに、 それは核を形成し、原子のほぼすべての質量 (99,9%) を表します。 中性子は原子核を安定させます。
原子にはエネルギー準位があり、原子核の周りには XNUMX つの殻があり、その中で電子が原子核の周りを回っています。 シェルには、K、L、M、N、O、P、および Q という名前が付けられています。各シェルは有限数の電子を保持できます。つまり、シェルごとに XNUMX つの電子です。 最外層は常に最も動的です。 水素原子だけが中性子を持たず、陽子の周りを XNUMX つの電子だけが回っています。
化学的特徴
化学では、原子は通常、すべての反応で元の特性を保持する基本単位です。 それらは破壊されたり作成されたりするのではなく、それらの間のさまざまな接続でさまざまな方法で配置されているだけです。
原子が集まって分子やその他の種類の物質を作ります。 化学反応で生成される結合には、さまざまな化学元素を区別する特定の組成があります。 これらの要素は、要素の周期表に表示されるものです。
これらの各元素は、核内に多くの陽子を持っています。 この番号は原子番号と呼ばれ、文字 Z で表されます。陽子の数が同じ原子はすべて同じ元素に属し、異なる化学元素であっても同じ化学的性質を持ちます。
さらに、 文字Aで表される質量数を見つけます。 この数は、原子に存在する核子の数を指します。 私たちが見つけることができ、私たちが最もよく知っている別のタイプの原子は、同位体です。 これらの原子は陽子の数は同じですが、中性子の数が異なります。 物理的性質は異なりますが、化学的性質は同じです。
前述したように、同位体は非常に重要です。 ウラン濃縮では、あるウラン同位体をより不安定な化学構造を持つ別のウラン同位体に変換する必要があり、連鎖反応を起こすことができるため、それらは原子力にとって不可欠です。
プロパティ
アトムを定義するプロパティは次のとおりです。
- 核内の陽子の数を示す原子番号 (Z)。 陽子の数が同じ原子はすべて同じ元素に属します。 たとえば、水素原子には陽子が XNUMX つしかありません。
- 質量数は、陽子と中性子の合計を指します。. 中性子の数が異なる元素は、同じ元素の異なる同位体です。
- 電気陰性度 これは、原子が化学結合を形成するときに電子を引き寄せる傾向です。
- 原子半径 これは、同じ元素の結合した XNUMX つの原子核間の距離の半分に相当します。
- イオン化ポテンシャル 元素から電子を取り出すのに必要なエネルギーです。
この情報で、原子とは何か、その特徴について理解を深めていただければ幸いです。
とても良い
RICARDO