U svijetu fizike postoji grana koja je odgovorna za proučavanje transformacija koje nastaju toplinom i radom u sustavu. Riječ je o termodinamika. To je grana fizike koja je zadužena za proučavanje svih transformacija koje su samo rezultat procesa koji uključuju promjene u varijablama stanja i temperature i energije na makroskopskoj razini.
U ovom ćemo vam članku reći sve što trebate znati o termodinamici i načelima termodinamike.
Glavne osobine
Ako napravimo analizu klasične termodinamike, vidimo da se ona temelji na konceptu makroskopskog sustava. Ovaj sustav nije ništa drugo nego dio fizičke ili konceptualne mase koji je odvojen od vanjskog okruženja. Kako bi se bolje proučavali termodinamički sustavi, uvijek se pretpostavlja da se radi o fizičkoj masi koju ne narušava razmjena energije s vanjskim ekosustavom.
Stanje makroskopskog sustava što je u ravnotežnim uvjetima određuje se veličinama koje se nazivaju termodinamičkim varijablama. Znamo sve ove varijable, a to su temperatura, tlak, volumen i kemijski sastav. Sve su te varijable ono što definira sustave i njihovu ravnotežu. Glavni zapisi kemijske termodinamike uspostavljeni su zahvaljujući primijenjenoj međunarodnoj uniji. Pomoću ovih jedinica zakon termodinamike može se bolje razraditi i objasniti.
Međutim, postoji grana termodinamike koja ne proučava ravnotežu, ali je odgovorna za analizu termodinamičkih procesa koje uglavnom karakteriziraju nemajući sposobnost postizanja uvjeta ravnoteže na stabilan način.
zakoni
Načela su se prokazala tijekom XNUMX. stoljeća Isaa koji su Oni su zaduženi za regulaciju svih transformacija i njihov napredak. Oni također analiziraju koje su stvarne granice kako bi se postiglo istinsko poimanje. Oni su aksiomi koji se ne mogu dokazati, ali su nedokazivi na temelju iskustva. Svaka se teorija termodinamike temelji na tim principima. Možemo razlikovati 3 osnovna principa plus načelo, ali to je ono koje definira temperaturu i što je implicitno u ostala 3 principa.
Nulti zakon
Opisat ćemo što je taj nulti zakon, koji je prvi koji opisuje temperaturu koja je implicitna u ostatku principa. Kada dva sustava međusobno komuniciraju i budu u toplinskoj ravnoteži, dijele neka svojstva. Ova svojstva koja međusobno dijele mogu se izmjeriti i dobiti numeričku vrijednost. Kao rezultat toga, ako su dva sustava u ravnoteži s trećim, oni će biti u ravnoteži jedni s drugima, a zajedničko svojstvo je temperatura.
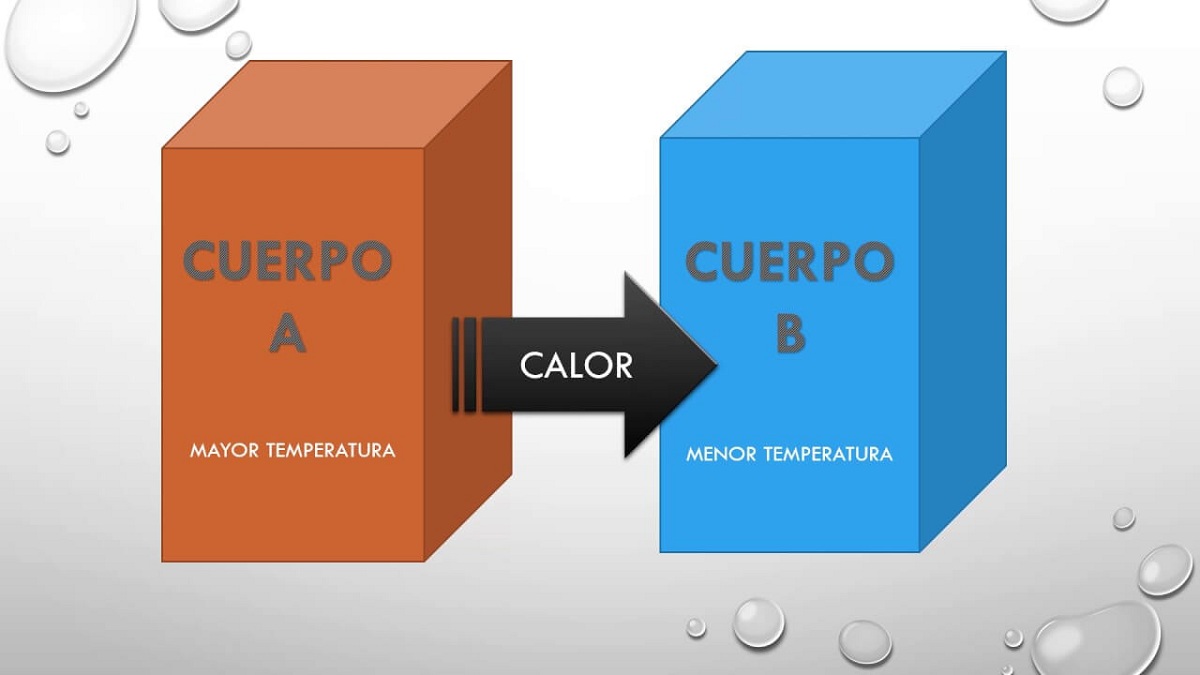
Stoga ovo načelo, ali jednostavno kaže da ako tijelo A bilo je u ravnoteži s tijelom B i ovo tijelo B bit će u toplinskoj ravnoteži s tijelom C, tada će tijela A i C također biti u ravnoteži toplinska. Ovaj princip objašnjava činjenicu da dva tijela na različitim temperaturama mogu međusobno izmjenjivati toplinu. Prije ili kasnije oba tijela postignu istu temperaturu, pa su u totalnoj ravnoteži.
Prvi zakon termodinamike
Kada se tijelo stavi u kontakt s hladnijim tijelom, dolazi do transformacije koja dovodi do stanja ravnoteže. Ovo se stanje ravnoteže temelji na činjenici da su temperature dvaju tijela jednake jer je pojačan prijenos energije između vrućeg tijela za hladno tijelo. Kako bi objasnili ovaj fenomen, znanstvenici su pretpostavili da je vruća tvar koja je prisutna u većim količinama prošla hladnije tijelo. Mislilo se na tekućinu koja se može kretati kroz masu kako bi mogla izmjenjivati toplinu.
Ovo je načelo odgovorno za prepoznavanje topline kao oblika energije. To nije materijalna tvar. Na taj bi se način moglo pokazati da su toplina koja se mjeri kalorijama i rad koji se mjeri u džulima jednaki. Stoga to danas znamo 1 kalorija je otprilike 4,186 džula.
Može se reći da je prvo načelo termodinamike načelo očuvanja energije. Količina energije u toplinskom stroju pretvara se u rad i može ga vidjeti bilo koji stroj koji može proizvesti takav rad bez trošenja energije. Ovaj prvi princip možemo uspostaviti kao: varijacija unutarnje energije zatvorenog termodinamičkog sustava jednaka je razlici koja postoji između topline dovedene u sustav i rada kojeg taj sustav obavlja u okolišu.
Drugi zakon termodinamike
Ovo na početku govori da je nemoguće napraviti ciklički stroj koji samo rezultira prijenosom topline iz hladnog tijela u toplo tijelo. Možemo reći da je nemoguće izvršiti transformaciju čiji će rezultat biti samo onaj pretvaranja topline koju smo izvukli iz jednog izvora u mehanički rad.
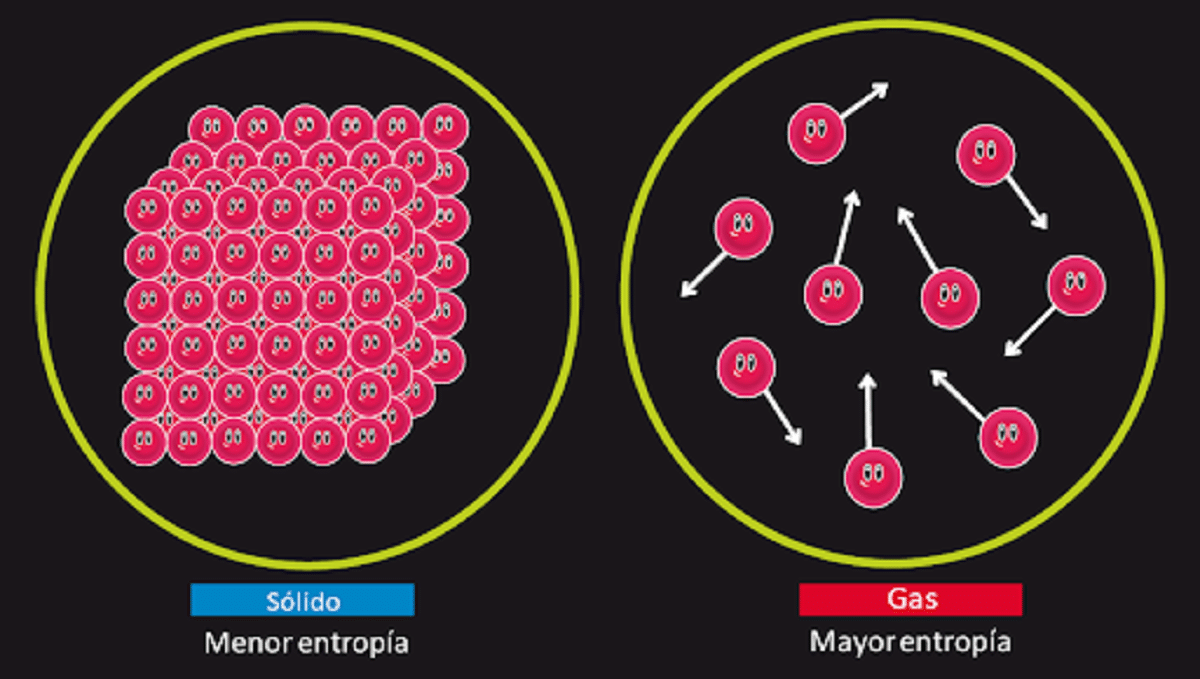
Ovo je načelo zaduženo za poricanje mogućnosti postojanja poznatog vječnog kretanja druge vrste. Znamo da entropija sustava ostaje izoliran nepromijenjen kada se dogodi reverzibilna transformacija. Također znamo da se povećava kad se dogodi nepovratna transformacija.
Treći zakon termodinamike
Ovo posljednje načelo usko je povezano s drugim i smatra se njegovom posljedicom. Ovaj princip potvrđuje da se apsolutno biće ne može postići u boji konačnim brojem transformacija. Znamo da apsolutna nula nije veća od minimalne temperature koja se može postići. U jedinicama Kelvina znamo da je 0, ali u Celzijevim stupnjevima ima vrijednost -273.15 stupnjeva.
Također se navodi da je entropija za krutinu koja je savršeno kristalna s temperaturom od 0 kelvina jednaka 0. To znači da ne bi bilo entropije, pa bi sustav bio potpuno stabilan. Energija oslobađanja, translacije i rotacije čestica koje ga čine ne bi bila ništa na temperaturi od 0 kelvina.
Nadam se da ćete s ovim informacijama saznati više o termodinamici i osnovnim principima.