Dans le monde de la physique, il existe une branche chargée d'étudier les transformations produites par la chaleur et le travail dans un système. Il s'agit du thermodynamique. C'est une branche de la physique qui est chargée d'étudier toutes les transformations qui résultent uniquement de processus impliquant des changements dans les variables d'état de température et d'énergie au niveau macroscopique.
Dans cet article, nous allons vous dire tout ce que vous devez savoir sur la thermodynamique et les principes de la thermodynamique.
Caractéristiques principales
Si nous faisons une analyse de la thermodynamique classique, nous voyons qu'elle est basée sur le concept de système macroscopique. Ce système n'est rien d'autre qu'une portion de masse physique ou conceptuelle séparée de l'environnement extérieur. Afin de mieux étudier les systèmes thermodynamiques, on suppose toujours qu'il s'agit d'une masse physique qui n'est pas perturbée par l'échange d'énergie avec l'écosystème externe.
L'état d'un système macroscopique qu'est-ce que dans des conditions d'équilibre, il est spécifié par des grandeurs appelées variables thermodynamiques. Toutes ces variables nous sont connues et sont la température, la pression, le volume et la composition chimique. Toutes ces variables définissent les systèmes et leur équilibre. Les principales notations de la thermodynamique chimique ont été établies grâce à l'union internationale appliquée. Avec ces unités, la loi de la thermodynamique peut être mieux travaillée et expliquée.
Cependant, il existe une branche de la thermodynamique qui n'étudie pas l'équilibre, mais est chargée d'analyser les processus thermodynamiques caractérisés principalement par ne pas avoir la capacité d'atteindre des conditions d'équilibre de manière stable.
lois
Les principes ont été dénoncés au XNUMXème siècle Isa ceux qui Ils sont chargés de réguler toutes les transformations et leur déroulement. Ils analysent également quelles sont les limites réelles pour avoir une vraie conception. Ce sont des axiomes qui ne peuvent être prouvés mais qui ne peuvent être démontrés sur la base de l'expérience. Chaque théorie de la thermodynamique est basée sur ces principes. On peut distinguer 3 principes de base plus le principe mais c'est celui qui définit la température et qui est implicite dans les 3 autres principes.
Loi zéro
Nous allons décrire ce qu'est cette loi zéro, qui est la première à décrire la température implicite dans le reste des principes. Lorsque deux systèmes interagissent l'un avec l'autre et sont en équilibre thermique, ils partagent certaines des propriétés. Ces propriétés qu'ils partagent les uns avec les autres peuvent être mesurées et attribuées à une valeur numérique. Par conséquent, si les deux systèmes sont en équilibre avec un troisième, ils seront en équilibre l'un avec l'autre et la propriété partagée est la température.
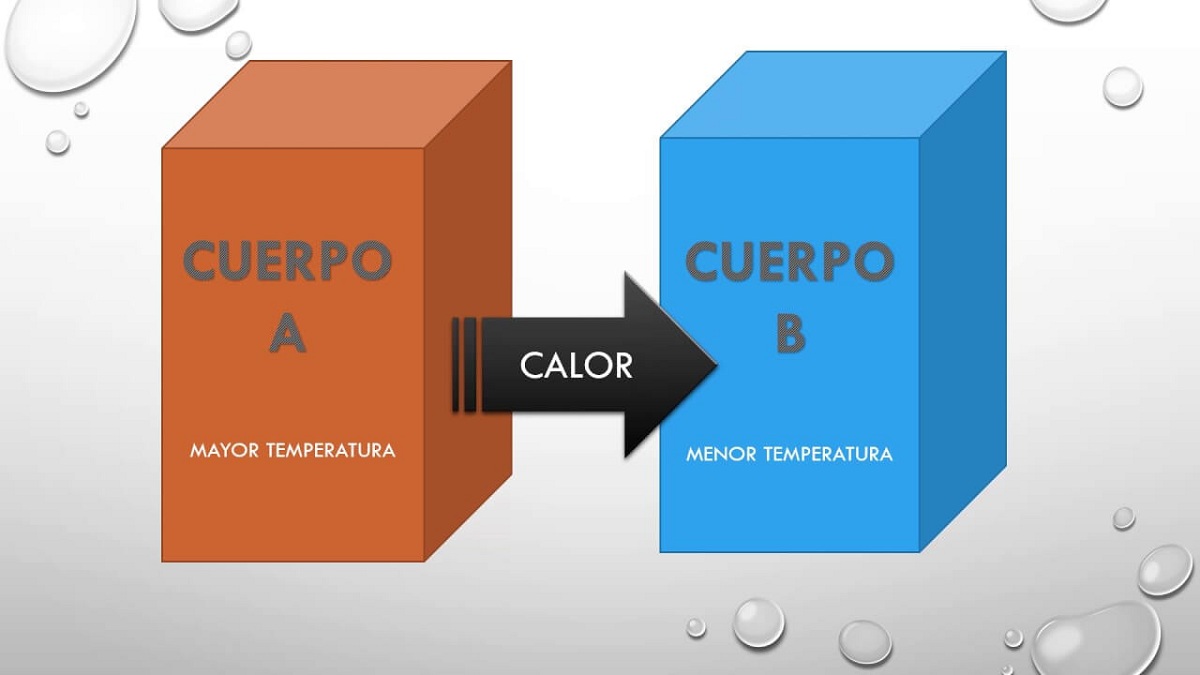
Par conséquent, ce principe indique simplement que si un corps A était en équilibre avec un corps B et ce corps B sera en équilibre thermique avec un corps C, alors les corps A et C seront également en équilibre thermique. Ce principe explique le fait que deux corps à des températures différentes peuvent échanger de la chaleur l'un avec l'autre. Tôt ou tard, les deux corps atteignent la même température, ils sont donc en équilibre total.
Première loi de la thermodynamique
Lorsqu'un corps est mis en contact avec un corps plus froid, il se produit une transformation qui conduit à un état d'équilibre. Cet état d'équilibre est basé sur le fait que la température des deux corps est égale car un transfert d'énergie est amélioré entre le corps chaud pour le corps froid. Afin d'expliquer ce phénomène, les scientifiques ont supposé qu'une substance chaude, présente en plus grande quantité, traversait un corps plus froid. On a pensé à un fluide qui pouvait se déplacer à travers la masse pour pouvoir échanger de la chaleur.
Ce principe est responsable de l'identification de la chaleur comme forme d'énergie. Ce n'est pas une substance matérielle. De cette manière, on pourrait montrer que la chaleur, qui se mesure en calories et le travail qui se mesure en joules, sont équivalents. Par conséquent, nous savons aujourd'hui que 1 calorie équivaut à environ 4,186 XNUMX joules.
On peut dire que le premier principe de la thermodynamique est un principe de conservation de l'énergie. Une quantité d'énergie dans un moteur thermique est convertie en travail et peut être vue par toute machine capable de produire un tel travail sans consommer d'énergie. On peut établir ce premier principe comme suit: la variation de l'énergie interne d'un système thermodynamique fermé est égale à la différence qui existe entre la chaleur fournie au système et le travail effectué par ledit système dans l'environnement.
Deuxième loi de la thermodynamique
Cela indique au départ qu'il est impossible de fabriquer une machine cyclique qui ne se traduit que par le transfert de chaleur d'un corps froid à un corps chaud. On peut dire qu'il est impossible qu'une transformation puisse être effectuée dont le résultat ne sera celui de convertir la chaleur que nous avons extraite d'une seule source en travail mécanique.
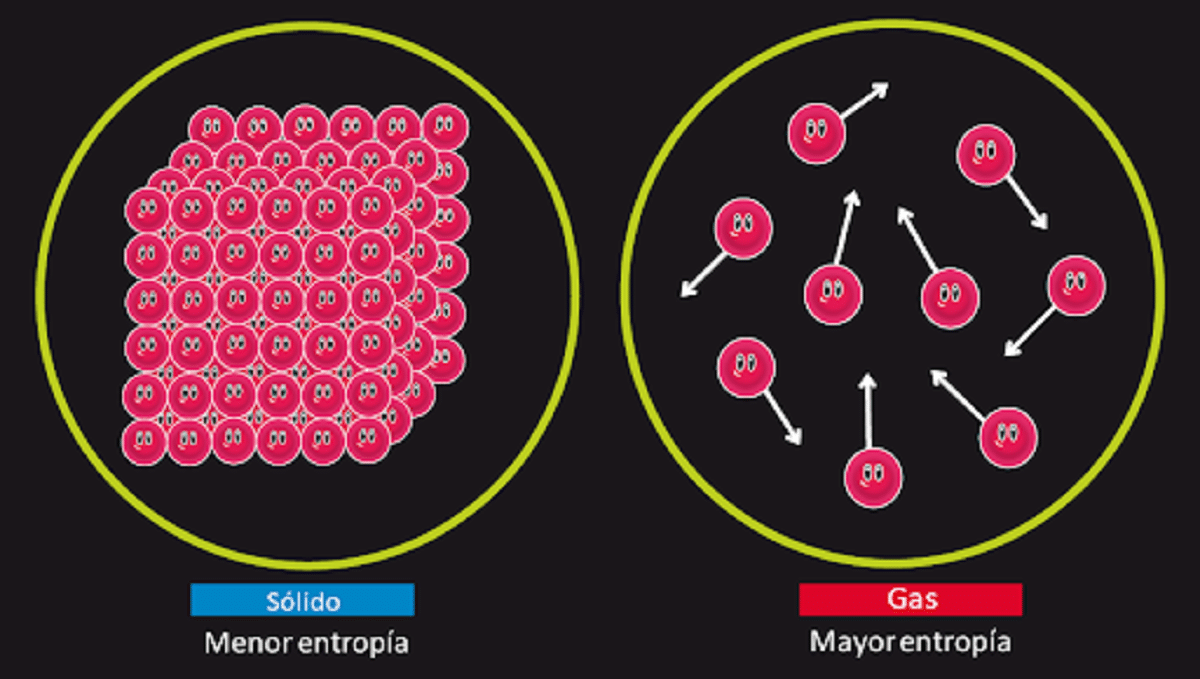
Ce principe est chargé de nier la possibilité que le mouvement perpétuel connu de la seconde espèce existe. Nous savons que le entropie d'un système reste isolé inchangé lorsqu'une transformation réversible a lieu. Nous savons également qu'elle augmente lorsqu'une transformation irréversible a lieu.
Troisième loi de la thermodynamique
Ce dernier principe est étroitement lié au second et est considéré comme une conséquence de celui-ci. Ce principe affirme que l'être absolu ne peut être atteint en couleur avec un nombre fini de transformations. On sait qu'il y a un zéro absolu qui n'est pas supérieur à la température minimale qui peut être atteinte. En unités Kelvin, nous savons qu'il est égal à 0, mais en degrés Celsius, il a une valeur de -273.15 degrés.
Il précise également que l'entropie d'un solide parfaitement cristallin avec une température de 0 kelvin est égale à 0. Cela signifie qu'il n'y aurait pas d'entropie, donc le système serait totalement stable. L'énergie de libération, de translation et de rotation des particules qui la composent ne serait rien à une température de 0 kelvin.
J'espère qu'avec ces informations, vous pourrez en apprendre davantage sur la thermodynamique et les principes de base.