Aujourd'hui, nous allons parler d'un isotope utilisé pour produire de l'énergie nucléaire. Il s'agit de deutérium. C'est l'une des espèces isotopiques de l'hydrogène et est représenté par le symbole D ou 2H. On lui a donné le nom commun d'hydrogène lourd parce que la masse est le double de celle du proton. Un isotope n'est rien de plus qu'une espèce qui provient du même élément chimique mais qui a un nombre de masse différent. Le deutérium est utilisé à diverses fins.
Par conséquent, nous allons dédier cet article pour vous parler de toutes les caractéristiques, structure, propriétés et utilisations du deutérium.
Caractéristiques principales
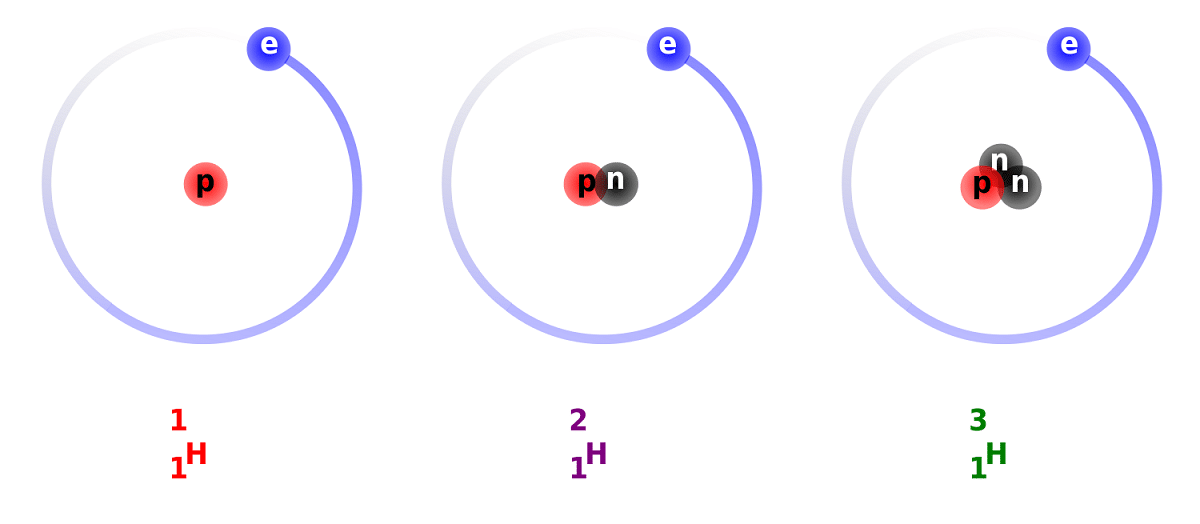
La distinction entre le deutérium et l'hydrogène est due à la différence du nombre de neutrons dont il dispose. Pour cette raison, le deutérium est considéré comme un isotope stable et peut être trouvé dans des composés formés par l'hydrogène d'origine totalement naturelle. Il faut garder à l'esprit que, bien qu'ils soient d'origine naturelle, ils se produisent dans une faible proportion. Compte tenu des propriétés qu'il a si similaires à l'hydrogène ordinaire, peut le remplacer dans son intégralité dans les réactions auxquelles il participe. De cette manière, il peut être converti en substances équivalentes.
Pour cette raison et pour d'autres, le deutérium a un grand nombre d'applications dans différents domaines de la science. Il est devenu au fil des ans l'un des éléments les plus importants pour la recherche et les progrès de la technologie et de l'information.
La structure principale de cet isotope est constituée d'un noyau qui a un proton et un neutron. Il a un poids atomique d'environ 2,014 XNUMX grammes. Cet isotope a été découvert grâce à Harold C. Urey, chimiste américain, et à ses collaborateurs Ferdinand Brickwedde et George Murphy, en 1931. La préparation pour rencontrer le deutérium à l'état pur a été réalisée avec succès pour la première fois en 1933. C'est déjà dans les années 50 qu'une phase solide qui a démontré une grande stabilité, connue sous le nom de deutéride de lithium, a commencé à être utilisée. Cette substance pourrait remplacer le deutérium et le tritium dans un grand nombre de réactions chimiques.
Les progrès de la science se produisent lorsqu'une substance est trouvée qui peut faciliter les réactions chimiques pour la génération de produits. En ce sens, si vous avez étudié l'abondance de cet isotope pour pouvoir observer certaines choses. On sait que la proportion de deutérium dans l'eau varie légèrement selon la zone où l'échantillon est prélevé. Certaines études de spectroscopie ont déterminé l'existence de cet isotope sur d'autres planètes de notre galaxie. Cela peut être d'une grande importance pour étudier la composition d'autres corps célestes.
Structure et origine du deutérium

Nous allons connaître quelques faits sur le deutérium. Comme nous l'avons mentionné précédemment, la principale différence entre les isotopes de l'hydrogène réside dans leur structure. Et est-ce que l'hydrogène, le deutérium et le tritium ont des quantités différentes de protons et de neutrons, de sorte qu'ils ont des propriétés chimiques différentes. Je dois également garder à l'esprit que le deutérium qui existe à l'intérieur d'autres corps stellaires est éliminé plus rapidement qu'il ne provient. C'est l'une des raisons pour lesquelles il est si difficile d'étudier la présence de deutérium dans les corps stellaires.
On considère que d'autres phénomènes de la nature forment une infime quantité de deutérium, de sorte que sa production continue de susciter un intérêt considérable aujourd'hui. D'après le pourcentage que nous avons mentionné précédemment sur la présence de deutérium dans la nature, il ne s'élève pas à 0.02%. Une série d'enquêtes scientifiques a révélé que la grande majorité des atomes qui ont été formés à partir de deutérium proviennent naturellement de l'explosion qui a donné lieu à l'origine de l'univers connu sous le nom de Big Bang. C'est l'une des principales raisons pour lesquelles on pense que le deutérium est présent dans les grandes planètes telles que Jupiter.
Le moyen le plus courant d'obtenir cet isotope naturellement est de les combiner avec de l'hydrogène. Lorsque cela se produit, il sera combiné sous la forme d'un protium. Les scientifiques souhaitent connaître la relation établie entre la proportion de le deutérium et l'hydrogène dans différents domaines scientifiques. Il est largement étudié dans les branches de la science comme l'astronomie ou la climatologie. Dans ces branches, il a quelques utilités pratiques pour connaître et comprendre l'univers et notre atmosphère.
Propriétés du deutérium

Nous allons savoir quelles sont les principales propriétés de cet isotope appartenant à l'hydrogène. La première chose à faire est de savoir ce qu'est un isotope dépourvu de caractéristiques radioactives. Cela signifie qu'il est de nature assez stable. Il peut être utilisé pour remplacer l'hydrogène dans diverses réactions chimiques. En ayant une grande stabilité naturellement, présente un comportement différent de l'hydrogène ordinaire. Cela se produit dans toutes les réactions de nature biochimique. Il faut savoir avant de substituer, que bien qu'il puisse être atteint en échangeant de l'hydrogène contre du deutérium dans des réactions chimiques, il est nécessaire de savoir qu'ils auront un comportement différent.
Lorsque les deux atomes d'hydrogène dans l'eau sont remplacés, un composé appelé eau lourde peut être obtenu. L'hydrogène présent dans l'océan et sous forme de deutérium il ne présente qu'une proportion de 0,016% par rapport au protium. Dans l'univers, cet isotope a tendance à fusionner plus rapidement pour donner naissance à l'hélium. Si nous combinons le deutérium avec l'oxygène atomique, nous voyons qu'il devient une espèce toxique. Malgré cela, et les propriétés chimiques ou très similaires à celles de l'hydrogène.
Une autre des propriétés de cet isotope est que lorsque des atomes de deutérium sont soumis au processus de fusion nucléaire à des températures élevées, de grandes quantités d'énergie peuvent être libérées. C'est l'exode, vous avez étudié pour pouvoir implanter la fusion nucléaire de notre planète. Certaines propriétés physiques telles que le point d'ébullition, la chaleur de vaporisation, le point triple et la densité ils ont des magnitudes supérieures à celles de l'hydrogène.
J'espère qu'avec ces informations, vous pourrez en savoir plus sur le deutérium et ses caractéristiques.