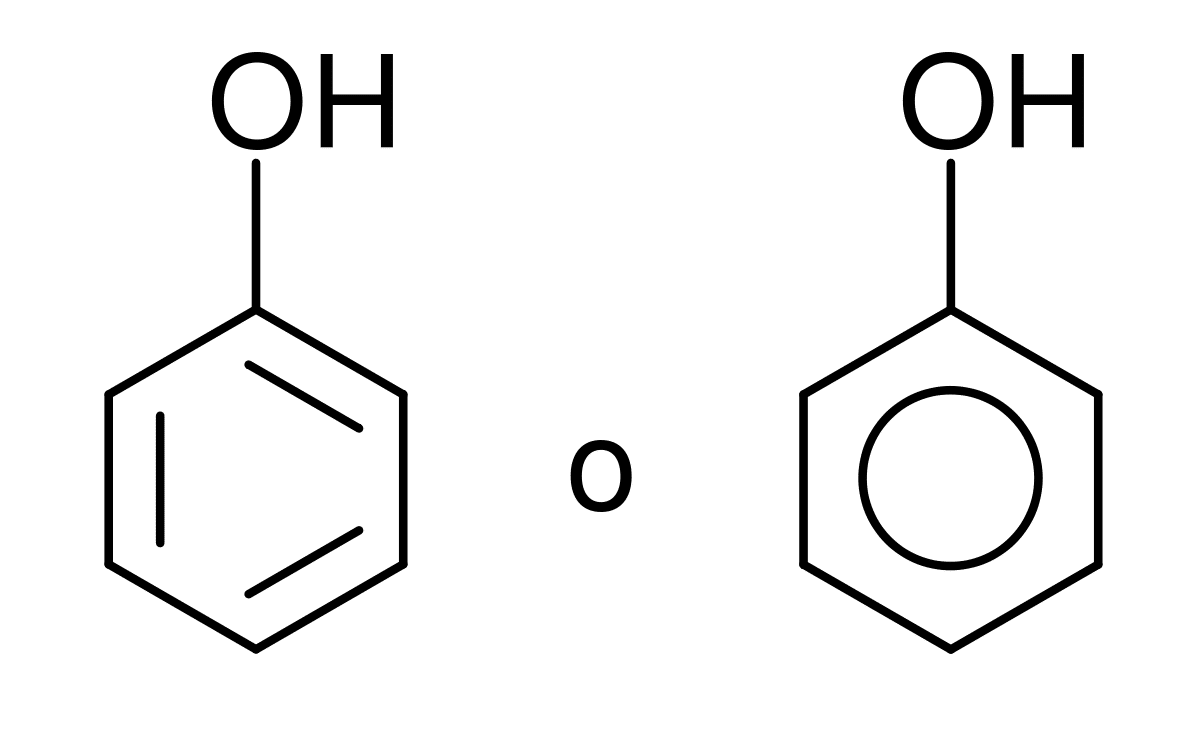
Група гідроксил Він складається з атома кисню та атома водню і нагадує молекулу води. Його можна знайти в різних хімічних формах, таких як група, іон або радикал. Для всіх тих людей, які вивчають органічну хімію, знання реакцій та значення цієї групи атомів є фундаментальним. І він здатний утворювати основні зв’язки з атомом вуглецю, хоча він може це робити також із сіркою та фосфором.
У цій статті ми розповімо вам про характеристики гідроксильної групи та її значення в органічній хімії.
ключові особливості
Коли ми аналізуємо гідроксильну групу з точки зору неорганічної хімії, ми бачимо, що вона більше бере участь як іон. Іншими словами, тип мережива, що існує між ним та металами, є не ковалентним, а іонним. Через це гідроксильна група стала важливим елементом, який допомагає визначити властивості та перетворення багатьох сполук.
Гідроксильна група приєднана до радикала, який визначений сз буквою R, якщо це алкіл, або з буквою Ar, якщо він ароматичний. Найбільше я знаю про науку - це те, що вносить гідроксильну групу в молекулу, в якій вона зв’язується. Найкращу відповідь можна знайти при дослідженні його протонів. І полягає в тому, що протони можуть захоплюватися сильними основами з утворенням солей. Це також може взаємодіяти з іншими оточуючими групами, які зв’язані між собою за допомогою водневих зв’язків. Крім того, найважливіше в гідроксильній групі полягає в тому, що, де б вона не була, вона може представляти потенційний регіон для утворення води.
Будова гідроксильної групи

Гідроксильна група стала досить цікавою молекулою з точки зору органічної хімії. Молекула води має кутоподібну форму і схожа на бумеранг. Якщо ми вирізаємо один з його кінців, що означає те саме, що і видалення протона, можуть виникати різні ситуації. Молекула води є перетворюється на гідроксильний радикал або гідроксильний іон. Однак обидва мають молекулярну лінійну геометрію і не є електронними.
Всі ці зв’язки пов’язані з тим, що вони орієнтовані на два атоми, щоб мати можливість постійно залишатися вирівняними. Те саме не стосується гібридних орбіталей. Ключовим для гідроксильної групи, що дозволяє різним молекулам змішуватися між собою, є водневі зв’язки. Ці водневі зв’язки самі по собі не міцні, однак із збільшенням кількості джерел та кількості гідроксильних груп у структурі ефекти множаться. Це збільшення кількості водневих зв’язків також відображається на фізичних властивостях сполуки.
Водневі зв’язки вимагають, щоб атоми були протилежними один одному. Є кілька атомів кисню однієї гідроксильної групи, які повинні бути розташовані таким чином, щоб він міг генерувати пряму лінію з воднем другої групи. Це дещо складніше, але це трапляється часто. Таким чином, виникають цілком конкретні просторові розташування, такі як що відбувається в структурі молекули ДНК. Це відбувається між азотистими основами, з яких складається ДНК.
Кількість гідроксильних груп можна назвати структурою, прямо пропорційною спорідненості води до молекули. Ми збираємось навести приклад, щоб краще це зрозуміти. Хоча цукор має гідрофобну структуру вуглецю, оскільки він має велику кількість гідроксильних груп, робить його дуже розчинним у воді.
Іони та їх функції
Гідроксильна група та іон дуже схожі, але мають різні хімічні властивості. Іон гідроксилу є надзвичайно сильною основою і працює шляхом захоплення протонів. Якщо змусити, це може перетворитися на воду. А це неповна молекула води, яка заряджена негативно і їй потрібен протон для добудови. З іншого боку, оскільки гідроксильна група йому не потрібно захоплювати протони, щоб завершити це поводиться як надзвичайно слабка база. Він здатний віддавати протони, хоча робить це лише проти дуже сильних основ.
Позитивні ядра - це атоми в молекулі, які страждають від електронного дефіциту в результаті свого електронегативного середовища.
Гідроксильна група та метеорологія

Ми знаємо, що він діє як вид миючого засобу в повітрі, який розщеплює інші гази. Ми знаємо, що гідроксильна група є основним контролем концентрації метану. Газ метан - парниковий газ, який лише перевищує концентрацію на вуглекислий газ у його внеску в глобальне потепління. Незважаючи на те, що газ метан знаходиться в атмосфері в меншій мірі, він здатний утримувати більшу кількість тепла, ніж вуглекислий газ.
Існує нове дослідження під керівництвом наукового співробітника NASA, яке показало, що гідроксильні радикали рециркулюють себе і здатні підтримувати постійну атмосферну концентрацію. Ця концентрація зберігається з часом, навіть якщо викиди метану збільшуються. Тому розуміння ролі гідроксилу є важливим для розуміння терміну корисного використання метану та атмосфери.
Вчені відзначають, що збільшення концентрацій та викидів метану може призвести до виснаження кількості гідроксильних радикалів у глобальному масштабі. Таким чином, термін корисного використання метану буде продовжений, що призведе до глобального потепління. Збільшуючи тривалість життя метану, нам не було б чим очистити атмосферу. Спостерігали первинні джерела гідроксилу та метану та їх реакцію. Переробка цієї групи відбувається після розпаду метану, а потім реформування в присутності інших газів. Концентрації гідроксилу з часом є досить стабільними. Вони не обов'язково повинні зникати, коли він реагує з метаном.
Я сподіваюся, що за допомогою цієї інформації ви зможете дізнатись більше про гідроксильну групу та про все її значення.