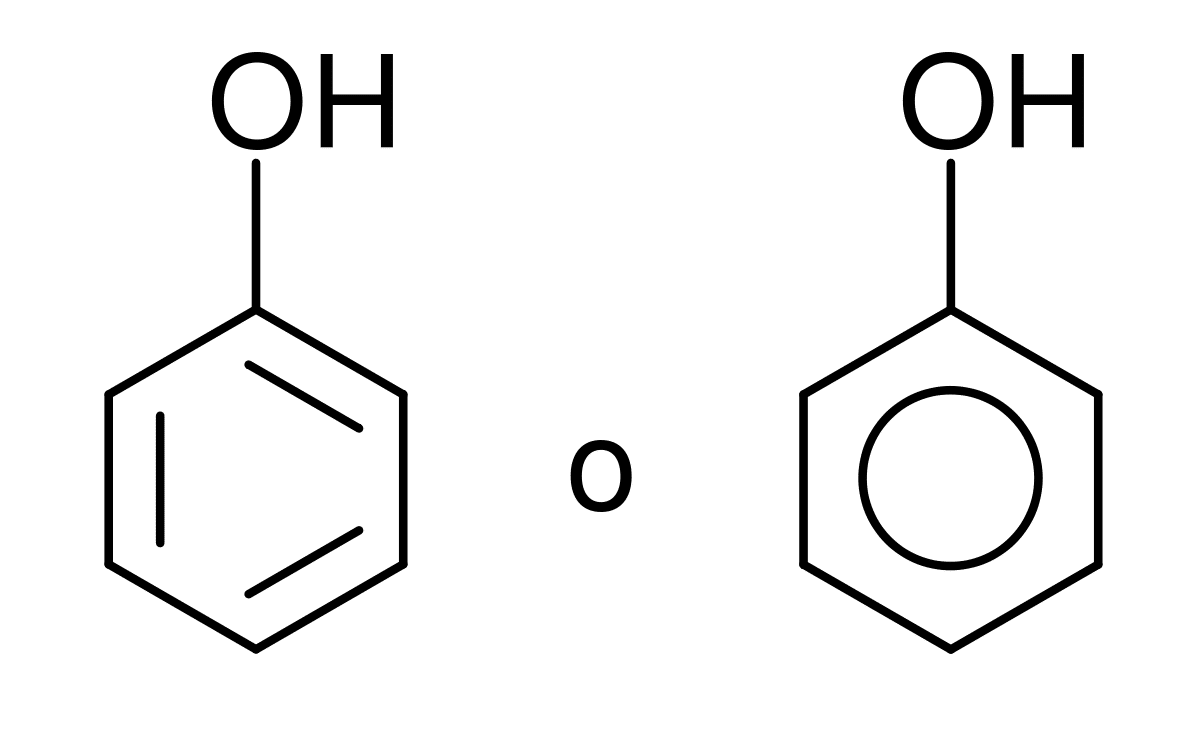
Grup hidroksil Bir oksijen atomu ve bir hidrojen atomundan oluşan ve bir su molekülüne benzeyen olandır. Bir grup, bir iyon veya bir radikal gibi çeşitli kimyasal formlarda bulunabilir. Organik kimya üzerine çalışan tüm insanlar için, bu atom grubunun reaksiyonlarını ve önemini bilmek çok önemlidir. Kükürt ve fosforla da yapabilmesine rağmen, karbon atomuyla temel bağlar oluşturabilir.
Bu yazımızda sizlere hidroksil grubunun özelliklerini ve organik kimyadaki önemini anlatacağız.
temel özellikleri
Hidroksil grubunu inorganik kimya açısından analiz ettiğimizde daha çok iyon olarak katıldığını görürüz. Yani metallerle arasında var olan dantel türü kovalent değil iyoniktir. Bu nedenle, hidroksil grubu, birçok bileşiğin özelliklerini ve dönüşümlerini tanımlamaya yardımcı olan önemli bir element haline gelmiştir.
Hidroksil grubu, c olarak tanımlanan bir köke bağlanıralkil ise R harfi ile, aromatik ise Ar harfi ile. Bilim hakkında en çok bildiğim şey, hidroksil grubunun bağlandığı moleküle katkıda bulunan şeydir. En iyi cevap, protonlarının incelenmesinde bulunur. Ve protonlar, tuz oluşturabilmek için güçlü bazlar tarafından alınabilir. Bu, hidrojen bağları ile birbirine bağlanan diğer çevre gruplarla da etkileşime girebilir. Ek olarak, hidroksil grubu ile ilgili en önemli şey, nerede olursa olsun, su oluşumu için potansiyel bir bölgeyi temsil edebilmesidir.
Hidroksil grubunun yapısı

Hidroksil grubu, organik kimya açısından oldukça ilginç bir molekül haline geldi. Su molekülü köşelidir ve bir bumerang gibi görünür. Uçlarından birini kesersek, bu bir protonu çıkarmakla aynı anlama gelir, çeşitli durumlar ortaya çıkabilir. Su molekülü hidroksil radikaline veya hidroksil iyonuna dönüştürülür. Bununla birlikte, her ikisinin de doğrusal bir moleküler geometrisi vardır ve elektronik değildir.
Tüm bu bağlar, her zaman aynı hizada kalabilmek için iki atoma yönelik olmaları gerçeğinden kaynaklanmaktadır. Aynısı hibrit orbitaller için geçerli değildir. Hidroksil grubunun farklı moleküllerin birbiriyle karışmasına izin vermesinin anahtarı, hidrojen bağlarına ihtiyaç duyar. Bu hidrojen bağları kendi başlarına güçlü değildir, ancak kaynakların sayısı arttıkça ve bir yapıdaki hidroksil gruplarının sayısı arttıkça etkiler de artar. Hidrojen bağlarının sayısındaki bu artış, bileşiğin fiziksel özelliklerine de yansır.
Hidrojen bağları, atomların birbirinin karşısına yerleştirilmesini gerektirir. Bir hidroksil grubunun, ikinci bir grubun hidrojeni ile düz bir çizgi oluşturabilecek şekilde düzenlenmesi gereken bazı oksijen atomları vardır. Bu biraz daha karmaşık ama sık sık oluyor. Bu şekilde, oldukça özel mekansal düzenlemeler ortaya çıkar. DNA molekülünün yapısında ne olur. Bu, DNA'yı oluşturan azotlu bazlar arasında gerçekleşir.
Hidroksil gruplarının sayısına, suyun moleküle afinitesi ile doğru orantılı bir yapı diyebiliriz. Daha iyi anlamak için bir örnek vereceğiz. Şeker, hidrofobik karbon yapısına sahip olmasına rağmen, çok sayıda hidroksil grubuna sahip olduğu için, suda çok çözünür hale getirir.
İyonlar ve işlevleri
Hidroksil grubu ve iyon çok benzerdir ancak farklı kimyasal özelliklere sahiptir. Hidroksil iyonu son derece güçlü bir bazdır ve protonları yakalayarak çalışır. Zorlarsak suya dönüşebilir. Ve bu, negatif yüklü ve tamamlanması için bir protona ihtiyaç duyan eksik bir su molekülüdür. Öte yandan, hidroksil grubu Tamamlamak için protonları yakalamasına gerek yoktur, son derece zayıf bir temel gibi davranır. Proton bağışlama yeteneğine sahiptir, ancak bunu yalnızca çok güçlü olan bazlara karşı yapar.
Pozitif çekirdekler, elektronegatif ortamlarının bir sonucu olarak bir elektronik eksiklikten muzdarip bir moleküldeki atomlardır.
Hidroksil grubu ve meteoroloji

Havada diğer gazları parçalayan bir deterjan türü olduğunu biliyoruz. Hidroksil grubunun metan konsantrasyonunun ana kontrolü olduğunu biliyoruz. Metan gazı, konsantrasyon olarak yalnızca aşılan bir sera gazıdır. küresel ısınmaya katkısında karbondioksit. Metan gazı atmosferde daha az bulunmasına rağmen, karbondioksitten daha fazla miktarda ısı tutma kapasitesine sahiptir.
Hidroksil radikallerinin kendilerini geri dönüştürdüğünü gösteren bir NASA doktora sonrası araştırmacı tarafından yürütülen yeni bir araştırma var. sabit bir atmosferik konsantrasyonu koruyabilen. Bu konsantrasyon, metan emisyonları artsa bile zamanla korunur. Bu nedenle, metanın ve atmosferin yararlı ömrünü anlamak için hidroksilin rolünü anlamak çok önemlidir.
Bilim adamları, artan metan gazı konsantrasyonlarının ve emisyonlarının, hidroksil radikallerinin miktarının küresel ölçekte tükenmesine neden olabileceğine işaret ettiler. Böylelikle metanın faydalı ömrü uzayacak, bu da küresel ısınmaya katkıda bulunacak bir sorun. Metanın ömrünü uzatırsak, atmosferi temizleyecek hiçbir şeyimiz kalmazdı. Hidroksil ve metanın birincil kaynakları ve nasıl tepki verdikleri gözlemlenmiştir. Bu grubun geri dönüşümü metan ayrıştıktan sonra gerçekleşir ve daha sonra diğer gazların varlığında yeniden oluşur.. Hidroksil konsantrasyonları zaman içinde oldukça kararlıdır. Metanla reaksiyona girdiğinde mutlaka yok olmaları gerekmez.
Umarım bu bilgilerle hidroksil grubu ve tüm önemi hakkında daha fazla bilgi edinebilirsiniz.