
Sa parehong pisika at kimika isang konsepto ang ginagamit upang masukat ang lakas na nilalaman sa katawan. Pinag-uusapan natin ang tungkol sa entalpy. Ito ay isang uri ng pagsukat na nagpapahiwatig ng dami ng enerhiya na nilalaman sa isang katawan o system na may isang tiyak na lakas ng tunog, na nasa ilalim ng presyon at na maaaring ipagpalit sa kapaligiran. Ang entalpy ng isang sistema ay kinakatawan ng letrang H at ang pisikal na yunit na nauugnay dito upang ipahiwatig ang mga halaga ng enerhiya ay ang Joule.
Sa artikulong ito sasabihin namin sa iyo ang lahat ng mga katangian at kahalagahan ng entalpy.
pangunahing katangian
Maaari nating sabihin na ang entalpy ay katumbas ng panloob na enerhiya na ang system ay may plus ang presyon beses ang dami ng parehong system. Kapag nakita natin na ang enerhiya ng system, ang presyon at ang dami ay mga pagpapaandar ng estado, ang entalpy ay din. Nangangahulugan ito na, pagdating ng oras, maaari itong mangyari sa ilang mga pangwakas na paunang kondisyon upang ang variable ay makakatulong upang mapag-aralan ang buong sistema bilang isang buo.
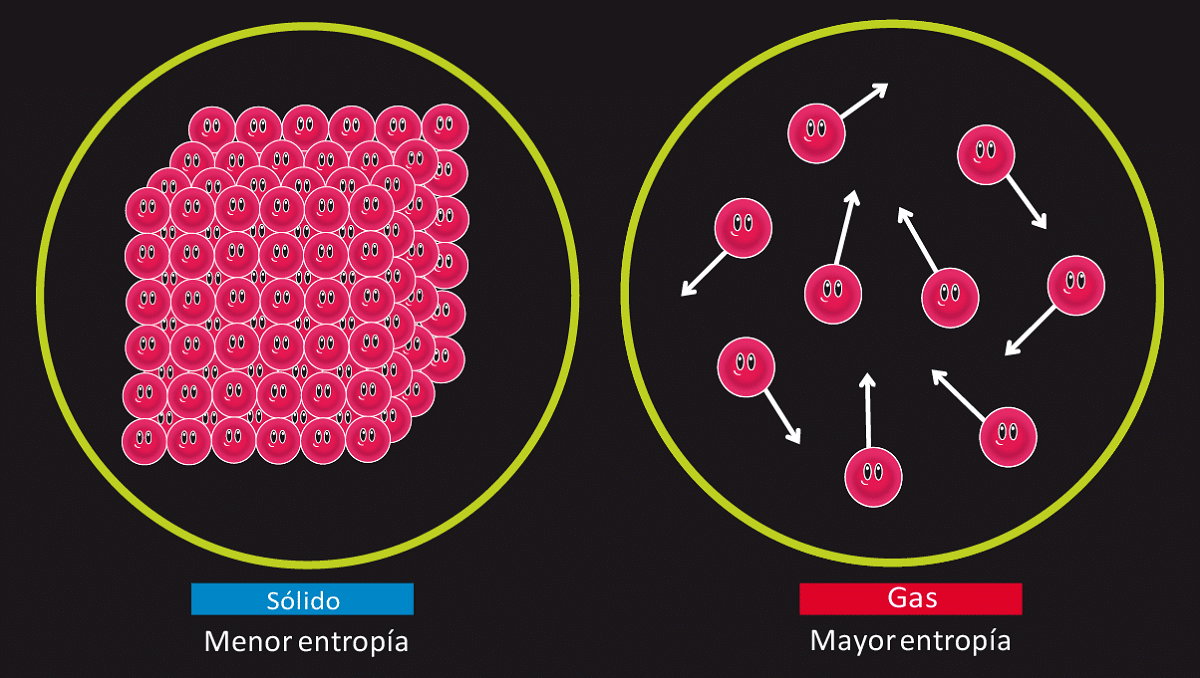
Ang unang bagay ay upang malaman kung ano ang entalpy ng pagbuo. Ito ay tungkol hinihigop ang init na nakalimutan ng system kapag ang 1 taling ng sangkap ng produkto ay ginawa mula sa mga elemento sa normal na estado. Ang mga estado na ito ay maaaring maging solid, likido o gas o sa kaso ng solusyon. Ang estado ng allotropic ay ang pinaka matatag na estado. Halimbawa, ang pinaka-matatag na estado ng allotropic na mayroon ang carbon ay ang grapayt, bilang karagdagan sa ilalim ng normal na mga kondisyon kung saan ang mga halaga ng depression ay Ang 1 kapaligiran at temperatura ay 25 degree.
Binibigyang diin namin na ang mga entalpiyo ng pormasyon ayon sa tinukoy namin ay para sa 1 taling ng tambalang ginawa. Sa ganitong paraan, nakasalalay sa dami ng mga umiiral na mga produktong reagent, ang reaksyon ay dapat na ayusin sa mga praksyonal na koepisyent.
Entralpy na pormasyon

Alam namin na sa anumang proseso ng kemikal, ang entalpy ng pagbuo ay maaaring parehong positibo at negatibo. Ang entalpy na ito ay positibo kapag ang reaksyon ay endothermic. Na ang isang reaksyong kemikal na endothermic ay nangangahulugang maaari itong makuha ang init ng daluyan. Sa kabilang kamay, mayroon kaming isang negatibong entalpy kapag ang reaksyon ay exothermic. Ang isang reaksyong kemikal na exothermic ay nangangahulugang naglalabas ito ng init mula sa system hanggang sa labas.
Para sa isang exothermic na reaksyon na maganap, ang mga reactant ay dapat magkaroon ng mas mataas na enerhiya kaysa sa mga produkto. Sa kabaligtaran, para sa isang endothermic na reaksyon na maganap ang mga reactant ay dapat magkaroon ng mas kaunting enerhiya kaysa sa mga produkto. Upang ang equation ng kemikal ng lahat ng ito ay maaaring nakasulat nang maayos, kinakailangang sumunod sa batas ng pangangalaga ng bagay. Iyon ay, ang equation ng kemikal ay dapat maglaman ng impormasyon tungkol sa pisikal na estado ng mga reactant at produkto. Ito ay kilala bilang estado ng pagsasama-sama
Kailangan mo ring tandaan iyon ang mga sangkap na dalisay ay mayroong isang entalpy na pormasyon na katumbas ng zero. Ang mga halagang entalpy na ito ay nakuha sa ilalim ng karaniwang mga kundisyon, tulad ng mga nabanggit sa itaas, at sa kanilang pinaka-matatag na form. Sa isang kemikal na sistema kung saan may mga reactant at produkto, ang entalpy na reaksyon ay katumbas ng entalpy ng pormasyon sa ilalim ng karaniwang mga kondisyon.
Alam namin na ang entalpy ng mga halaga ng pagbuo ng ilang mga inorganic at organic na kemikal na compound ay itinatag sa mga kondisyon ng 1 kapaligiran ng presyon at 25 degree na temperatura.
Enthalpy ng reaksyon
Nabanggit na namin kung ano ang entalpy ng pormasyon. Ngayon ay ilalarawan namin kung ano ang entalpy ng reaksyon. Ito ay isang thermodynamic function na makakatulong upang kalkulahin ang init na nakuha o ang init na naihatid sa panahon ng reaksyong kemikal. Ang balanse ng trainer ay hinahangad, nananatili o tumatanggap ng parehong mga reagent at mga produkto. Ang isa sa mga aspeto na dapat matupad upang makalkula ang entalpy ng reaksyon ay ang reaksyon mismo ay dapat mangyari sa patuloy na presyon. Sa madaling salita, sa buong panahon na kinakailangan upang maganap ang reaksyong kemikal, ang presyon ay dapat panatilihing pare-pareho.
Alam namin na ang entalpy ay may sukat ng enerhiya at iyon ang dahilan kung bakit ito sinusukat sa mga joule. Upang maunawaan ang ugnayan ng entalpy sa init na ipinagpapalit habang reaksyon ng kemikal kinakailangan upang pumunta sa unang batas ng thermodynamics. At ito ang unang batas na ito na nagsasabi sa atin na ang init na ipinagpapalit sa isang proseso na thermodynamic ay katumbas ng pagkakaiba-iba ng panloob na enerhiya ng sangkap o sangkap na kasangkot sa proseso kasama ang gawaing ginawa ng nasabing mga sangkap sa panahon ng proseso.
Alam natin na ang lahat ng mga reaksyong kemikal ay hindi hihigit sa iba`t ibang mga proseso ng thermodynamic na nangyayari sa isang tiyak na presyon. Ang pinaka-karaniwang mga halaga ng presyon ay ibinibigay sa ilalim ng karaniwang mga kondisyon ng presyon ng atmospera. Samakatuwid, ang lahat ng mga proseso ng thermodynamic na nagaganap sa ganitong paraan ay tinatawag na isobaric, dahil nangyayari ito sa patuloy na presyon.
Ito ay napaka-pangkaraniwan na tawagan ang entalpy heat. Gayunpaman, dapat na malinaw na hindi ito pareho sa init, ngunit palitan ng init. Iyon ay, hindi ang init ang maaaring magturo ng isang aralin o ang panloob na init na mayroon ang mga reactant at produkto. Ito ang init na ipinagpapalit sa buong proseso ng reaksyon ng kemikal.
Relasyon sa init
Hindi tulad ng napag-usapan natin dati, ang entalpy ay isang pagpapaandar ng estado. Kapag kinakalkula namin ang pagbabago ng entalpy, talagang kinakalkula namin ang pagkakaiba ng dalawang pagpapaandar. Ang mga pagpapaandar na ito ay karaniwang nakasalalay nang eksklusibo sa estado ng system. Ang estado ng system na ito ay nag-iiba depende sa panloob na enerhiya at dami ng system mismo. Dahil alam natin na ang bersyon ay nananatiling pare-pareho sa buong reaksyong kemikal, ang entalpy ng reaksyon ay hindi hihigit sa isang pagpapaandar ng estado na nakasalalay sa parehong panloob na enerhiya at dami.
Samakatuwid, maaari nating tukuyin ang entalpy ng mga reactant sa isang reaksyong kemikal bilang kabuuan ng bawat isa sa kanila. Sa kabilang banda, tinutukoy namin ang parehong bagay ngunit sa mga produkto bilang kabuuan ng entalpy ng lahat ng mga produkto.
Inaasahan ko na sa impormasyong ito maaari kang matuto nang higit pa tungkol sa entalpy at mga katangian nito.
