
La Boyles lag den upptäcktes av Robert Boyle på XNUMX-talet och lade grunden för att förklara sambandet mellan tryck och volym som finns i gaser. Genom en rad experiment lyckades han visa att om temperaturen är konstant, minskar en gas sin volym när den utsätts för mer tryck, och ökar i volym om trycket sänks.
I den här artikeln kommer vi att berätta allt du behöver veta om Boyles lag, dess egenskaper och betydelse.
Huvudegenskaper
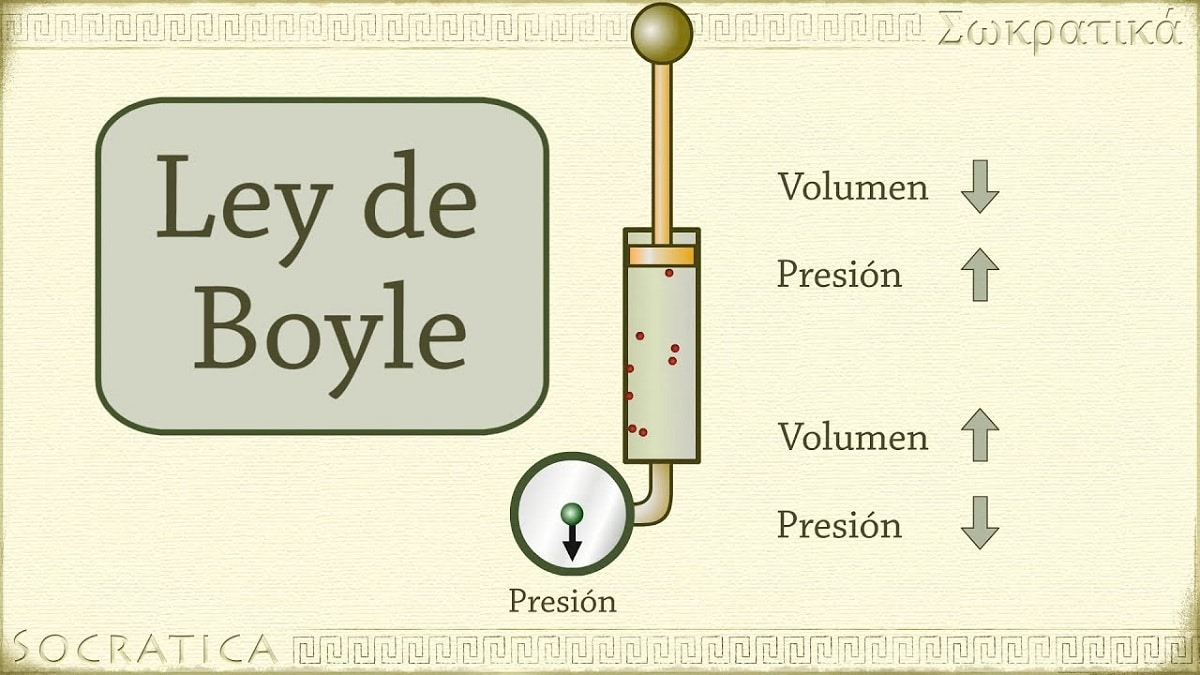
1662 upptäckte Robert Boyle att trycket som utövas på en gas är omvänt proportionellt mot dess volym och antal mol vid konstant temperatur. Med andra ord, om trycket som appliceras på en gas fördubblas, samma gas kommer att komprimeras och dess volym kommer att halveras.
När volymen av behållaren som innehåller gasen ökar, ökar också avståndet som partiklarna måste färdas innan de kolliderar med behållarens väggar. Denna ökning av avståndet gör att frekvensen av stötarna minskar, så trycket på väggen är mindre än tidigare när volymen var mindre.
Boyles lag upptäcktes första gången 1662 av Robert Boyle. Edme Mariotte var en annan vetenskapsman som tänkte och kom fram till samma slutsatser som BoyleMariotte offentliggjorde dock inte sitt arbete förrän 1676. Det är därför vi i många böcker hittar denna lag som kallas Boyle och Mariots lag Boyle-Mariots lag, även känd som Mattuts lag, utvecklad av den brittiske fysikern och kemisten Robert. Den formulerades oberoende av Boyle och den franske fysikern och botanikern Edmé Mattout.
Det hänvisar till en av de lagar som relaterar volymen och trycket hos en gas till en viss mängd gas som hålls vid en konstant temperatur. Boyles lag säger följande: Trycket som utövas av en kraft är fysiskt omvänt proportionellt mot volymen av gasformigt material så länge dess temperatur förblir konstant. Eller enklare, vi kan tolka det som: vid en högre konstant temperatur är volymen av en fast gasmassa omvänt proportionell mot det konstanta trycket den utövar.
Experiment och tillämpningar av Boyles lag

För att bevisa teorin om Boyles lag var Mariot ansvarig för att införa gas i en cylinder med en kolv och kunde verifiera de olika trycken som skapades när kolven sänktes. Man drar slutsatsen från detta experiment att när volymen ökar, minskar trycket.
Boyles lag har många tillämpningar i det moderna livet, bland vilka vi till exempel kan nämna dykning, detta beror på att dykaren måste driva ut luften från sina lungor när den stiger upp eftersom den expanderar när trycket minskar, om man inte gör det kan det orsaka vävnadsskador.
Det finns i all utrustning som använder eller drivs av pneumatisk kraft, till exempel robotarmar som använder komponenter som pneumatiska kolvar, ställdon, tryckregulatorer och övertrycksventiler.
Bensin-, gas- eller dieselmotorer använder också Boyles lag under förbränning, eftersom luft första gången kommer in i cylindern med volym och tryck, andra gången minskar den volymen genom att öka trycket.
Bilar har krockkuddesystem som fungerar genom att stöta ut en viss mängd luft eller gas från en kammare som når den yttre krockkudden, där trycket minskar och volymen ökar med en konstant temperatur.
Boyles lag är mycket viktig idag eftersom det är lagen som talar till oss och förklarar gasernas beteende. Det förklarar definitivt att trycket och volymen av en gas är omvänt proportionella mot varandra. Därför, när tryck appliceras på en gas, minskar dess volym och dess tryck ökar.
idealisk gasmodell

Boyle-Mariottes lag gäller för så kallade idealgaser, en teoretisk modell som avsevärt förenklar beteendet hos vilken gas som helst, förutsatt att:
- gasmolekyler de är så små att det inte är nödvändigt att tänka på deras storlek, särskilt med tanke på att detta är mycket mindre än avståndet de reser.
- Dessutom, molekylerna samverkar knappt, förutom när de kolliderar mycket kort, och när de gör det, är kollisionen elastisk, så både momentum och kinetisk energi bevaras.
- Antag slutligen att denna kinetiska energi är proportionell mot temperaturen på det gasformiga provet, dvs. ju mer omrörda partiklarna är, desto högre temperatur.
Lätta gaser, oavsett deras identitet, följer dessa riktlinjer mycket strikt under standardförhållanden för temperatur och tryck (dvs: 0ºC och atmosfärstryck (1 atmosfär). För dessa gaser beskriver Boyle-Mariotte-lagen deras beteende mycket exakt. .
Eftersom P∙V är konstant vid en given temperatur, om gasens tryck ändras, ändras volymen så att produkten förblir densamma, så i två olika tillstånd 1 och 2 kan likheten uttryckas enligt följande:
P1∙V1 = P2∙V2
Om du sedan känner till ett tillstånd, plus en variabel från det andra tillståndet, kan du känna till den saknade variabeln genom att ta bort den från Boyle-Mariot-lagen.
Boyles lags historia
brittisk kemist. Pionjär inom experiment inom kemiområdet, särskilt när det gäller egenskaperna hos gaser,
Robert Boyles avhandling om materiens beteende på partikelnivå var en föregångare till den moderna teorin om kemiska grundämnen. Han var också en av grundarna av Royal Society of London.
Robert Boyle föddes i en adlig familj i Irland och gick i de bästa engelska och europeiska skolorna. Från 1656 till 1668 tjänstgjorde han som Robert Hookes assistent vid Oxford University, och samarbetade med honom i en serie experiment som bestämde luftens fysiska egenskaper och hur den brinner, andas och överför ljud.
Resultaten av dessa bidrag samlades i deras "Nya fysisk-mekaniska experiment om luftens elasticitet och dess effekter» (1660). I den andra upplagan av detta arbete (1662) avslöjade han den berömda egenskapen hos gaser, Boyle-Mariottes lag, som angav att volymen som upptas av en gas vid konstant temperatur är omvänt proportionell mot dess tryck. Idag är det känt att denna lag är uppfylld endast när det teoretiska ideala beteendet hos gaser accepteras.
Jag hoppas att du med denna information kan lära dig mer om Boyles lag, dess egenskaper och tillämpningar i vetenskapens värld.