Данас ћемо разговарати о изотопу који се користи за производњу нуклеарне енергије. Ради се о деутеријум. Једна је од изотопских врста водоника и представљена је симболом Д или 2Х. Добио је заједнички назив тешки водоник јер је маса двоструко већа од протона. Изотоп није ништа друго до врста која потиче од истог хемијског елемента, али има другачији масени број. Деутеријум се користи у разне сврхе.
Стога ћемо посветити овај чланак да бисмо вам испричали све карактеристике, структуру, својства и употребу деутерија.
Главне карактеристике
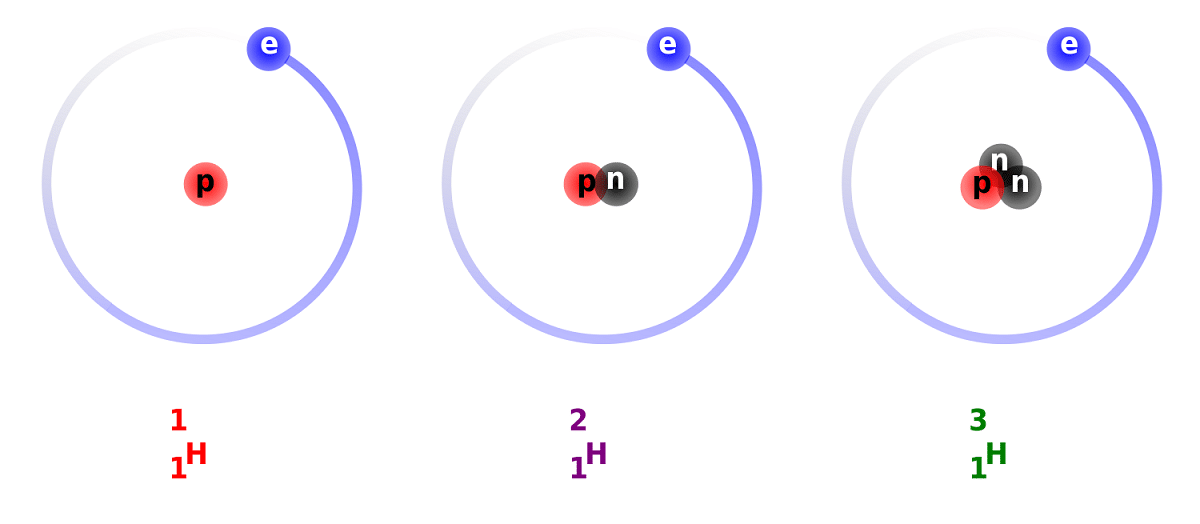
Разлика између деутерија и водоника настаје због разлике у броју неутрона које има. Из тог разлога, деутеријум се сматра стабилним изотопом и може се наћи у једињењима формираним од водоника потпуно природног порекла. Мора се узети у обзир да, иако су природног порекла, јављају се у малом проценту. С обзиром на својства која има толико слична обичном водонику, може га у целини заменити у реакцијама у којима учествује. На тај начин се може претворити у еквивалентне супстанце.
Из овог и других разлога, деутеријум има велики број примена у различитим областима науке. Током година постао је један од најважнијих елемената за истраживање и напредак у технологији и информацијама.
Главну структуру овог изотопа чини језгро које има протон и неутрон. Има атомску тежину од приближно 2,014 грама. Овај изотоп је откривен захваљујући Харолду Ц. Уреиу, хемичару из Сједињених Држава, и његовим сарадницима Фердинанду Брицкведдеу и Георгеу Мурпхију, 1931. Припрема за сусрет са деутеријумом у чистом стању први пут је успешно изведена 1933. године. Већ је педесетих година 50. века почела да се користи чврста фаза која је показала велику стабилност, позната као литијум деутерид. Ова супстанца би могла да замени деутеријум и тритијум у великом броју хемијских реакција.
Напредак у науци настаје када се пронађе супстанца која може да олакша хемијске реакције за стварање производа. У том смислу, ако сте проучавали обиље овог изотопа да бисте могли да посматрате одређене ствари. Познато је да удео деутерија у води незнатно варира у зависности од подручја на којем се узима узорак. Постоје неке студије спектроскопије које су утврдили постојање овог изотопа на другим планетама у нашој галаксији. Ово може бити од велике важности за проучавање састава других небеских тела.
Структура и порекло деутерија

Знаћемо неке чињенице о деутеријуму. Као што смо већ поменули, главна разлика између изотопа водоника лежи у њиховој структури. А да ли водоник, деутеријум и тритијум имају различите количине протона и неутрона, па имају различита хемијска својства. Такође морам узети у обзир да се деутеријум који постоји унутар других звезданих тела елиминише великом брзином него што је настао. То је један од разлога зашто је тако тешко проучавати присуство деутерија у звезданим телима.
Сматра се да други феномени природе формирају сићушну количину деутерија, па његова производња и данас изазива значајно интересовање. Из процента који смо раније помињали у вези са присуством деутерија у природи, не износи 0.02%. Низ научних истраживања открио је да је велика већина атома насталих из деутерија природно настала у експлозији која је довела до настанка свемира познатог као Биг Банг. То су један од главних разлога због којих се сматра да је деутеријум присутан на великим планетама попут Јупитера.
Најчешћи начин да се овај изотоп добије природним путем је када се комбинују са водоником. Када се то догоди, биће комбиновано у облику противума. Научнике занима сазнање о односу успостављеном између удела деутеријум и водоник у различитим областима науке. Широко се проучава у научним гранама као што су астрономија или климатологија. У овим гранама има неколико практичних програма за познавање и разумевање универзума и наше атмосфере.
Особине деутерија

Сазнаћемо која су главна својства овог изотопа који припада водонику. Прво што треба учинити је знати шта је изотоп лишен радиоактивних карактеристика. То значи да је прилично стабилне природе. Може се користити за замену водоника у разним хемијским реакцијама. Имајући велику стабилност природно, показује другачије понашање од обичног водоника. То се дешава у свим реакцијама које имају биохемијску природу. Пре замене потребно је знати да, иако се то може постићи разменом водоника за деутеријум у хемијским реакцијама, мора се знати да ће се они понашати другачије.
Када замените два атома водоника у води, можете добити једињење познато као тешка вода. Водоник који је присутан у океану и који је у облику деутерија представља само удео од 0,016% у односу на против. У свемиру овај изотоп има тенденцију да се брже стапа и ствара хелијум. Ако комбинујемо деутеријум са атомским кисеоником, видимо да он постаје токсична врста. Упркос томе, и хемијским својствима или врло сличним особинама водоника.
Још једно од својстава овог изотопа је да када се атоми деутерија подвргну процесу нуклеарне фузије на високим температурама, могу се ослободити велике количине енергије. То је егзодус, ви сте проучавали да бисте могли да примените нуклеарну фузију наше планете. Нека физичка својства као што су тачка кључања, топлота испаравања, трострука тачка и густина поседују величине веће од водоника.
Надам се да ћете помоћу ових информација сазнати више о деутеријуму и његовим карактеристикама.