
Tako v fiziki kot v kemiji se koncept uporablja za merjenje energije, ki jo vsebuje telo. Govorimo o entalpija. To je vrsta merjenja, ki označuje količino energije v telesu ali sistemu, ki ima določeno prostornino, ki je pod pritiskom in jo je mogoče izmenjati z okoljem. Entalpijo sistema predstavlja črka H, fizična enota, povezana z njo, ki označuje energijske vrednosti, pa je Joule.
V tem članku vam bomo predstavili vse značilnosti in pomen entalpije.
Glavne značilnosti
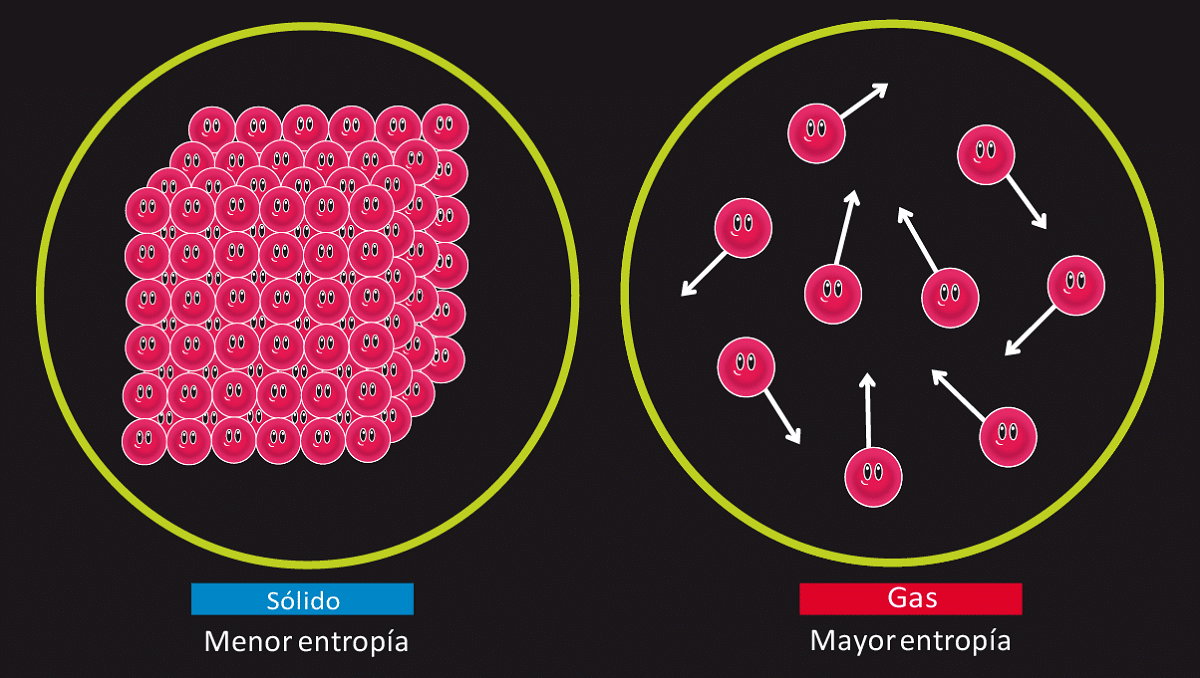
Lahko rečemo, da entalpija je enaka notranji energiji, ki jo ima sistem plus tlak, pomnožen s prostornino istega sistema. Ko vidimo, da so energija sistema, tlak in prostornina funkcije stanja, je tudi entalpija. To pomeni, da se lahko, ko pride čas, pojavi v določenih končnih začetnih pogojih, tako da lahko spremenljivka pomaga pri preučevanju celotnega sistema.
Prva stvar je vedeti, kaj je entalpija tvorbe. To je približno absorbirana toplota, ki jo sistem pozabi, ko iz elementov v normalnem stanju nastane 1 mol snovi izdelka. Ta stanja so lahko trdna, tekoča ali plinasta ali v primeru raztopine. Alotropno stanje je najbolj stabilno stanje. Na primer, najbolj stabilno alotropno stanje ogljika je grafit, poleg tega pa je v normalnih pogojih, kjer so vrednosti depresije 1 ozračje in temperatura je 25 stopinj.
Poudarjamo, da entalpije tvorbe v skladu z opredelitvijo veljajo za 1 mol proizvedene spojine. Na ta način bo treba reakcijo prilagoditi z delnimi koeficienti, odvisno od količine obstoječih reagenskih produktov.
Entalpija tvorbe

Vemo, da je v vsakem kemičnem procesu entalpija tvorbe lahko pozitivna in negativna. Ta entalpija je pozitivna, kadar je reakcija endotermna. Da je kemična reakcija endotermna, pomeni, da lahko absorbira toploto medija. Po drugi strani, imamo negativno entalpijo, kadar je reakcija eksotermna. Da je kemična reakcija eksotermna, pomeni, da oddaja toploto iz sistema navzven.
Da lahko pride do eksotermne reakcije, morajo imeti reaktanti večjo energijo kot produkti. Nasprotno, za reakcijo endoterme morajo imeti reaktanti manj energije kot produkti. Da bi lahko kemijsko enačbo vsega tega dobro napisali, je treba upoštevati zakon o ohranjanju snovi. To pomeni, da mora kemijska enačba vsebovati informacije o agregatnem stanju reaktantov in produktov. To je znano kot agregacijsko stanje
Upoštevajte tudi to čiste snovi imajo entalpijo tvorbe, ki je enaka nič. Te vrednosti entalpije se dobijo v standardnih pogojih, kot so zgoraj omenjeni, in v njihovi najbolj stabilni obliki. V kemičnem sistemu, kjer so reaktanti in produkti, je entalpija reakcije enaka entalpiji tvorbe v standardnih pogojih.
Vemo, da se entalpija tvorbenih vrednosti nekaterih anorganskih in organskih kemičnih spojin določi v pogojih 1 atmosfere tlaka in 25 stopinj temperature.
Entalpija reakcije
Omenili smo že, kaj je entalpija tvorbe. Zdaj bomo opisali, kaj je entalpija reakcije. To je termodinamična funkcija, ki pomaga izračunajte toploto, ki je bila pridobljena ali toplota, ki je bila oddana med kemično reakcijo. Išče se tehtnica, ostane ali prejme reagente in izdelke. Eden od vidikov, ki jih je treba izpolniti za izračun entalpije reakcije, je, da mora reakcija sama potekati pri stalnem tlaku. Se pravi, ves čas, ko traja kemična reakcija, mora biti tlak konstanten.
Vemo, da ima entalpija dimenzije energije, zato jo merimo v džulih. Da bi razumeli odnos entalpije do toplote, ki se izmenjuje med kemijsko reakcijo treba je iti do prvega termodinamičnega zakona. In to je, da nam ta prvi zakon pravi, da je toplota, ki se izmenjuje v termodinamičnem procesu, enaka spremembi notranje energije snovi ali snovi, ki sodelujejo v procesu, in dela, ki ga te snovi opravijo med postopkom.
Vemo, da vse kemijske reakcije niso nič drugega kot različni termodinamični procesi, ki potekajo pod določenim tlakom. Najpogostejše vrednosti tlaka so podane v standardnih pogojih atmosferskega tlaka. Zato se vsi termodinamični procesi, ki se pojavljajo na ta način, imenujejo izobarični, saj se pojavljajo pri stalnem tlaku.
Zelo pogosto imenujemo entalpijska toplota. Jasno pa mora biti, da ni isto kot toplota, ampak izmenjava toplote. To pomeni, da ni toplota tista, ki lahko nauči lekcijo, ali notranja toplota, ki jo imajo reaktanti in proizvodi. Toplota se med celotnim postopkom kemijske reakcije izmenjuje.
Odnos s toploto
Za razliko od tega, o čemer smo že govorili, je entalpija državna funkcija. Ko izračunamo spremembo entalpije, dejansko izračunamo razliko dveh funkcij. Te funkcije so običajno odvisne izključno od stanja sistema. To stanje sistema se razlikuje glede na notranjo energijo in prostornino samega sistema. Ker vemo, da je različica ves čas kemične reakcije nespremenjena, entalpija reakcije ni nič drugega kot funkcija stanja, ki je odvisna tako od notranje energije kot od volumna.
Zato lahko entalpijo reaktantov v kemijski reakciji določimo kot vsoto vsakega od njih. Po drugi strani določimo isto stvar, vendar v izdelkih, kot vsoto entalpije vseh izdelkov.
Upam, da boste s temi informacijami izvedeli več o entalpiji in njenih značilnostih.
