W świecie fizyki istnieje gałąź, która jest odpowiedzialna za badanie przemian wywoływanych przez ciepło i pracę w systemie. Chodzi o termodynamika. Jest to dziedzina fizyki odpowiedzialna za badanie wszystkich przemian, które są jedynie wynikiem procesów obejmujących zmiany zmiennych stanu zarówno temperatury, jak i energii na poziomie makroskopowym.
W tym artykule powiemy Ci wszystko, co musisz wiedzieć o termodynamice i zasadach termodynamiki.
Główne cechy
Jeśli przeanalizujemy klasyczną termodynamikę, zobaczymy, że opiera się ona na koncepcji układu makroskopowego. Ten system to nic innego jak część fizycznej lub konceptualnej masy oddzielonej od środowiska zewnętrznego. Aby lepiej badać układy termodynamiczne zawsze przyjmuje się, że jest to masa fizyczna, która nie jest zakłócana wymianą energii z ekosystemem zewnętrznym.
Stan układu makroskopowego, jaki jest w warunkach równowagi określają ją wielkości zwane zmiennymi termodynamicznymi. Wszystkie te zmienne są nam znane i są to temperatura, ciśnienie, objętość i skład chemiczny. Wszystkie te zmienne definiują systemy i ich równowagę. Główne zapisy termodynamiki chemicznej zostały ustalone dzięki stosowanej unii międzynarodowej. Dzięki tym jednostkom można lepiej zrozumieć i wyjaśnić prawo termodynamiki.
Istnieje jednak gałąź termodynamiki, która nie bada równowagi, ale jest odpowiedzialna za analizę procesów termodynamicznych, które charakteryzują się głównie brak zdolności do stabilnego osiągania warunków równowagi.
prawa
Zasady zostały potępione w XIX wieku Isa tych, którzy Odpowiadają za regulację wszystkich przemian i ich postępów. Analizują również, jakie są rzeczywiste ograniczenia, aby mieć prawdziwą koncepcję. Są to aksjomaty, których nie można udowodnić, ale nie da się ich udowodnić na podstawie doświadczenia. Każda teoria termodynamiki opiera się na tych zasadach. Możemy wyróżnić 3 podstawowe zasady plus zasadę, ale to jest ta, która definiuje temperaturę i jest zawarta w pozostałych 3 zasadach.
Zero prawa
Opiszemy, czym jest to prawo zerowe, które jako pierwsze opisuje temperaturę zawartą w pozostałych zasadach. Kiedy dwa systemy oddziałują ze sobą i znajdują się w równowadze termicznej, mają pewne wspólne właściwości. Te wspólne właściwości można zmierzyć i nadać im wartość liczbową. W rezultacie, jeśli oba układy są w równowadze z trzecim, będą w równowadze między sobą, a wspólną właściwością jest temperatura.
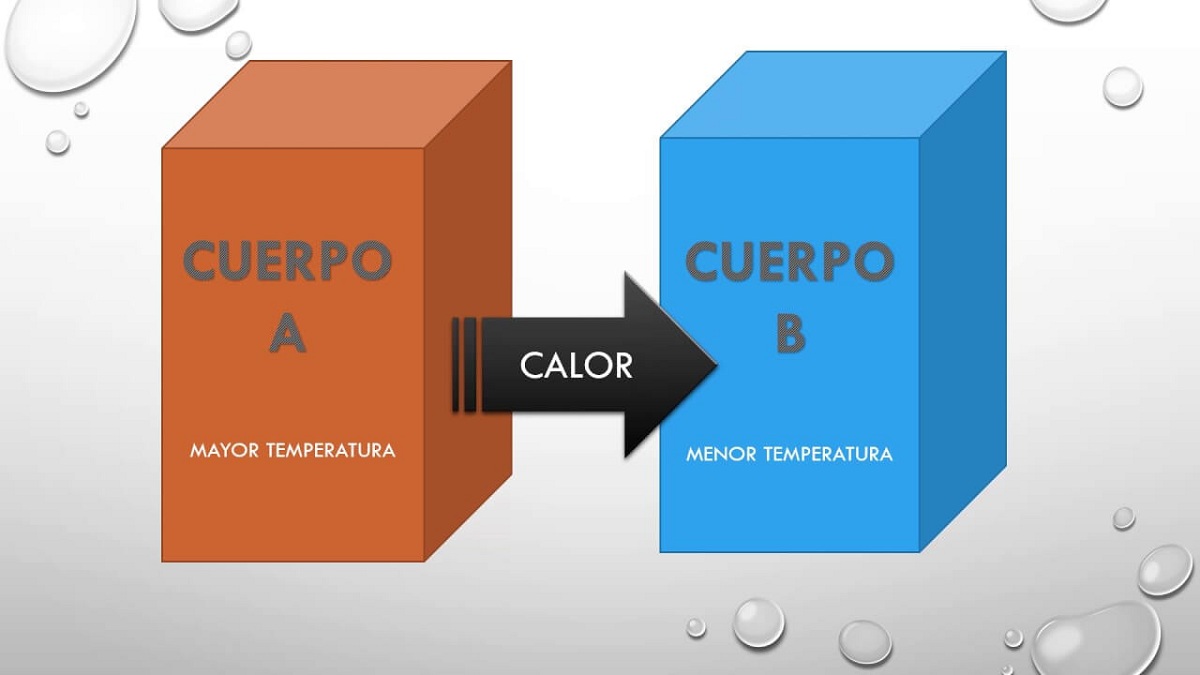
Dlatego ta zasada, ale po prostu stwierdza, że jeśli ciało A było w równowadze z ciałem B i to ciało B będzie w równowadze termicznej z ciałem C, wtedy ciała A i C również będą w równowadze termiczny. Zasada ta wyjaśnia fakt, że dwa ciała w różnych temperaturach mogą wymieniać ze sobą ciepło. Wcześniej czy później oba ciała osiągają tę samą temperaturę, więc są w całkowitej równowadze.
Pierwsza zasada termodynamiki
Kiedy dochodzi do kontaktu ciała z ciałem, które jest zimniejsze, następuje przemiana, która prowadzi do stanu równowagi. Ten stan równowagi opiera się na fakcie, że temperatury obu ciał są równe, ponieważ transfer energii jest wzmocniony między gorącym ciałem a zimnym ciałem. Aby wyjaśnić to zjawisko, naukowcy założyli, że gorąca substancja obecna w większych ilościach przechodzi przez zimniejsze ciało. Pomyślano o płynie, który mógłby przepływać przez masę, aby móc wymieniać ciepło.
Zasada ta jest odpowiedzialna za identyfikację ciepła jako formy energii. Nie jest to substancja materialna. W ten sposób można wykazać, że ciepło mierzone w kaloriach i praca w dżulach są równoważne. Dlatego dziś to wiemy 1 kaloria to około 4,186 dżuli.
Można powiedzieć, że pierwszą zasadą termodynamiki jest zasada zachowania energii. Ilość energii w silniku cieplnym jest zamieniana na pracę i może być zauważona przez każdą maszynę, która może wykonać taką pracę bez zużywania energii. Możemy przyjąć tę pierwszą zasadę jako: zmiana energii wewnętrznej zamkniętego układu termodynamicznego jest równa różnicy istniejącej między ciepłem dostarczonym do układu a pracą wykonywaną przez ten układ w środowisku.
Druga zasada termodynamiki
To na wstępie stwierdza, że niemożliwe jest wykonanie cyklicznej maszyny, która skutkuje jedynie przeniesieniem ciepła z ciała zimnego do ciała ciepłego. Można powiedzieć, że niemożliwe jest przeprowadzenie transformacji, której wynikiem będzie tylko chodzi o zamianę ciepła, które pobieramy z jednego źródła w pracę mechaniczną.
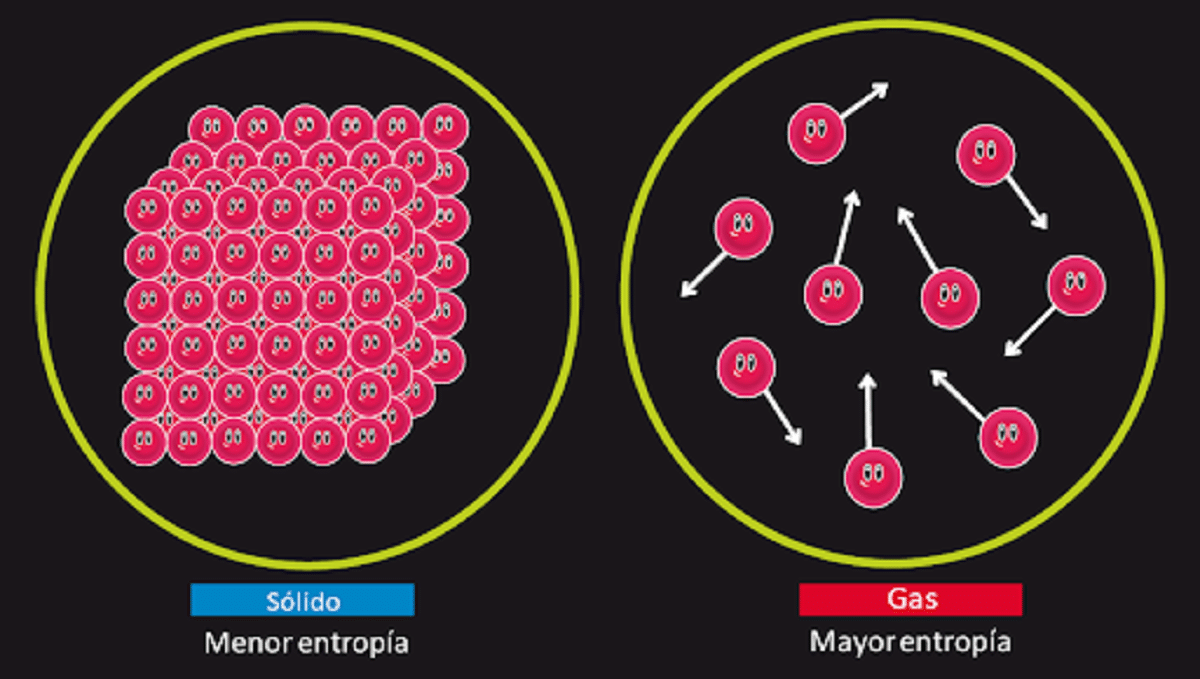
Zasada ta odpowiada za zaprzeczanie możliwości istnienia znanego wiecznego ruchu drugiego gatunku. Wiemy, że entropia systemu pozostaje niezmieniony, gdy zachodzi odwracalna transformacja. Wiemy również, że wzrasta, gdy następuje nieodwracalna przemiana.
Trzecia zasada termodynamiki
Ta ostatnia zasada jest ściśle związana z drugą i jest uważana za jej konsekwencję. Zasada ta potwierdza, że bytu absolutnego nie można osiągnąć w kolorze przy skończonej liczbie przekształceń. Wiemy, że istnieje zero absolutne, to nie więcej niż minimalna temperatura, jaką można osiągnąć. W jednostkach Kelwin wiemy, że jest to 0, ale w stopniach Celsjusza ma wartość -273.15 stopnia.
Stwierdza również, że entropia dla ciała stałego, które jest doskonale krystaliczne o temperaturze 0 kelwinów, jest równa 0. Oznacza to, że nie byłoby entropii, więc układ byłby całkowicie stabilny. Energia wyzwolenia, translacji i rotacji cząstek, które go tworzą, byłaby niczym w temperaturze 0 kelwinów.
Mam nadzieję, że dzięki tym informacjom możesz dowiedzieć się więcej o termodynamice i podstawowych zasadach.