
Po znajomości Model atomowy Thomsona, który uważał, że elektrony znajdują się w dodatnio naładowanym ośrodku, bardziej zaawansowany model znany jako Model atomowy Rutherforda. Naukowcem odpowiedzialnym za ten nowy przełom w nauce był Ernest Rutherford. Urodził się 20 sierpnia 1871 r., zmarł 19 października 1937 r. W swoim życiu wniósł wielki wkład w chemię i świat nauki w ogóle.
Dlatego poświęcimy ten artykuł, aby powiedzieć ci wszystko, co musisz wiedzieć o modelu atomu Rutherforda.
Eksperyment ze złotym liściem
Stary model Thomsona mówił, że elektrony znajdują się w dodatnio naładowanym ośrodku. W roku 1909 Ernest Rutherford w towarzystwie dwóch asystentów, Geigera i Marsdena, przeprowadził badanie znane jako eksperyment Złotego Liścia, w którym byli w stanie zweryfikować, że Dobrze znany „budyń rodzynkowy” Thomsona był zły. Chodzi o to, że ten nowy eksperyment był w stanie wykazać, że atom ma strukturę o silnym ładunku dodatnim. Ten eksperyment nie mógł pomóc w przywróceniu pewnych wniosków, które ostatecznie zostały przedstawione jako model atomowy Rutherforda w 1911 roku.
Eksperyment znany jako Złoty Liść nie był wyjątkowy, ale został przeprowadzony w latach 1909-1913. W tym celu wykorzystali laboratoria fizyczne Uniwersytetu w Manchesterze. Eksperymenty te miały ogromne znaczenie, ponieważ na podstawie ich wyników można było wyciągnąć nowe wnioski, które doprowadziły do rewolucyjnego modelu atomu.
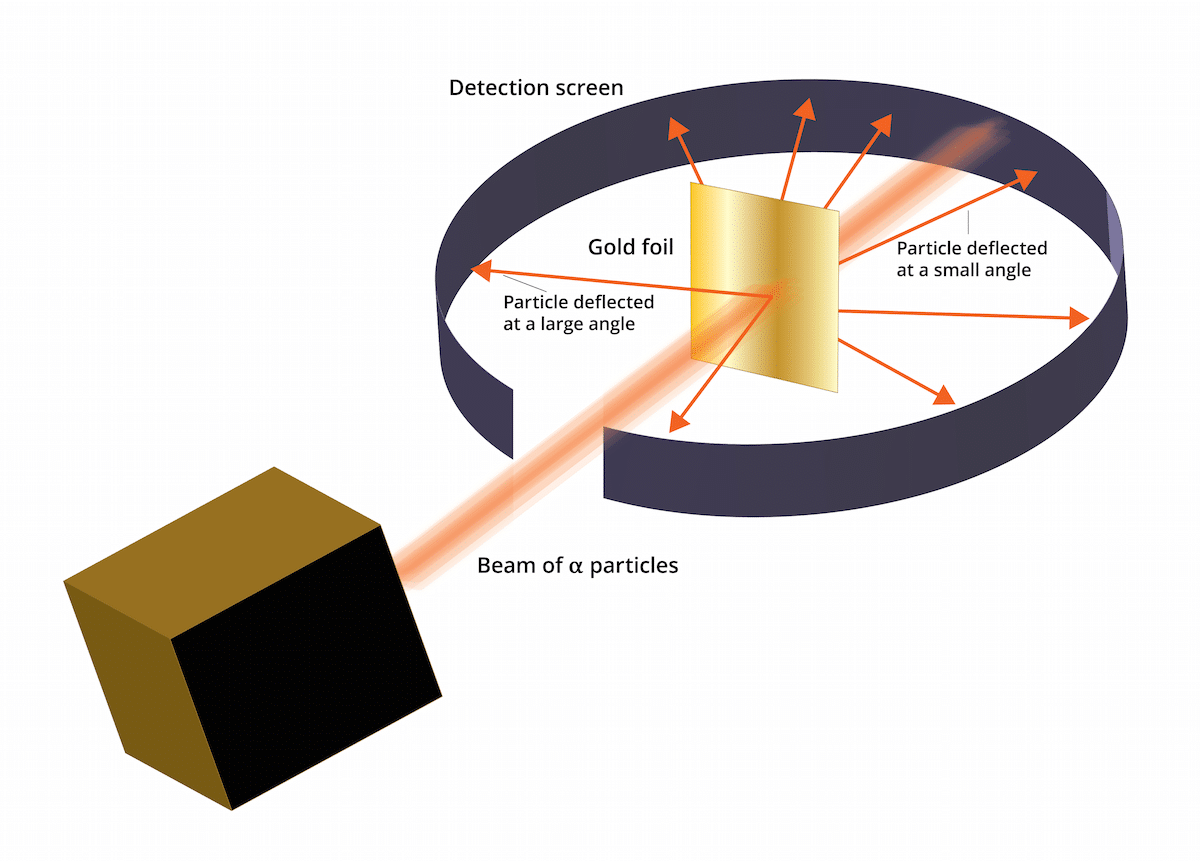
Ten eksperyment składał się z następujących elementów: cienki arkusz złota o grubości zaledwie 100 nm musiał zostać zbombardowany dużą ilością cząstek alfa. Te cząstki alfa były i jony. Oznacza to, że atomy nie mają elektronów, więc miały tylko protony i neutrony. Posiadając neutrony i protony, całkowity ładunek atomu był dodatni. Ten eksperyment miał głównie na celu potwierdzenie poprawności modelu Thomsona. Jeśli ten model był właściwy, cząsteczki alfa musiały przejść przez atomy złota w linii prostej.
Aby zbadać ugięcie spowodowane przez cząstki alfa, wokół cienkiej złotej folii trzeba było umieścić filtr fluorescencyjny z siarczku cynku. Wynikiem tego eksperymentu było to, że można było zaobserwować, że niektóre cząstki były w stanie przechodzić przez atomy złota w arkuszu w linii prostej. Jednak niektóre z tych cząstek alfa zostały odchylone w losowych kierunkach.
Wnioski z eksperymentu Gold Leaf

Biorąc pod uwagę ten fakt, nie było możliwe potwierdzenie tego, co uważa się za poprzednie modele atomowe. Chodzi o to, że te modele atomowe wskazywały, że ładunek dodatni był równomiernie rozłożony w atomach, co ułatwiłoby jego przekroczenie, ponieważ ładunek nie byłby tak silny w pewnym punkcie.
Wyniki tego eksperymentu ze Złotym Liściem były zupełnie nieoczekiwane. To sprawiło, że Rutherford pomyślał, że atom ma centrum z silnym ładunkiem dodatnim, który powoduje, gdy cząstka alfa spróbuj przekazać to odrzucone przez centralną strukturę. Aby ustalić bardziej wiarygodne źródło, cząstki zostały uwzględnione w ilościach tych, które zostały odbite, i tych, które nie zostały odbite. Dzięki takiemu doborowi cząstek możliwe było wyznaczenie wielkości jądra w stosunku do orbity otaczających je elektronów. Można również stwierdzić, że większość przestrzeni atomu jest pusta.
Widać było, że niektóre cząsteczki alfa zostały odbite przez złotą folię. Niektóre z nich odchylały się tylko pod bardzo małymi kątami. Pomogło to wywnioskować, że ładunek dodatni w atomie nie jest równomiernie rozłożony. Oznacza to, że ładunek dodatni znajduje się w atomie w sposób skoncentrowany w bardzo małej objętości przestrzeni.
Bardzo niewiele cząstek alfa odpłynęło z powrotem. To odchylenie wskazuje, jak następuje, wspomniane cząstki mogły się odbić. Dzięki tym wszystkim nowym rozważaniom model atomowy Rutherforda mógł zostać ustalony z nowymi pomysłami.
Model atomowy Rutherforda

Zbadamy, jakie są zasady modelu atomowego Rutherforda:
- Cząsteczki, które mają ładunek dodatni w atomie mają one bardzo małą objętość, jeśli porównamy ją z całkowitą objętością wspomnianego atomu.
- Prawie cała masa atomu znajduje się w wspomnianej małej objętości. Ta wewnętrzna masa została nazwana jądrem.
- Elektrony z ładunkami ujemnymi znajdują się obracając się wokół jądra.
- Elektrony obracają się z dużą prędkością, gdy znajdują się wokół jądra i robią to po kołowych torach. Te trajektorie nazywano orbitami. Później to zrobię są znane jako orbitale.
- Zarówno elektrony, które były naładowane ujemnie, jak i samo jądro dodatnio naładowanego atomu są zawsze utrzymywane razem dzięki elektrostatycznej sile przyciągania.
Akceptacja i ograniczenia modelu atomowego Rutherforda
Zgodnie z oczekiwaniami, ten nowy model ukazał zupełnie nową panoramę atomu w świecie naukowym. Dzięki temu modelowi atomowemu wielu późniejszych naukowców mogło badać i określać liczbę elektronów, jakie ma każdy element układu okresowego pierwiastków. Ponadto można by dokonać nowych odkryć, które pomogą wyjaśnić działanie atomu w najprostszy sposób.
Jednak ten model ma również pewne ograniczenia i błędy. Chociaż oznaczały one wielki postęp w świecie fizyki, nie były ani doskonałym, ani kompletnym modelem. I to jest z zgodnie z prawami Newtona i ważnym aspektem praw Maxwella, ten model nie mógł wyjaśnić pewnych rzeczy:
- Nie potrafił wyjaśnić, w jaki sposób ładunki ujemne były w stanie utrzymać się razem w jądrze. Według elektronicznej piszczeli, ładunki dodatnie muszą się odpychać.
- Kolejna sprzeczność dotyczyła podstawowych praw elektrodynamiki. Gdyby przyjąć, że dodatnio naładowane elektrony krążą wokół jądra, powinny emitować promieniowanie elektromagnetyczne. Emitując to promieniowanie, energia jest zużywana na dzień przed zapadnięciem się elektronów w jądro. Z tego powodu prążkowany model atomu nie może wyjaśnić stabilności, jaką ma atom.
Mam nadzieję, że dzięki tym informacjom dowiesz się więcej o modelu atomowym Rutherforda.