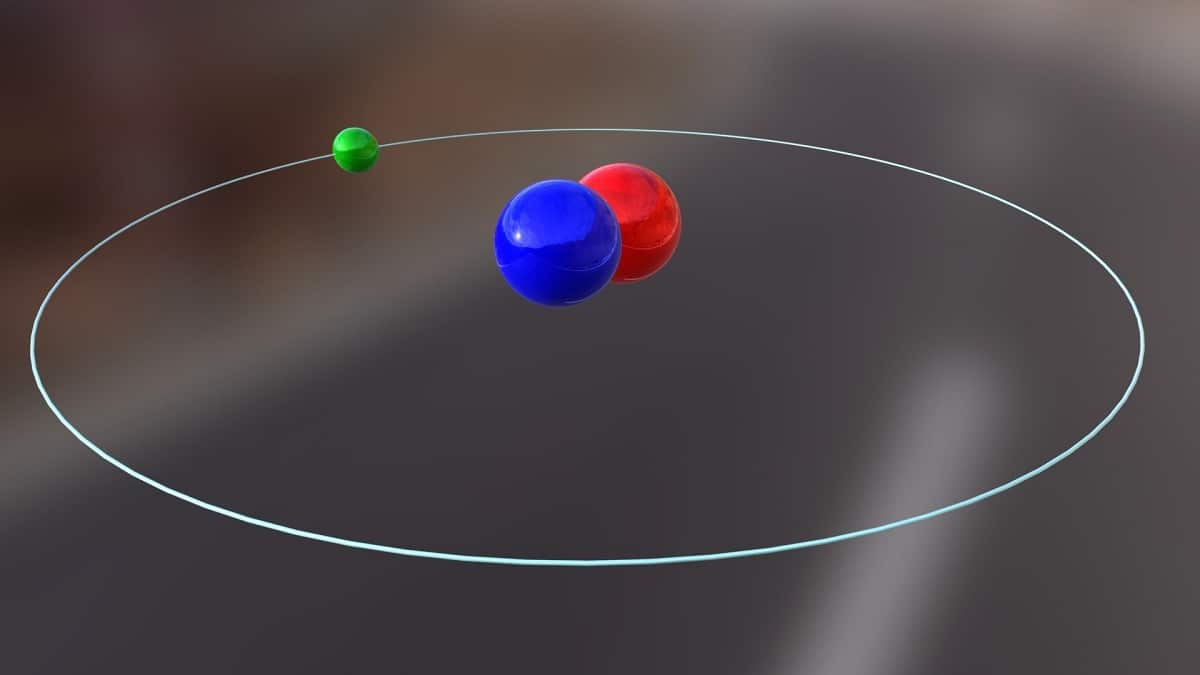
Dzisiaj porozmawiamy o izotopie używanym do produkcji energii jądrowej. To jest o deuter. Jest to jeden z rodzajów izotopów wodoru i jest reprezentowany przez symbol D lub 2H. Nadano mu potoczną nazwę ciężki wodór, ponieważ jego masa jest dwukrotnie większa od masy protonu. Izotop to nic innego jak gatunek pochodzący z tego samego pierwiastka chemicznego, ale o innej liczbie masowej. Deuter jest używany do różnych celów.
Dlatego zamierzamy poświęcić ten artykuł, aby przedstawić wszystkie cechy, strukturę, właściwości i zastosowania deuteru.
Główne cechy
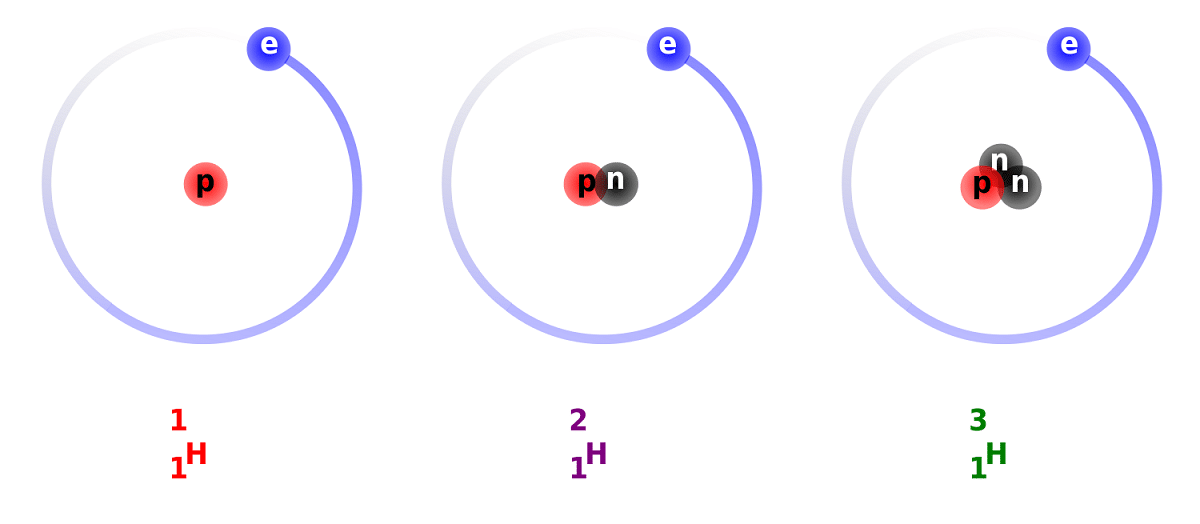
Różnica między deuterem a wodorem wynika z różnicy w liczbie neutronów, które ma. Z tego powodu deuter jest uważany za stabilny izotop i można go znaleźć w związkach utworzonych przez wodór o całkowicie naturalnym pochodzeniu. Należy wziąć pod uwagę, że choć są pochodzenia naturalnego, występują w niewielkiej proporcji. Biorąc pod uwagę jego właściwości podobne do zwykłego wodoru, może go w całości zastąpić w reakcjach, w których uczestniczy. W ten sposób można go przekształcić w równoważne substancje.
Z tego i innych powodów deuter ma wiele zastosowań w różnych dziedzinach nauki. Z biegiem lat stał się jednym z najważniejszych elementów badań i rozwoju technologii i informacji.
Główna struktura tego izotopu składa się z jądra zawierającego proton i neutron. Ma masę atomową około 2,014 gramów. Izotop ten został odkryty dzięki Haroldowi C. Ureyowi, chemikowi ze Stanów Zjednoczonych, oraz jego współpracownikom Ferdinandowi Brickwedde i George'owi Murphy'emu w 1931 roku. Przygotowania do spotkania z deuterem w stanie czystym po raz pierwszy z powodzeniem przeprowadzono w 1933 roku. Już w latach pięćdziesiątych XX wieku zaczęto stosować fazę stałą, która wykazywała dużą stabilność, zwaną deuterkiem litu. Substancja ta mogłaby zastąpić deuter i tryt w wielu reakcjach chemicznych.
Postęp w nauce następuje, gdy zostanie znaleziona substancja, która może ułatwić reakcje chemiczne prowadzące do powstania produktów. W tym sensie, jeśli zbadałeś obfitość tego izotopu, aby móc obserwować pewne rzeczy. Wiadomo było, że zawartość deuteru w wodzie zmienia się nieznacznie w zależności od obszaru, z którego pobierana jest próbka. Jest kilka badań spektroskopowych ustalili istnienie tego izotopu na innych planetach w naszej galaktyce. Może to mieć ogromne znaczenie w badaniu składu innych ciał niebieskich.
Struktura i pochodzenie deuteru

Dowiemy się kilku faktów na temat deuteru. Jak wspomnieliśmy wcześniej, główna różnica między izotopami wodoru polega na ich strukturze. Chodzi o to, że wodór, deuter i tryt mają różne ilości protonów i neutronów, więc mają różne właściwości chemiczne. Muszę również wziąć pod uwagę, że deuter, który znajduje się w innych ciałach gwiazdowych, jest eliminowany z większą prędkością niż jest początkowy. Jest to jeden z powodów, dla których tak trudno jest zbadać obecność deuteru w ciałach gwiazdowych.
Uważa się, że inne zjawiska przyrodnicze tworzą niewielką ilość deuteru, więc jego produkcja nadal cieszy się dużym zainteresowaniem. Z procentu, o którym wspominaliśmy wcześniej o obecności deuteru w przyrodzie, nie wynosi 0.02%. Seria badań naukowych ujawniła, że ogromna większość atomów, które zostały utworzone z deuteru, powstała naturalnie w eksplozji, która dała początek wszechświatowi znanemu jako Wielki Wybuch. To jeden z głównych powodów, dla których uważa się, że deuter występuje na dużych planetach, takich jak Jowisz.
Najczęstszym sposobem uzyskania tego izotopu w sposób naturalny jest połączenie ich z wodorem. Kiedy to się stanie, zostanie połączone w formę protium. Naukowcy są zainteresowani poznaniem związku ustalonego między proporcją deuter i wodór w różnych dziedzinach nauki. Jest szeroko badany w takich gałęziach nauki, jak astronomia czy klimatologia. W tych gałęziach ma kilka praktycznych możliwości poznania i zrozumienia wszechświata i naszej atmosfery.
Właściwości deuteru

Dowiemy się, jakie są główne właściwości tego izotopu wodoru. Przede wszystkim trzeba wiedzieć, czym jest izotop pozbawiony właściwości radioaktywnych. Oznacza to, że ma dość stabilny charakter. Może być stosowany do zastępowania wodoru w różnych reakcjach chemicznych. Mając w naturalny sposób dużą stabilność, zachowuje się inaczej niż zwykły wodór. Dzieje się tak we wszystkich reakcjach, które mają charakter biochemiczny. Przed podstawieniem trzeba wiedzieć, że choć można to osiągnąć poprzez wymianę wodoru na deuter w reakcjach chemicznych, to trzeba wiedzieć, że będą one zachowywały się inaczej.
Kiedy wymieniasz dwa atomy wodoru w wodzie, możesz otrzymać związek zwany ciężką wodą. Wodór obecny w oceanie w postaci deuteru w stosunku do protu stanowi tylko 0,016%. We wszechświecie izotop ten ma tendencję do szybszego topienia się, tworząc hel. Jeśli połączymy deuter z tlenem atomowym, zobaczymy, że staje się on gatunkiem toksycznym. Mimo to i właściwości chemiczne lub bardzo podobne do właściwości wodoru.
Inną właściwością tego izotopu jest to, że gdy atomy deuteru są poddawane procesowi syntezy jądrowej w wysokich temperaturach, mogą zostać uwolnione duże ilości energii. To exodus, który zbadaliście, aby móc wdrożyć syntezę jądrową naszej planety. Niektóre właściwości fizyczne, takie jak temperatura wrzenia, ciepło parowania, punkt potrójny i gęstość mają wielkości większe niż wodór.
Mam nadzieję, że dzięki tym informacjom możesz dowiedzieć się więcej o deuteru i jego właściwościach.