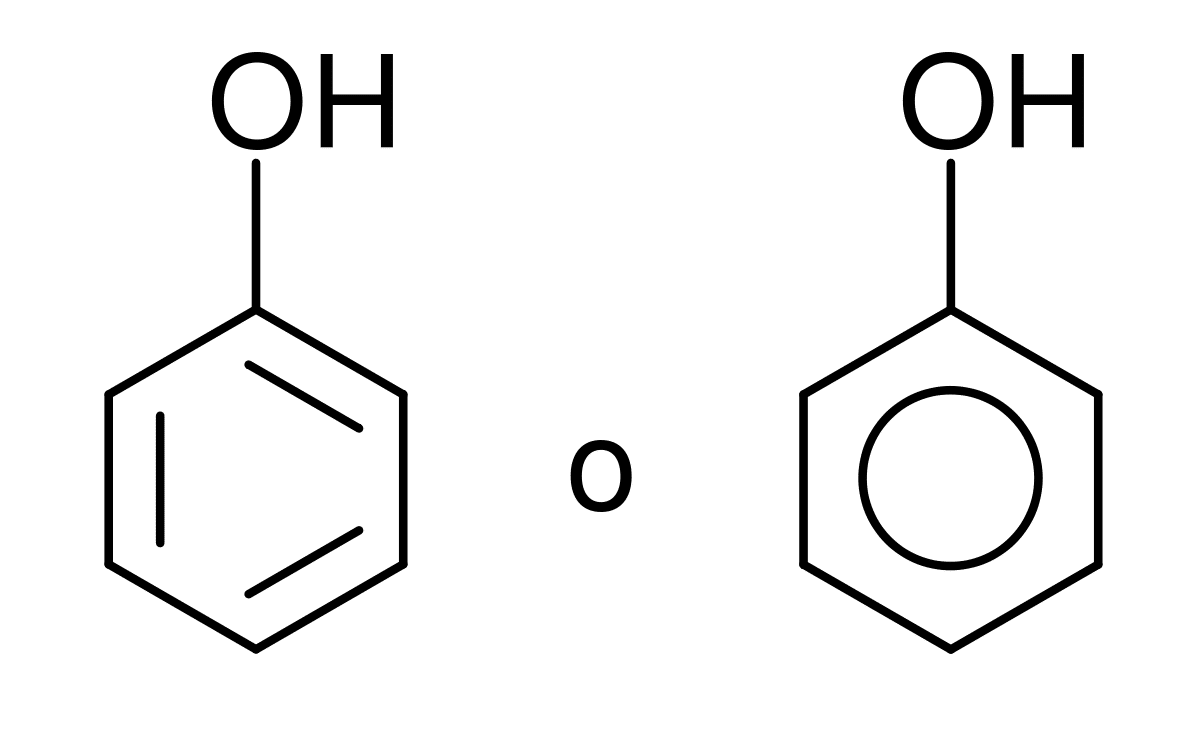
El grupo hydroxyl Het is degene die is samengesteld uit een zuurstofatoom en een waterstofatoom en lijkt op een watermolecuul. Het kan in verschillende chemische vormen worden gevonden, zoals in een groep, een ion of een radicaal. Voor al die mensen die organische chemie studeren, is het fundamenteel om de reacties en het belang van deze groep atomen te kennen. En het is in staat om essentiële bindingen te vormen met het koolstofatoom, hoewel het dat ook kan doen met zwavel en fosfor.
In dit artikel gaan we je vertellen over de kenmerken van de hydroxylgroep en het belang ervan in de organische chemie.
hoofdkenmerken
Wanneer we de hydroxylgroep analyseren vanuit het oogpunt van anorganische chemie, zien we dat het meer als een ion deelneemt. Met andere woorden, het type kant dat er tussen zit en de metalen is niet covalent, maar ionisch. Hierdoor is de hydroxylgroep een belangrijk element geworden dat helpt bij het definiëren van de eigenschappen en transformaties van veel verbindingen.
De hydroxylgroep is gebonden aan een groep die wordt gedefinieerd cmet de letter R als het alkyl is of met de letter Ar als het aromatisch is. Wat ik het meest weet over wetenschap, is wat de hydroxylgroep bijdraagt aan het molecuul waarin het zich bindt. Het beste antwoord wordt gevonden in de studie van zijn protonen. En is dat protonen kunnen worden weggerukt door sterke basen om zouten te vormen. Dit kan ook interageren met andere omringende groepen die met elkaar zijn verbonden door waterstofbruggen. Bovendien is het belangrijkste van de hydroxylgroep dat deze, waar deze zich ook bevindt, een potentieel gebied voor de vorming van water kan vertegenwoordigen.
Structuur van de hydroxylgroep

De hydroxylgroep is vanuit het oogpunt van organische chemie een behoorlijk interessant molecuul geworden. Het watermolecuul is hoekig van vorm en ziet eruit als een boemerang. Als we een van de uiteinden afsnijden, wat hetzelfde betekent als het verwijderen van een proton, verschillende situaties kunnen voorkomen. Het watermolecuul is omgezet in de hydroxylgroep of het hydroxylion. Beide hebben echter een moleculaire lineaire geometrie en zijn niet elektronisch.
Al deze bindingen zijn te wijten aan het feit dat ze gericht zijn op twee atomen om te allen tijde uitgelijnd te kunnen blijven. Hetzelfde is niet het geval met hybride orbitalen. De sleutel voor de hydroxylgroep om de verschillende moleculen met elkaar te laten mengen, heeft waterstofbruggen nodig. Deze waterstofbruggen zijn op zichzelf niet sterk, maar naarmate het aantal bronnen en het aantal hydroxylgroepen in een structuur toeneemt, vermenigvuldigen de effecten zich. Deze toename van het aantal waterstofbruggen wordt ook weerspiegeld in de fysische eigenschappen van de verbinding.
Waterstofbindingen vereisen dat de atomen tegenover elkaar staan. Er zijn enkele zuurstofatomen van een hydroxylgroep die zo gerangschikt moeten worden dat deze een rechte lijn kan genereren met de waterstof van een tweede groep. Dit is wat ingewikkelder, maar komt vaak voor. Op deze manier ontstaan vrij specifieke ruimtelijke ordeningen zoals wat gebeurt er binnen de structuur van het DNA-molecuul. Dit gebeurt tussen de stikstofbasen waaruit het DNA bestaat.
We kunnen het aantal hydroxylgroepen een structuur noemen die recht evenredig is met de affiniteit van water voor het molecuul. We gaan een voorbeeld geven om het beter te begrijpen. Hoewel suiker een hydrofobe koolstofstructuur heeft, omdat het een groot aantal hydroxylgroepen heeft, maakt het zeer oplosbaar in water.
Ionen en hun functies
De hydroxylgroep en het ion lijken erg op elkaar, maar hebben verschillende chemische eigenschappen. Het hydroxylion is een extreem sterke base en werkt door protonen op te vangen. Als we het forceren, kan het in water veranderen. En dit is een onvolledig watermolecuul dat negatief geladen is en een proton nodig heeft om te voltooien. Aan de andere kant, sinds de hydroxylgroep het heeft geen noodzaak om protonen te vangen om het te voltooien, gedraagt zich als een extreem zwakke basis. Het is in staat protonen te doneren, hoewel het dit alleen doet tegen basen die erg sterk zijn.
Positieve kernen zijn atomen in een molecuul die door hun elektronegatieve omgeving aan een elektronisch defect lijden.
Hydroxylgroep en meteorologie

We weten dat het werkt als een soort wasmiddel in de lucht dat andere gassen afbreekt. We weten dat de hydroxylgroep de belangrijkste controle heeft over de methaanconcentratie. Methaangas is een broeikasgas dat alleen in concentratie wordt overtroffen koolstofdioxide als bijdrage aan de opwarming van de aarde. Hoewel methaangas in mindere mate in de atmosfeer wordt aangetroffen, is het in staat om een grotere hoeveelheid warmte vast te houden dan kooldioxide.
Er is nieuw onderzoek onder leiding van een postdoctoraal onderzoeker van NASA dat heeft aangetoond dat hydroxylradicalen zichzelf recyclen zijn in staat om een constante atmosferische concentratie te handhaven. Deze concentratie blijft in de loop van de tijd behouden, zelfs als de methaanemissies toenemen. Daarom is het begrijpen van de rol van hydroxyl essentieel om de nuttige levensduur van methaan en de atmosfeer te begrijpen.
Wetenschappers hebben erop gewezen dat toenemende concentraties en emissies van methaangas ertoe kunnen leiden dat de hoeveelheid hydroxylradicalen wereldwijd uitgeput raakt. Op deze manier zou de nuttige levensduur van methaan worden verlengd, een probleem dat zou bijdragen aan de opwarming van de aarde. Door de levensduur van methaan te verlengen, zouden we niets hebben om de atmosfeer mee schoon te maken. De belangrijkste bronnen van hydroxyl en methaan en hoe ze reageren, zijn waargenomen. Recycling van deze groep vindt plaats nadat methaan is afgebroken en vervolgens wordt hervormd in aanwezigheid van andere gassen. Hydroxylconcentraties zijn vrij stabiel in de tijd. Ze hoeven niet per se te verdwijnen als het reageert met methaan.
Ik hoop dat je met deze informatie meer te weten kunt komen over de hydroxylgroep en al het belang ervan.