
भौतिकशास्त्र आणि रसायनशास्त्र या दोन्हीमध्ये शरीरात असलेली उर्जा मोजण्यासाठी एक संकल्पना वापरली जाते. आम्ही बोलत आहोत श्वास घेणे. हे मोजमाप करण्याचा एक प्रकार आहे जो शरीरात किंवा प्रणालीमध्ये असलेल्या उर्जेची मात्रा दर्शवितो ज्याची विशिष्ट मात्रा असते, त्यास दबावाखाली आणले जाते आणि त्या वातावरणासह देवाणघेवाण देखील होऊ शकते. सिस्टमची एन्थॅल्पी एच या पत्राद्वारे दर्शविली जाते आणि उर्जा मूल्ये दर्शविण्यासाठी त्याशी संबंधित भौतिक युनिट जूल आहे.
या लेखात आम्ही आपल्याला एंथलपीची सर्व वैशिष्ट्ये आणि महत्त्व सांगणार आहोत.
मुख्य वैशिष्ट्ये
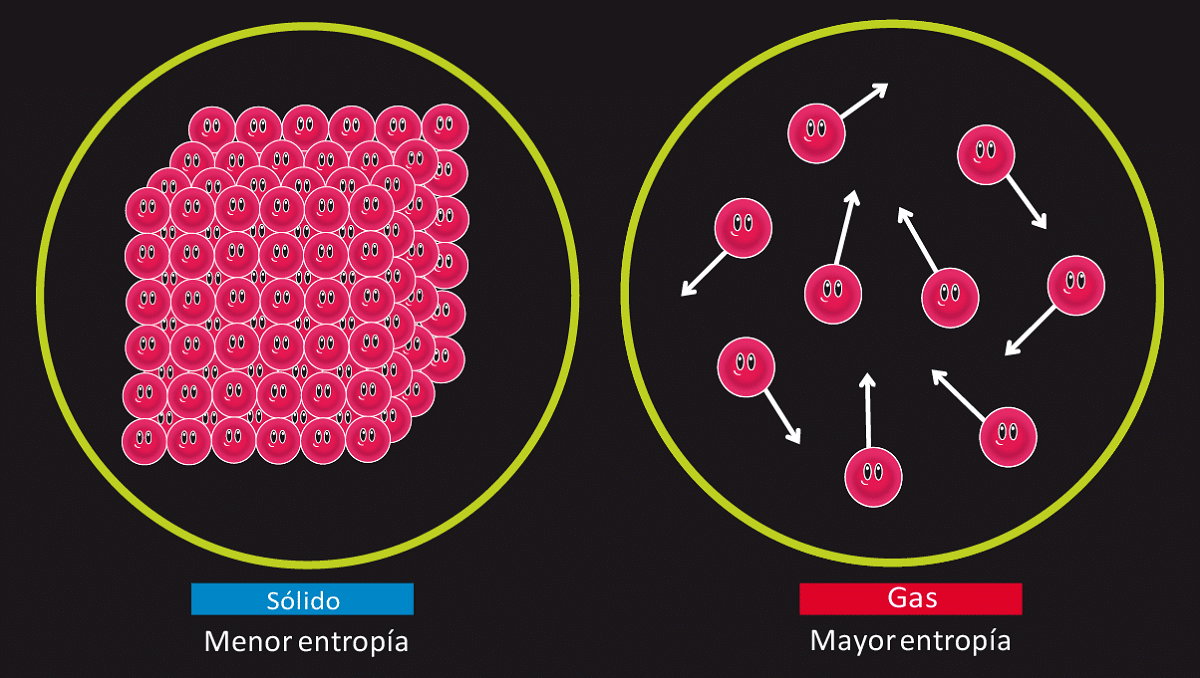
आम्ही म्हणू शकतो की एन्थॅल्पी सिस्टमची अंतर्गत उर्जा तितकीच असते आणि त्याच सिस्टमच्या व्हॉल्यूमच्या दाबाच्या वेळा. जेव्हा आपण पाहतो की यंत्रणेची उर्जा, दबाव आणि व्हॉल्यूम ही राज्याची कार्ये असतात तेव्हा एन्थॅल्पी देखील होते. याचा अर्थ असा की जेव्हा वेळ येईल तेव्हा ती विशिष्ट अंतिम प्रारंभिक परिस्थितीत उद्भवू शकते जेणेकरुन चल संपूर्ण प्रणालीचा अभ्यास करण्यास मदत करू शकेल.
पहिली गोष्ट म्हणजे रचनेची एन्थलपी म्हणजे काय ते जाणून घेणे. याबद्दल जेव्हा उत्पादनामध्ये 1 तीळ सामान्य स्थितीतील घटकांमधून तयार होते तेव्हा प्रणालीद्वारे विसरलेली उष्णता शोषली जाते. ही राज्ये घन, द्रव किंवा वायूयुक्त किंवा समाधानाच्या बाबतीत असू शकतात. Otलोट्रॉपिक राज्य सर्वात स्थिर राज्य आहे. उदाहरणार्थ, कार्बनची सर्वात स्थिर otलोट्रॉपिक अवस्था म्हणजे नैराश्य मूल्ये असलेल्या सामान्य परिस्थितीत व्यतिरिक्त ग्रेफाइट 1 वातावरण आणि तपमान 25 अंश आहे.
आम्ही यावर जोर देतो की आम्ही जे परिभाषित केले आहे त्यानुसार निर्मितीच्या ओहोटी उत्पादित कंपाऊंडच्या 1 तीळसाठी आहेत. अशाप्रकारे, विद्यमान रीएजेंट उत्पादनांच्या प्रमाणावर अवलंबून, प्रतिक्रिया भिन्नांश गुणांकांसह समायोजित करावी लागेल.
स्थापना एन्थॅल्पी

आम्हाला माहित आहे की कोणत्याही रासायनिक प्रक्रियेत, निर्मितीची मुदतवाढ सकारात्मक आणि नकारात्मक दोन्ही असू शकते. जेव्हा प्रतिक्रिया एंडोथर्मिक असते तेव्हा ही एन्थॅल्पी सकारात्मक असते. एक रासायनिक प्रतिक्रिया एंडोथेरमिक आहे म्हणजे ती माध्यमांची उष्णता शोषू शकते. दुसरीकडे, जेव्हा प्रतिक्रिया एक्स्टॉर्मिक असते तेव्हा आमच्यात नकारात्मक एन्थॅल्पी असते. रासायनिक अभिक्रिया म्हणजे बाह्यत्व म्हणजे याचा अर्थ असा होतो की ही प्रणालीपासून बाहेरून उष्णता बाहेर टाकते.
एक्झोथर्मिक प्रतिक्रिया होण्यासाठी, अणुभट्ट्यांमध्ये उत्पादनांपेक्षा जास्त उर्जा असणे आवश्यक आहे. उलटपक्षी, एंडोथर्मिक प्रतिक्रिया घेण्यासाठी रिअॅक्टन्समध्ये उत्पादनांपेक्षा कमी उर्जा असणे आवश्यक आहे. जेणेकरून या सर्वांचे रासायनिक समीकरण चांगल्या प्रकारे लिहिले जाऊ शकते, पदार्थाच्या संवर्धनाच्या कायद्याचे पालन करणे आवश्यक आहे. म्हणजेच, रासायनिक समीकरणात रिअॅक्टंट्स आणि उत्पादनांच्या भौतिक स्थितीची माहिती असणे आवश्यक आहे. हे एकत्रीकरण राज्य म्हणून ओळखले जाते
आपल्याला ते देखील लक्षात ठेवणे आवश्यक आहे शुद्ध पदार्थ पदार्थ शून्याइतकी तयार होण्यास उत्सुक असतात. ही एन्थॅल्पी मूल्ये मानक परिस्थितीत प्राप्त केली आहेत, जसे की वर नमूद केलेली आणि त्यांच्या सर्वात स्थिर स्वरुपात. रासायनिक प्रणालीमध्ये जिथे रिअॅक्टंट्स आणि उत्पादने असतात, प्रतिक्रियेची इनफॅल्पी मानक परिस्थितीत तयार होण्याच्या एन्फॅल्पीइतकीच असते.
आम्हाला माहित आहे की काही अकार्बनिक आणि सेंद्रीय रासायनिक संयुगे तयार करण्याच्या मूल्यांचे द्वितीयक वातावरण 1 दबाव आणि 25 डिग्री तपमानाच्या परिस्थितीत स्थापित केले जाते.
प्रतिक्रियेची दमछाक
आम्ही निर्मितीचा मोह काय आहे हे आधीच नमूद केले आहे. आता आपण अभिप्रायाची एन्थलपी म्हणजे काय ते वर्णन करणार आहोत. हे एक थर्मोडायनामिक फंक्शन आहे ज्यास मदत करते प्राप्त झालेल्या उष्माची किंवा रासायनिक अभिक्रिया दरम्यान वितरित करण्यात आलेली उष्णता मोजा. ट्रेनर शिल्लक रीएजेन्ट्स आणि उत्पादने दोन्ही मिळवितात, राहतात किंवा प्राप्त करतात. प्रतिक्रियेच्या एन्थॅल्पीची गणना करण्यासाठी ज्या पैलू पूर्ण करणे आवश्यक आहे त्यापैकी एक म्हणजे प्रतिक्रिया स्वत: च सतत दबावात उद्भवली पाहिजे. दुसर्या शब्दांत, रासायनिक अभिक्रिया होण्यास लागणारा संपूर्ण वेळ, दबाव कायम ठेवणे आवश्यक आहे.
आम्हाला माहित आहे की एन्थॅल्पीला उर्जेचे परिमाण आहेत आणि म्हणूनच ते जूलमध्ये मोजले जाते. रासायनिक अभिक्रियेदरम्यान देवाणघेवाण होते त्या उष्माशी संबंध समजून घेण्यासाठी थर्मोडायनामिक्सच्या पहिल्या कायद्याकडे जाणे आवश्यक आहे. आणि हा पहिला कायदा आपल्याला सांगतो की थर्मोडायनामिक प्रक्रियेमध्ये ज्या उष्णतेची देवाणघेवाण केली जाते ती प्रक्रियेमध्ये समाविष्ट असलेल्या पदार्थ किंवा प्रक्रियेमध्ये समाविष्ट असलेल्या पदार्थांच्या अंतर्गत ऊर्जेच्या भिन्नतेसह तसेच प्रक्रियेदरम्यान पदार्थांद्वारे केलेल्या कार्याच्या समान असते.
आम्हाला माहित आहे की सर्व रासायनिक प्रतिक्रिया विशिष्ट थर्मोडायनामिक प्रक्रियेशिवाय काही नसतात जे एका विशिष्ट दाबावर उद्भवतात. सर्वात सामान्य दबाव मूल्ये वातावरणाच्या दाबांच्या मानक परिस्थितीत दिली जातात. म्हणूनच, अशा प्रकारे होणार्या सर्व थर्मोडायनामिक प्रक्रियेस आयसोबेरिक असे म्हणतात, कारण ते सतत दबावात उद्भवते.
एन्थेलपी उष्णता कॉल करणे खूप सामान्य आहे. तथापि, हे स्पष्ट केले पाहिजे की ते उष्णतेसारखेच नाही, परंतु उष्णता विनिमय आहे. म्हणजेच, ही एक उष्णता नाही जी धडा शिकवू शकते किंवा अणुभट्टी आणि उत्पादनांमधील अंतर्गत उष्णता. ही उष्णता आहे ज्याची संपूर्ण रासायनिक प्रतिक्रिया प्रक्रियेमध्ये देवाणघेवाण होते.
उष्णतेशी संबंध
आम्ही यापूर्वी ज्या गोष्टी बोललो त्यापेक्षा एन्थॅल्पी हे एक राज्य कार्य आहे. जेव्हा आपण एन्थॅल्पी बदलांची गणना करतो तेव्हा आपण दोन फंक्शन्समधील फरक मोजत आहोत. ही कार्ये सामान्यत: सिस्टमच्या स्थितीवरच अवलंबून असतात. सिस्टमची ही स्थिती अंतर्गत उर्जा आणि सिस्टमच्या स्वतःच प्रमाणात अवलंबून असते. आम्हाला माहित आहे की संपूर्ण रासायनिक प्रतिक्रियेमध्ये ही आवृत्ती स्थिर राहते, प्रतिक्रियेची आतुरता ही राज्य उर्जा आणि व्हॉल्यूम या दोन्ही गोष्टींवर अवलंबून असते.
म्हणूनच, आम्ही रासायनिक अभिक्रियात रिअॅक्टंट्सची एन्थॅल्पी त्या प्रत्येकाची बेरीज म्हणून परिभाषित करू शकतो. दुसरीकडे, आम्ही तीच गोष्ट परिभाषित करतो परंतु उत्पादनांमध्ये सर्व उत्पादनांच्या एन्थलपीची बेरीज म्हणून.
मी आशा करतो की या माहितीसह आपण एन्थॅल्पी आणि त्याच्या वैशिष्ट्यांबद्दल अधिक जाणून घेऊ शकता.
