Grupė hidroksilas Tai yra tas, kuris susideda iš deguonies atomo ir vandenilio atomo ir primena vandens molekulę. Jis gali būti įvairių cheminių formų, tokių kaip grupė, jonas ar radikalas. Visiems žmonėms, kurie studijuoja organinę chemiją, būtina žinoti šios atomų grupės reakcijas ir svarbą. Jis sugeba užmegzti esminius ryšius su anglies atomu, nors tai gali padaryti ir su siera bei fosforu.
Šiame straipsnyje mes jums pasakysime apie hidroksilo grupės ypatybes ir jos svarbą organinėje chemijoje.
pagrindinės funkcijos
Kai analizuojame hidroksilo grupę neorganinės chemijos požiūriu, matome, kad ji daugiau dalyvauja kaip jonas. Kitaip tariant, nėrinių, esančių tarp jo ir metalų, tipas nėra kovalentinis, bet joninis. Dėl to hidroksilo grupė tapo svarbiu elementu, padedančiu apibrėžti daugelio junginių savybes ir transformacijas.
Hidroksilo grupė yra prijungta prie radikalo, kuris yra apibrėžtas csu raide R, jei ji yra alkilas, arba su raide Ar, jei ji yra aromatinė. Labiausiai apie mokslą žinau tai, kas hidroksilo grupę prisideda prie molekulės, kurioje jis jungiasi. Geriausias atsakymas yra jo protonų tyrimas. Ir tai yra tai, kad protonus gali pašalinti stiprios bazės, kad būtų galima suformuoti druskas. Tai taip pat gali sąveikauti su kitomis aplinkinėmis grupėmis, kurios yra sujungtos viena su kita vandenilio jungtimis. Be to, svarbiausia hidroksilo grupėje yra tai, kad, kad ir kur ji būtų, ji gali būti potencialus vandens susidarymo regionas.
Hidroksilo grupės struktūra

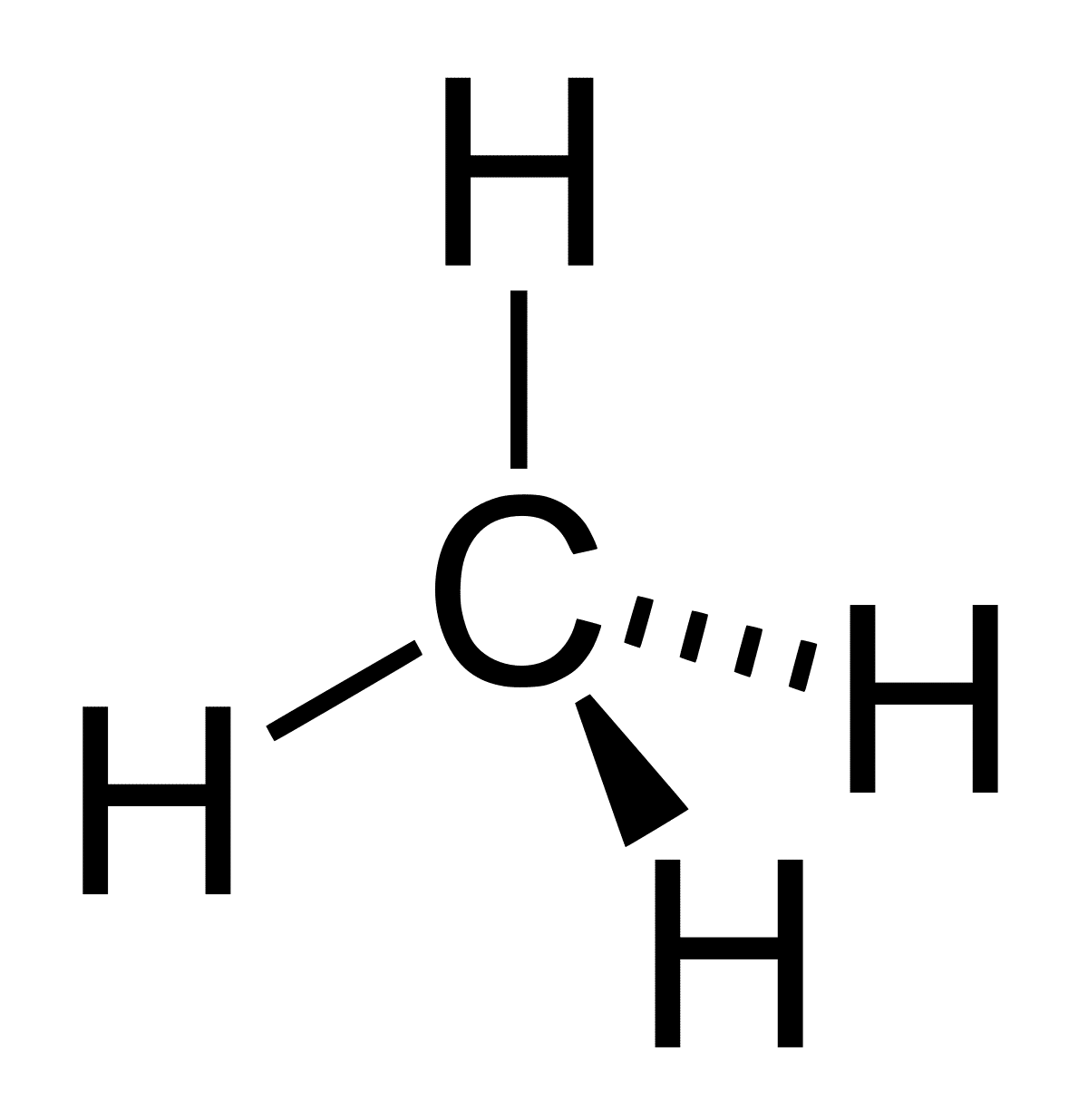
Organinės chemijos požiūriu hidroksilo grupė tapo gana įdomia molekule. Vandens molekulė yra kampinės formos ir atrodo kaip bumerangas. Jei nupjausime vieną iš jo galų, tai reiškia, kad pašalinsime protoną, gali pasitaikyti įvairių situacijų. Vandens molekulė yra virsta hidroksilo radikalu arba hidroksilo jonu. Tačiau abiejų molekulinė geometrija yra tiesinė ir nėra elektroninė.
Visos šios jungtys yra dėl to, kad jos yra orientuotos į du atomus, kad galėtų visada išlikti lygios. Panašiai nėra su hibridinėmis orbitomis. Hidroksilo grupės raktas, leidžiantis skirtingoms molekulėms maišytis tarpusavyje, turi vandenilio jungčių. Šios vandenilio jungtys savaime nėra stiprios, tačiau didėjant šaltinių ir hidroksilo grupių skaičiui struktūroje, poveikis daugėja. Šis vandenilio ryšių skaičiaus padidėjimas atsispindi ir junginio fizinėse savybėse.
Vandenilio jungtys reikalauja, kad atomai būtų vienas priešais kitą. Yra keletas vienos hidroksilo grupės deguonies atomų, kurie turi būti išdėstyti taip, kad galėtų generuoti tiesią liniją su antrosios grupės vandeniliu. Tai yra šiek tiek sudėtingiau, bet tai atsitinka dažnai. Tokiu būdu atsiranda gana specifiniai erdviniai išdėstymai, pvz kas vyksta DNR molekulės struktūroje. Tai atsitinka tarp azoto bazių, sudarančių DNR.
Hidroksilo grupių skaičių galime vadinti struktūra, tiesiogiai proporcinga vandens afinitetui molekulei. Pateiksime pavyzdį, kad geriau jį suprastume. Nors cukrus turi hidrofobinę anglies struktūrą, kadangi jame yra daug hidroksilo grupių, daro jį labai tirpų vandenyje.
Jonai ir jų funkcijos
Hidroksilo grupė ir jonas yra labai panašūs, tačiau turi skirtingas chemines savybes. Hidroksilo jonas yra ypač stipri bazė ir veikia sulaikydama protonus. Jei mes jį priverstume, jis gali virsti vandeniu. Tai yra neišsami vandens molekulė, kuri yra neigiamai įkrauta ir kuriai užbaigti reikia protono. Kita vertus, kadangi hidroksilo grupė jai nereikia užfiksuoti protonų, kad užbaigtų, jis elgiasi kaip itin silpna bazė. Jis sugeba paaukoti protonus, nors tai daro tik prieš labai stiprias bazes.
Teigiami branduoliai yra molekulės atomai, kurie dėl elektronegatyvios aplinkos kenčia nuo elektroninio trūkumo.
Hidroksilo grupė ir meteorologija

Mes žinome, kad jis veikia kaip ore esantis ploviklis, kuris skaido kitas dujas. Mes žinome, kad hidroksilo grupė yra pagrindinė metano koncentracijos kontrolė. Metano dujos yra šiltnamio efektą sukeliančios dujos, kurių koncentracija viršija tik anglies dioksido indėlį į visuotinį atšilimą. Nors metano dujų atmosferoje randama mažiau, jos sugeba išlaikyti didesnį šilumos kiekį nei anglies dioksidas.
Yra naujų tyrimų, vadovaujamų NASA doktorantų, kurie parodė, kad hidroksilo radikalai perdirbami patys ir sugeba palaikyti pastovią atmosferos koncentraciją. Ši koncentracija laikui bėgant išlieka, net jei metano emisija didėja. Todėl norint suprasti metano ir atmosferos naudingumą, būtina suprasti hidroksilo vaidmenį.
Mokslininkai atkreipė dėmesį, kad didėjančios metano dujų koncentracijos ir išmetimai gali sukelti hidroksilo radikalų kiekį visame pasaulyje. Tokiu būdu prailgėtų metano naudingo tarnavimo laikas, o tai dar labiau padidintų klimato atšilimą. Pailginę metano gyvenimo trukmę, neturėtume kuo valyti atmosferos. Buvo pastebėti pagrindiniai hidroksilo ir metano šaltiniai ir jų reakcija. Šios grupės perdirbimas įvyksta, kai metanas suyra, o po to vykdo reformas, esant kitoms dujoms. Hidroksilo koncentracija laikui bėgant yra gana stabili. Jie nebūtinai turėtų išnykti, kai jis reaguoja su metanu.
Tikiuosi, kad turėdami šią informaciją galite sužinoti daugiau apie hidroksilo grupę ir visą jos svarbą.