
Tiek fizikoje, tiek chemijoje sąvoka naudojama kūno energijai matuoti. Mes kalbame apie entalpija. Tai yra matavimo tipas, nurodantis energijos kiekį kūne ar sistemoje, kuris turi tam tikrą tūrį, yra veikiamas slėgio ir gali būti keičiamas su aplinka. Sistemos entalpija yra raidė H, o fizinis vienetas, susijęs su energijos vertėmis, yra Džaulė.
Šiame straipsnyje mes jums pasakysime apie visas entalpijos ypatybes ir svarbą.
pagrindinės funkcijos
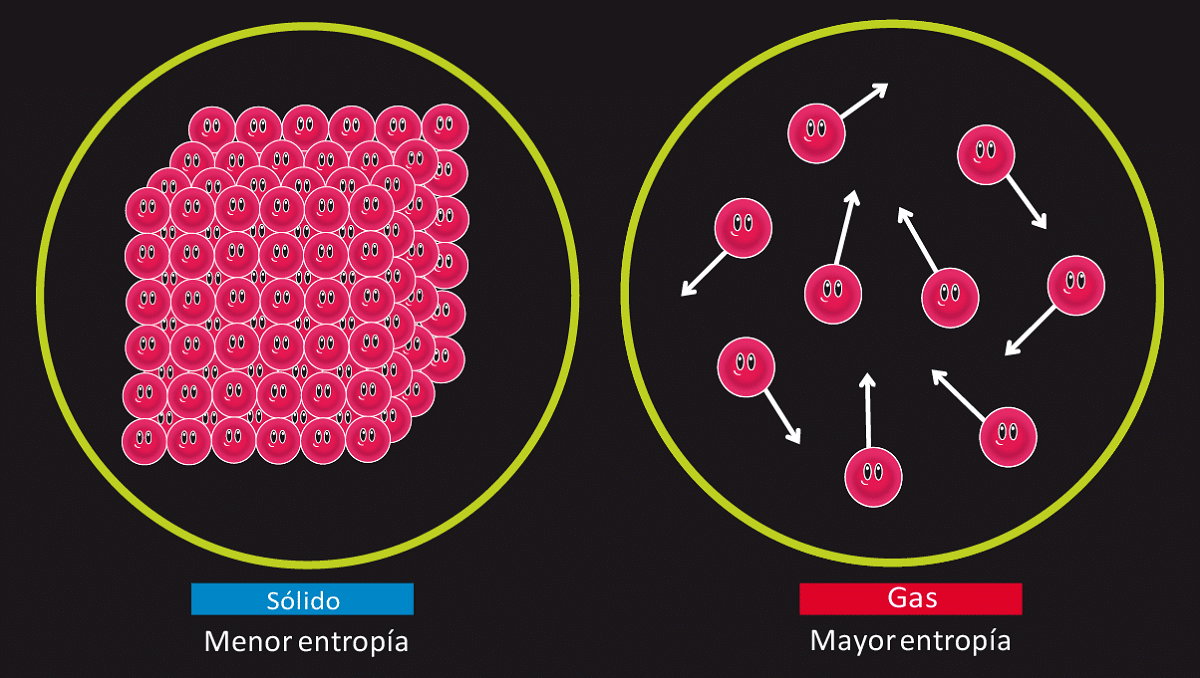
Galime sakyti, kad entalpija yra lygus vidinei energijai, kurią turi sistema, pridėjus slėgį, padaugintą iš tos pačios sistemos tūrio. Kai matome, kad sistemos energija, slėgis ir tūris yra būsenos funkcijos, entalpija taip pat yra. Tai reiškia, kad atėjus laikui, jis gali įvykti tam tikromis galutinėmis pradinėmis sąlygomis, kad kintamasis galėtų padėti ištirti visą sistemą kaip visumą.
Pirmiausia reikia žinoti, kas yra formavimosi entalpija. Tai apie absorbuota šiluma, kurią pamiršta sistema, kai iš normalios būsenos elementų susidaro 1 molis produkto medžiagos. Šios būsenos gali būti kietos, skystos, dujinės arba tirpalo atveju. Alotropinė būsena yra stabiliausia būsena. Pvz., Stabiliausia anglies alotropinė būsena yra grafitas, be to, esant normaliomis sąlygomis, kurių depresijos vertės yra 1 atmosfera ir temperatūra yra 25 laipsniai.
Mes pabrėžiame, kad susidarymo entalpijos pagal tai, ką mes apibrėžėme, yra 1 molis pagaminto junginio. Tokiu būdu, atsižvelgiant į esamų reagento produktų kiekį, reakciją reikės koreguoti taikant trupmeninius koeficientus.
Formacijos entalpija

Mes žinome, kad bet kuriame cheminiame procese formavimosi entalpija gali būti teigiama ir neigiama. Ši entalpija yra teigiama, kai reakcija yra endoterminė. Tai, kad cheminė reakcija yra endoterminė, reiškia, kad ji gali absorbuoti terpės šilumą. Iš kitos pusės, mes turime neigiamą entalpiją, kai reakcija yra egzoterminė. Tai, kad cheminė reakcija yra egzoterminė, reiškia, kad ji išskiria šilumą iš sistemos į išorę.
Kad įvyktų egzoterminė reakcija, reagentai turi turėti didesnę energiją nei produktai. Priešingai, norint įvykti endoterminę reakciją, reagentai turi turėti mažiau energijos nei produktai. Kad viso to cheminė lygtis būtų gerai parašyta, būtina laikytis materijos išsaugojimo dėsnio. Tai yra, cheminėje lygtyje turi būti informacija apie reagentų ir produktų fizinę būseną. Tai vadinama kaupimo būsena
Jūs taip pat turite nepamiršti to grynos medžiagos susidarymo entalpija lygi nuliui. Šios entalpijos vertės gaunamos standartinėmis sąlygomis, tokiomis kaip minėta aukščiau, ir jų stabiliausia forma. Cheminėje sistemoje, kur yra reagentų ir produktų, reakcijos entalpija yra lygi formavimo entalpijai standartinėmis sąlygomis.
Mes žinome, kad kai kurių neorganinių ir organinių cheminių junginių susidarymo entalpija nustatoma esant 1 atmosferos slėgiui ir 25 laipsnių temperatūrai.
Reakcijos entalpija
Mes jau minėjome, kas yra formavimosi entalpija. Dabar aprašysime, kokia yra reakcijos entalpija. Tai padeda termodinaminė funkcija apskaičiuokite gautą šilumą arba šilumą, kuri buvo suteikta cheminės reakcijos metu. Trenerio pusiausvyra ieškoma, lieka arba gauna tiek reagentus, tiek produktus. Vienas iš aspektų, kuris turi būti įvykdytas norint apskaičiuoti reakcijos entalpiją, yra tai, kad pati reakcija turi vykti esant pastoviam slėgiui. Tai yra, per visą laiką, kol praeina cheminė reakcija, slėgis turi būti palaikomas pastovus.
Mes žinome, kad entalpija turi energijos matmenis, todėl ji matuojama džauliais. Suprasti entalpijos santykį su šiluma, kuria keičiamasi cheminės reakcijos metu būtina pereiti prie pirmojo termodinamikos dėsnio. Ir tai yra tas, kad šis pirmasis dėsnis mums sako, kad šiluma, kuria keičiamasi termodinaminio proceso metu, yra lygi medžiagos ar medžiagų, dalyvaujančių procese, vidinės energijos kitimui, taip pat minėtų medžiagų proceso metu atliekamam darbui.
Mes žinome, kad visos cheminės reakcijos yra ne kas kita, kaip įvairūs termodinaminiai procesai, vykstantys esant tam tikram slėgiui. Dažniausios slėgio vertės pateikiamos standartinėmis atmosferos slėgio sąlygomis. Todėl visi tokiu būdu vykstantys termodinaminiai procesai vadinami izobariniais, nes jie vyksta esant pastoviam slėgiui.
Labai dažnai entalpijos vadinama šiluma. Tačiau turi būti aišku, kad tai ne tas pats, kas šiluma, o šilumos mainai. Tai reiškia, kad ne šiluma gali išmokti pamoką, nei vidinė šiluma, kurią turi reagentai ir produktai. Tai šiluma, kuri keičiama per visą cheminės reakcijos procesą.
Santykis su šiluma
Skirtingai nuo to, apie ką kalbėjome anksčiau, entalpija yra valstybės funkcija. Skaičiuodami entalpijos pokytį, mes iš tikrųjų apskaičiuojame dviejų funkcijų skirtumą. Šios funkcijos paprastai priklauso tik nuo sistemos būklės. Ši sistemos būsena skiriasi priklausomai nuo pačios sistemos vidinės energijos ir tūrio. Kadangi žinome, kad versija išlieka pastovi visos cheminės reakcijos metu, reakcijos entalpija yra ne kas kita, kaip būsenos funkcija, kuri priklauso ir nuo vidinės energijos, ir nuo tūrio.
Todėl cheminių reakcijų metu reaguojančių medžiagų entalpiją galime apibrėžti kaip kiekvieno iš jų sumą. Kita vertus, mes apibrėžiame tą patį dalyką, bet produktuose kaip visų produktų entalpijos sumą.
Tikiuosi, kad turėdami šią informaciją galite sužinoti daugiau apie entalpiją ir jos ypatybes.
