
화학적 변화는 물질의 화학적 구조를 변화시키는 물질의 변화입니다. 즉, 물질의 모양뿐만 아니라 특성도 변화시킵니다. 이것은 화학 반응 또는 화학 현상으로도 알려진 화학 변화가 하나의 물질 또는 화합물에서 화학 결합을 끊고 형성하여 새로운 물질 또는 화합물을 형성하는 것을 의미합니다. 수많은 화학적 변화 세계 요.
이러한 이유로, 우리는 이 기사를 존재하는 주요 화학적 변화와 그 예를 설명하는 데 바칠 것입니다.
화학적 변화란 무엇입니까?

두 개 이상의 물질(반응물 또는 반응물이라고 함)이 있을 때 화학 반응을 겪고 그 과정에서 화학 구조를 변경하고 소비할 수 있습니다. (흡열 반응) 또는 방출(발열 반응) 에너지, 두 개 이상의 물질(제품이라고 함)을 생성합니다. 일부 화학 반응은 독성 또는 부식성 화합물을 포함하거나 생성할 수 있기 때문에 인간에게 위험합니다. 특정 발열 반응과 같은 다른 반응은 폭발을 일으킬 수 있습니다.
화학 산업에서는 일상 생활에서 사용하는 많은 물질이 제어된 화학 반응을 통해 생산됩니다. 일부 반응은 자발적으로 발생하고 다른 반응은 공장이나 화학 실험실에서 인간이 생성해야 합니다. 화학 반응이 일어나려면 특정 시간이 걸립니다. 반응물의 특성과 반응이 일어나는 조건에 따라 다릅니다.
따라서 화학 반응 속도에 영향을 미치는 요인은 일반적으로 다음과 같습니다.
- 온도가 상승합니다. 온도의 증가는 화학 반응 속도를 증가시키는 경향이 있습니다.
- 압력 증가. 압력을 높이면 일반적으로 화학 반응 속도가 빨라집니다. 이것은 일반적으로 가스와 같이 압력 변화에 민감한 물질이 반응할 때 발생합니다. 액체와 고체의 경우 압력 변화는 반응 속도에 큰 변화를 일으키지 않습니다.
- 시약 응집 상태. 고체는 일반적으로 액체나 기체보다 더 느리게 반응하지만 속도는 각 물질의 반응성에 따라 달라집니다.
- 촉매 사용. 그들은 화학 반응의 속도를 높이는 데 사용되는 물질입니다. 이러한 물질은 반응을 방해하지 않으며 단지 반응이 일어나는 속도를 제어할 뿐입니다. 같은 방식으로 사용되지만 반대 효과가 있어 반응을 늦추는 억제제라는 물질도 있습니다.
- 빛 에너지. 일부 화학 반응은 빛이 비추면 속도가 빨라집니다.
- 시약 농도. 반응물의 농도가 높으면 대부분의 화학 반응이 더 빨리 일어납니다.
화학적 변화의 예
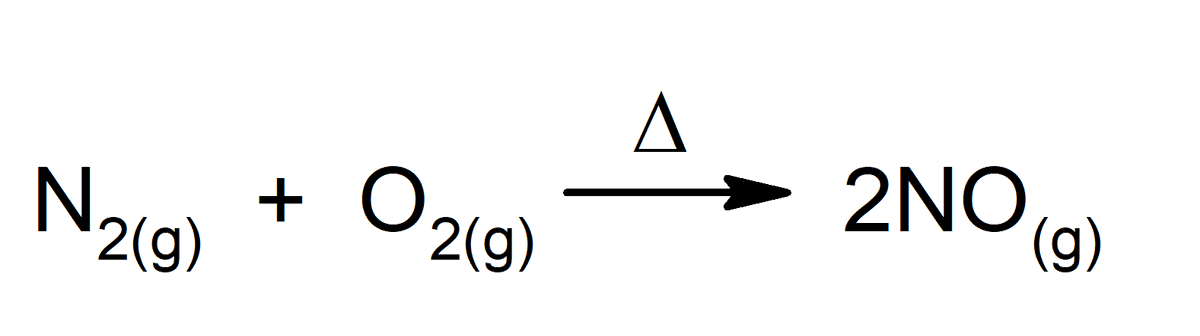
모든 화학 반응은 우리 몸 안에서 일어나는 화학 변화의 완벽한 예입니다. 몇 가지 예는 다음과 같습니다.
- 호흡. 이것은 화학적으로 변경된 생물학적 과정으로, 공기에서 산소를 가져와 음식에서 얻는 포도당과 반응하여 높은 수준의 화학 에너지(ATP)와 다량의 폐 이산화탄소(CO2)를 생성하는 데 사용됩니다. 배설.
- 산성비. 대기 오염이 심한 환경에서 발생합니다. 그것은 일반적으로 구름에 저장된 물과 공기 중에 분산된 다른 가스 사이의 화학적 변화의 결과이며, 이 가스의 황산화물 또는 질소 산화물 함량은 빗물과 함께 떨어지는 황산 또는 질산을 생성하여 염을 형성합니다. 배터리 내부에서 일어나는 반응은 산과 금속 사이에서 발생합니다. 예를 들어, 납과 황산을 사용하는 배터리는 백염인 황산납(II)을 생성합니다. 오존 분해. 오존 분자는 일종의 빛의 작용으로 산소 분자로 분해됩니다.
화학적 변화와 물리적 변화

물질의 물리적 변화는 그 구성을 바꾸지 않습니다. 즉, 물질의 화학적 구조를 바꾸지 않기 때문에 물리적 변화에 의해 물질이 분해되거나 형성될 수 없습니다. 물리적 변화는 단순히 모양, 밀도 및 응집 상태(고체, 액체, 기체)와 같은 물질의 물리적 특성을 변경합니다. 반면 신체적 변화는 일반적으로 물질의 모양이나 상태는 변경하지만 구성은 변경하지 않기 때문에 가역적입니다.
예를 들어, 물이 끓으면 액체가 기체로 변할 수 있지만 그 결과 발생하는 증기는 여전히 물 분자로 구성되어 있습니다. 반대로 물을 얼리면 고체가 되지만 화학적으로는 같은 물질입니다.
또 다른 예는 담배 라이터에 사용하는 액화 가스, 일반적으로 부탄(C4H10) 또는 프로판(C3H8)은 고압이 가해지면 액체가 되지만 화학적 조성은 변하지 않습니다.
화학적 변화는 물질 내 원자의 배열과 결합을 변경하여 다른 방식으로 결합하여 원래 물질과 다른 물질을 만듭니다. 화학적 변화가 일어날 때, 물질은 생성되거나 파괴될 수 없고 단지 변형될 수 있기 때문에 비율이 다르더라도 항상 처음에 사용했던 것과 동일한 양의 물질로 끝납니다.
예를 들어 물(H2O)과 칼륨(K)을 반응시키면 수산화칼륨(KOH)과 수소 기체(H2)라는 두 가지 새로운 물질이 생깁니다. 이것은 일반적으로 많은 에너지를 방출하는 반응이므로 매우 위험합니다.
물질의 화학적 변화의 예
베이킹 쿠키 또는 케이크
쿠키, 케이크, 컵케이크 등과 같은 일반적인 것들. 발효라고 하는 화학 반응을 숨깁니다. 효모에서 생성되는 가스로 인해 반죽이 부풀어 오릅니다.. 빵을 만들 때 효모는 전분을 포도당으로 변환합니다.
소화
음식의 소화는 가수분해(물의 작용에 의한 유기물의 분해)를 통한 물질의 화학적 변화의 명백한 예입니다. 과일, 야채, 육류 등 우리가 먹는 음식은 영양분을 더 잘 흡수하기 위해 위액과 섞이는 과정을 거친다. 유기체의 필요에 따라 다양한 물질로 변환합니다.
같은 과정에서 과도한 요소나 독소는 원래의 것과 다른 방식으로 유기체에서 제거됩니다. 대변, 소변, 땀 등의 형태로
풀케
발효는 포도당 분자가 산소 부족으로 분해되는 이화 과정입니다. 발효 과정을 통해 얻은 알코올 음료 중 일부는 사이다, 맥주 및 소프트 와인이며 후자는 세계에서 가장 덜 알려진 음료 중 하나입니다. Pulque는 장인의 공정을 통해 용설란 식물에서 얻습니다.l, 물질의 숙성이 어떤 입맛에도 맞지 않는 매우 특정한 풍미를 지닌 하얗고 시큼하며 점성이 있는 최종 제품을 얻는 데 핵심입니다.
발효는 빵, 요거트, 치즈 등을 만드는 동안에도 발생합니다.
Caramelo
캐러멜은 고체 백설탕이 몇 분 동안 가열되어 기분 좋은 향을 가진 호박색 점액으로 변하는 것과 같은 물질의 화학적 변화에 대한 기본적인 예입니다. 즉, 원본과 완전히 다른 제품이 생성됩니다.
이 정보를 통해 화학 변화와 그 예에 대해 더 많이 배울 수 있기를 바랍니다.