
원자는 물질의 기본 단위이며 화학 원소를 식별할 수 있는 가장 작은 부분입니다. 그것은 중성자와 양성자를 포함하는 원자핵과 핵을 둘러싼 전자로 구성됩니다. 원자라는 용어는 그리스어에서 파생되었으며 나눌 수 없음을 의미합니다. 그러나 많은 사람들이 잘 알지 못한다. 원자란 무엇인가 그것의 특성은 무엇입니까?
따라서 우리는 원자가 무엇인지, 그 특성과 중요성에 대해 설명하기 위해 이 기사를 바칠 것입니다.
원자란 무엇인가

원자는 양성자(양전하를 띤 입자)와 중성자(전기적으로 중성인 입자)가 있는 핵이라는 중심 부분으로 구성됩니다. 핵 주위의 영역은 전자(음으로 하전된 입자)에 의해 점유됩니다. 이 영역을 전기 레이어라고 합니다. 전기 쉘(음전하)과 코어(양전하)는 전기적 인력에 의해 결합됩니다.
원자의 평균 직경은 약 10-10m이고 핵의 평균 직경은 약 10-15m입니다. 그래서, 원자는 핵보다 10.000배에서 100.000배 더 큰 직경을 가지고 있습니다. 예를 들어, 원자가 축구장 크기라면 핵은 경기장 중앙에 있는 공과 같은 크기가 될 것입니다. 원자의 지름이 100미터라면 원자핵의 지름은 1센티미터입니다.
일부 역사

그리스 철학자 아리스토텔레스(기원전 384년 – 322년)는 모든 물질의 구성을 흙, 공기, 불, 물의 원소로 설명하려고 했습니다. 데모크리토스(기원전 546년 – 기원전 460년)는 입자의 크기에 한계가 있다는 생각을 제안한 그리스의 과학자이자 수학자였습니다. 이 입자들은 너무 작아져서 더 이상 나눌 수 없다고 그는 말했다. 그는 그러한 입자를 "원자"라고 불렀습니다.
XNUMX세기 대부분 동안 당시 고대인의 생각을 훨씬 뛰어넘는 원자 이론을 제안한 것은 영국 과학자 달튼의 원자 모델이었습니다.
이 이론은 모든 물질은 원자라고 하는 작은 불가분의 입자로 구성되어 있습니다. 최근 연구에 따르면 원자는 아원자 입자라고 하는 다른 작은 입자로 구성되어 있습니다.
역사적으로 원자 구조에 대한 현재 지식을 얻기 전에 물질의 구성에 대한 다양한 원자 이론이 개발되었습니다. 원자 이론을 바탕으로, 과학자들은 점진적으로 진화하는 원자 모델을 시연해 왔습니다.
John Dalton이 제안한 첫 번째 모델은 Niels Bohr의 원자 모델로 발전했습니다. 보어는 핵 주위를 도는 전자의 현재 모델과 매우 유사한 모델을 제안했습니다.
원자의 구조
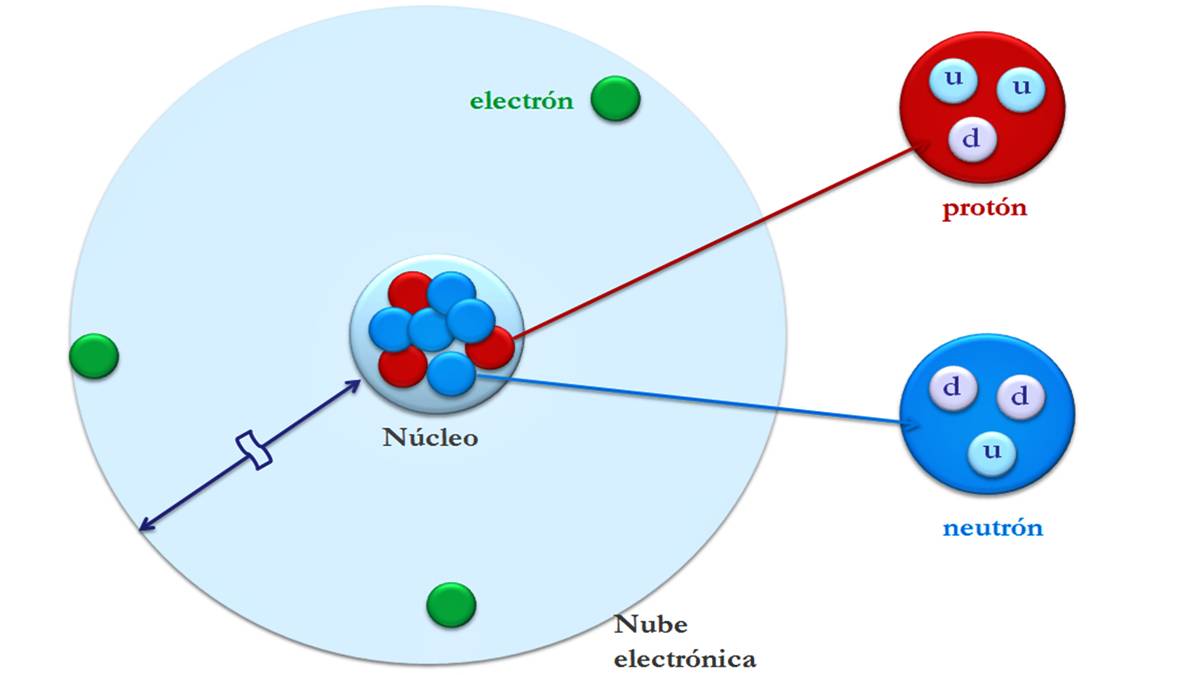
원자는 전자, 양성자 및 중성자와 같은 아 원자 입자라고하는 작은 입자로 구성됩니다. 원자 질량의 대부분은 핵에 집중되어 있습니다. 그리고 가장 큰 부피는 전자가 발견되는 전기 껍질에 있습니다.
전자, 양성자 및 중성자
전자는 음전하를 띠고 거의 질량이 없습니다. 그 질량은 원자핵의 약 1840배입니다.. 그들은 원자의 중심 핵 주위를 회전하는 작은 입자입니다. 또한 전자기장을 생성하는 핵 주위를 빠르게 이동합니다.
양성자는 절대값에서 전자의 전하와 동일한 양전하를 가지므로 양성자와 전자는 서로 끌어당기는 경향이 있습니다. 이들은 질량 단위를 구성하고 중성자와 함께 원자핵을 형성합니다.
중성자는 전하가 없습니다. 즉, 중성 전하를 가집니다. 양성자와 함께, 그것은 핵을 형성하고 원자의 거의 모든 질량(99,9%)을 나타냅니다. 중성자는 핵에 안정성을 제공합니다.
원자에는 에너지 준위가 있으며, 핵 주위를 돌고 있는 전자가 있는 핵 주위에 XNUMX개의 껍질이 있습니다. 껍질의 이름은 K, L, M, N, O, P, Q입니다. 각 껍질은 한정된 수의 전자를 수용할 수 있습니다(껍질당 XNUMX개의 전자). 가장 바깥쪽 레이어는 항상 가장 역동적입니다. 수소 원자만 중성자를 갖지 않고 오직 하나의 전자만이 양성자 주위를 공전합니다.
화학적 특성
화학에서 원자는 일반적으로 모든 반응에서 원래의 특성을 유지하는 기본 단위입니다. 그것들은 파괴되거나 생성되지 않고 단순히 그들 사이의 다른 연결을 통해 다른 방식으로 배열됩니다.
원자는 서로 뭉쳐서 분자와 다른 종류의 물질을 만듭니다. 화학 반응에서 생성된 결합은 다른 화학 원소를 구별하는 특정 구성을 가지고 있습니다. 이러한 원소는 원소 주기율표에 나타나는 원소입니다.
이러한 각 요소는 핵에 많은 양성자를 가지고 있습니다. 이 숫자를 원자 번호라고 하며 문자 Z로 표시합니다. 동일한 양성자 수를 가진 모든 원자는 동일한 원소에 속하며 서로 다른 화학 원소이지만 동일한 화학적 특성을 갖습니다.
또한, 문자 A로 표시된 질량 수를 찾습니다. 이 숫자는 원자에 존재하는 핵자의 수를 나타냅니다. 우리가 찾을 수 있고 우리가 가장 잘 알고 있는 또 다른 유형의 원자는 동위원소입니다. 이 원자들은 양성자 수는 같지만 중성자 수는 다릅니다. 물리적 특성은 서로 다르지만 화학적 특성은 동일합니다.
앞서 언급했듯이 동위 원소는 매우 중요합니다. 우라늄 농축은 하나의 우라늄 동위원소를 더 불안정한 화학 구조를 가진 다른 동위원소로 변환하여 연쇄 반응을 일으킬 수 있기 때문에 원자력 발전에 필수적입니다.
등록
원자를 정의하는 속성은 다음과 같습니다.
- 핵의 양성자 수를 나타내는 원자 번호(Z). 같은 수의 양성자를 가진 모든 원자는 같은 원소에 속합니다. 예를 들어, 양성자가 하나만 있는 수소 원자.
- 질량수는 양성자와 중성자의 합을 의미합니다.. 중성자 수가 다른 원소는 같은 원소의 다른 동위원소입니다.
- 전기음성도 원자가 화학 결합을 형성할 때 전자를 끌어당기는 경향입니다.
- 원자 반경 같은 원소의 결합된 두 핵 사이의 거리의 절반에 해당합니다.
- 이온화 잠재력 원소에서 전자를 제거하는 데 필요한 에너지입니다.
이 정보를 통해 원자가 무엇이며 그 특성에 대해 더 많이 알 수 있기를 바랍니다.
매우 좋은
리카르도