Dalam bidang fisika, terdapat cabang yang bertugas mempelajari transformasi yang dihasilkan oleh kalor dan usaha dalam sistem. Ini tentang termodinamika. Ini adalah cabang fisika yang bertanggung jawab untuk mempelajari semua transisi, yang hanya merupakan hasil dari proses yang melibatkan perubahan variabel keadaan suhu dan energi pada tingkat makro. Ada beberapa prinsip termodinamika yang mendasar bagi banyak aspek fisika.
Oleh karena itu, kami akan memberi tahu Anda dalam artikel ini apa prinsip-prinsip termodinamika dan apa pentingnya.
Karakteristik termodinamika
Jika kita menganalisis termodinamika klasik, kita akan menemukan bahwa termodinamika didasarkan pada konsep sistem makroskopik. Sistem ini hanya bagian dari kualitas fisik atau konseptual pemisahan dari lingkungan eksternal. Untuk mempelajari sistem termodinamika dengan lebih baik, selalu diasumsikan bahwa itu adalah massa fisik yang itu tidak terganggu oleh pertukaran energi dengan ekosistem eksternal.
Keadaan sistem makroskopik dalam kesetimbangan ditentukan oleh kuantitas yang disebut variabel termodinamika. Kita tahu semua variabel ini: suhu, tekanan, volume, dan komposisi kimia. Semua variabel ini mendefinisikan sistem dan keseimbangannya. Berkat aliansi aplikasi internasional, simbol utama termodinamika kimia telah ditetapkan. Menggunakan unit ini dapat bekerja lebih baik dan menjelaskan prinsip-prinsip termodinamika.
Namun, ada cabang termodinamika yang tidak mempelajari kesetimbangan, Sebaliknya, mereka bertugas menganalisis proses termodinamika yang terutama ditandai dengan tidak memiliki kemampuan untuk mencapai kondisi keseimbangan dengan cara yang stabil.
Prinsip termodinamika
Ada 4 prinsip termodinamika, terdaftar dari nol sampai tiga poin, hukum-hukum ini membantu untuk memahami semua hukum fisika di alam semesta kita dan tidak mungkin untuk melihat fenomena tertentu di dunia kita. Mereka juga dikenal dengan nama hukum termodinamika. Hukum-hukum ini memiliki asal-usul yang berbeda. Beberapa diformulasikan dari formula sebelumnya. Hukum termodinamika terakhir yang diketahui adalah hukum nol. Undang-undang ini bersifat permanen dalam semua penyelidikan dan penyelidikan yang dilakukan di laboratorium. Mereka sangat penting untuk memahami bagaimana alam semesta kita bekerja. Kami akan menjelaskan prinsip-prinsip termodinamika satu per satu.
Prinsip pertama
Hukum ini mengatakan bahwa energi tidak dapat diciptakan atau dimusnahkan, hanya dapat diubah. Ini juga dikenal sebagai hukum kekekalan energi. Sebenarnya, ini berarti bahwa dalam setiap sistem fisik yang terisolasi dari lingkungannya, semua energinya akan selalu sama. Meskipun energi dapat diubah menjadi jenis energi lain dalam satu atau lain bentuk, jumlah semua energi ini selalu sama.
Kami akan memberikan contoh untuk memahaminya dengan lebih baik. Mengikuti prinsip ini, jika kita menyumbangkan sejumlah energi ke sistem fisik dalam bentuk panas, kita dapat menghitung energi total dengan menemukan perbedaan antara peningkatan energi internal dan pekerjaan yang dilakukan oleh sistem dan lingkungannya. Artinya, perbedaan antara energi yang dimiliki sistem pada saat itu dan kerja yang dilakukan sistem akan menjadi energi panas yang dilepaskan.
Prinsip kedua
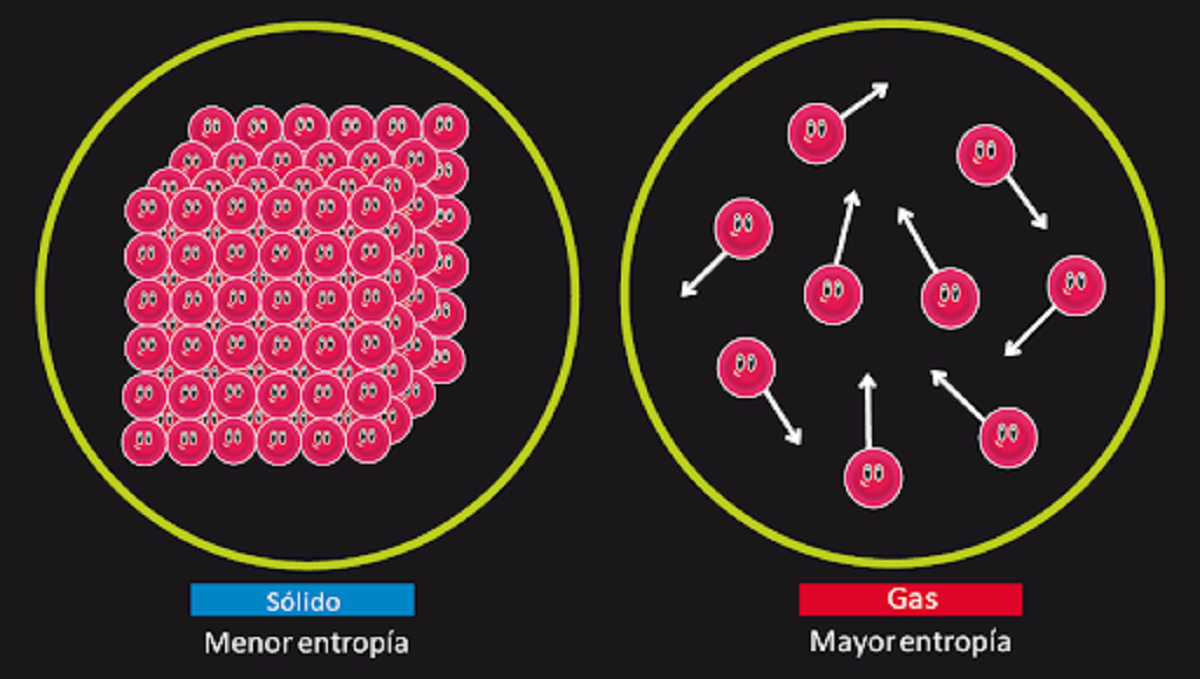
Jika ada cukup waktu, semua sistem pada akhirnya akan kehilangan keseimbangan. Prinsip ini juga disebut hukum entropi. Dapat diringkas sebagai berikut. Jumlah entropi di alam semesta akan meningkat seiring waktu. Entropi sistem adalah indeks untuk mengukur derajat ketidakteraturan. Dengan kata lain, Prinsip kedua termodinamika memberitahu kita bahwa setelah sistem mencapai titik kesetimbangan, itu akan meningkatkan tingkat gangguan dalam sistem. Ini bisa berarti bahwa jika kita memberikan waktu yang cukup pada sistem, pada akhirnya akan menjadi tidak seimbang.
Ini adalah hukum yang bertanggung jawab untuk menjelaskan ireversibilitas beberapa fenomena fisik. Misalnya, ini membantu kami menjelaskan mengapa sebuah makalah kertas yang telah terbakar tidak dapat kembali ke bentuk semula. Dalam sistem yang dikenal sebagai kertas dan api ini, kekacauan telah meningkat sedemikian rupa sehingga tidak mungkin untuk kembali ke asalnya. Hukum ini memperkenalkan fungsi keadaan entropi, yang dalam kasus sistem fisik bertanggung jawab untuk merepresentasikan tingkat ketidakteraturan dan kehilangan energinya yang tak terhindarkan.
Untuk memahami prinsip kedua termodinamika kita akan memberikan contoh. Jika kita membakar sejumlah materi dan kita menyatukan bola dengan abu yang dihasilkan, kita dapat melihat bahwa ada lebih sedikit materi daripada keadaan awal. Ini karena materi telah berubah menjadi gas yang Mereka tidak dapat dipulihkan dan mereka harus tersebar dan berantakan. Ini adalah bagaimana kita melihat bahwa di negara bagian satu setidaknya ada entropi daripada di negara bagian dua.
Prinsip ketiga
Ketika nol mutlak tercapai, proses sistem fisik berhenti. Nol mutlak adalah suhu terendah yang bisa kita capai. Dalam hal ini, kami mengukur suhu dalam derajat Kelvin. Dengan cara ini, dapat dikatakan bahwa suhu dan pendinginan menyebabkan entropi sistem menjadi nol. Dalam kasus ini, ini lebih seperti konstanta yang pasti. Ketika mencapai nol mutlak, proses sistem fisik berhenti. Oleh karena itu, entropi akan memiliki nilai minimum tetapi konstan.
Mencapai nol mutlak atau tidak adalah tugas yang mudah. Nilai nol mutlak dari derajat Kelvin adalah nol, tetapi jika kita menggunakannya dalam Pengukuran skala suhu Celcius, adalah -273,15 derajat.
Hukum nol
hukum ini adalah yang terakhir diasumsikan dan mengatakan bahwa jika A = C dan B = C, maka A = B. Ini menetapkan aturan dasar dan dasar dari tiga hukum termodinamika lainnya. Ini adalah nama yang mengasumsikan hukum keseimbangan termal. Dengan kata lain, jika sistem dan sistem lain secara independen dalam kesetimbangan termal, mereka harus berada dalam kesetimbangan termal. Hukum ini memungkinkan pembentukan prinsip-prinsip suhu. Prinsip ini digunakan untuk membandingkan energi panas dari dua benda yang berbeda dalam keadaan kesetimbangan termal. Jika kedua benda ini berada dalam kesetimbangan termal, mereka tidak perlu berada pada suhu yang sama. Di sisi lain, jika keduanya mengubah keseimbangan termal sistem ketiga, mereka juga akan saling mempengaruhi.
Saya berharap dengan informasi ini Anda dapat mempelajari lebih lanjut tentang prinsip-prinsip termodinamika karakteristiknya.