
La Hukum Boyle itu ditemukan oleh Robert Boyle pada abad ke-XNUMX dan meletakkan dasar untuk menjelaskan hubungan antara tekanan dan volume yang ada dalam gas. Melalui serangkaian percobaan, ia berhasil menunjukkan bahwa jika suhunya konstan, gas berkurang volumenya ketika diberi tekanan lebih, dan volumenya meningkat jika tekanannya dikurangi.
Pada artikel ini kami akan memberi tahu Anda semua yang perlu Anda ketahui tentang hukum Boyle, karakteristik dan kepentingannya.
Fitur utama
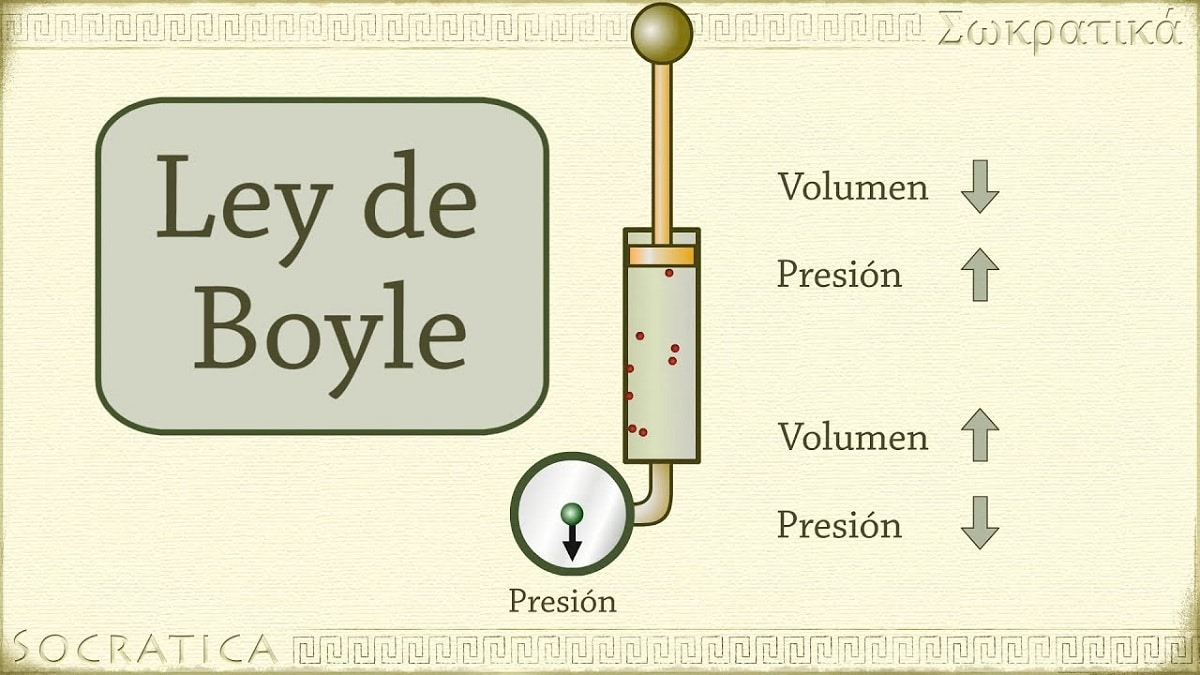
Pada tahun 1662, Robert Boyle menemukan bahwa tekanan yang diberikan pada gas berbanding terbalik dengan volume dan jumlah molnya pada suhu konstan. Dengan kata lain, jika tekanan yang diberikan pada gas menjadi dua kali lipat, gas yang sama akan dikompresi dan volumenya akan menjadi setengahnya.
Ketika volume wadah yang berisi gas meningkat, jarak yang harus ditempuh partikel sebelum bertabrakan dengan dinding wadah juga meningkat. Peningkatan jarak ini memungkinkan frekuensi guncangan berkurang, sehingga tekanan pada dinding lebih kecil dari sebelumnya ketika volumenya lebih kecil.
Hukum Boyle pertama kali ditemukan pada tahun 1662 oleh Robert Boyle. Edme Mariotte adalah ilmuwan lain yang berpikir dan sampai pada kesimpulan yang sama seperti Boyle, namun, Mariotte tidak mempublikasikan karyanya sampai tahun 1676. Itulah sebabnya dalam banyak buku kita menemukan hukum ini yang disebut Hukum Boyle dan Mariot Hukum Boyle-Mariot, juga dikenal sebagai Hukum Mattut, yang dikembangkan oleh fisikawan dan kimiawan Inggris Robert Ini dirumuskan independen oleh Boyle dan fisikawan dan ahli botani Prancis Edmé Mattout.
Ini mengacu pada salah satu hukum yang menghubungkan volume dan tekanan gas dengan sejumlah gas yang dipertahankan pada suhu konstan. Hukum Boyle menyatakan sebagai berikut: Tekanan yang diberikan oleh suatu gaya secara fisik berbanding terbalik dengan volume materi gas selama suhunya tetap konstan. Atau lebih sederhananya, kita bisa mengartikannya sebagai: pada suhu konstan yang lebih tinggi, volume gas dengan massa tetap berbanding terbalik dengan tekanan konstan yang diberikannya.
Eksperimen dan penerapan hukum Boyle

Untuk membuktikan teori Hukum Boyle, Mariot bertugas memasukkan gas ke dalam silinder dengan piston dan mampu memverifikasi berbagai tekanan yang diciptakan saat piston turun. Dari percobaan ini disimpulkan bahwa ketika volume meningkat, tekanan berkurang.
Hukum Boyle memiliki banyak aplikasi dalam kehidupan modern, di antaranya dapat kita sebutkan misalnya menyelam, hal ini karena penyelam harus mengeluarkan udara dari paru-parunya ketika naik karena mengembang ketika tekanan berkurang, jika tidak melakukannya dapat menyebabkan kerusakan jaringan.
Itu ditemukan di semua peralatan yang menggunakan atau ditenagai oleh tenaga pneumatik, seperti lengan robot yang menggunakan komponen seperti piston pneumatik, aktuator, pengatur tekanan, dan katup pelepas tekanan.
Mesin bensin, gas atau diesel juga menggunakan hukum Boyle selama pembakaran internal, karena pertama kali udara masuk ke silinder dengan volume dan tekanan, kedua kalinya mengurangi volume dengan meningkatkan tekanan.
Mobil memiliki sistem airbag yang bekerja dengan cara mengeluarkan sejumlah udara atau gas dari suatu ruangan yang mencapai luar airbag, di mana tekanan berkurang dan volume meningkat dengan mempertahankan suhu konstan.
Hukum Boyle sangat penting saat ini karena merupakan hukum yang berbicara kepada kita dan menjelaskan perilaku gas. Ini jelas menjelaskan bahwa tekanan dan volume gas berbanding terbalik satu sama lain. Oleh karena itu, ketika tekanan diterapkan pada gas, volumenya berkurang dan tekanannya meningkat.
model gas ideal

Hukum Boyle-Mariotte berlaku untuk apa yang disebut gas ideal, model teoretis yang sangat menyederhanakan perilaku gas apa pun, dengan asumsi:
- molekul gas mereka sangat kecil sehingga tidak perlu memikirkan ukurannya, terutama mengingat jarak ini jauh lebih kecil daripada jarak yang mereka tempuh.
- Selain itu, molekul hampir tidak berinteraksi, kecuali ketika mereka bertabrakan sangat singkat, dan ketika mereka bertabrakan, tumbukan itu elastis, sehingga momentum dan energi kinetik dilestarikan.
- Akhirnya, anggaplah bahwa energi kinetik ini sebanding dengan suhu sampel gas, yaitu, semakin diaduk partikel, semakin tinggi suhunya.
Gas ringan, terlepas dari identitasnya, ikuti panduan ini dengan sangat ketat di bawah kondisi suhu dan tekanan standar (yaitu: 0ºC dan tekanan atmosfer (1 atmosfer). Untuk gas-gas ini, hukum Boyle-Mariotte menjelaskan perilakunya dengan sangat tepat. .
Karena P∙V konstan pada suhu tertentu, jika tekanan gas berubah, volume berubah sehingga produk tetap sama, sehingga dalam dua keadaan berbeda 1 dan 2, persamaan dapat dinyatakan sebagai berikut:
P1∙V1 = P2∙V2
Kemudian mengetahui satu keadaan, ditambah variabel dari keadaan lain, Anda dapat mengetahui variabel yang hilang dengan menghapusnya dari hukum Boyle-Mariot.
Sejarah Hukum Boyle
ahli kimia Inggris. Pelopor eksperimen di bidang kimia khususnya pada sifat-sifat gas,
Tesis Robert Boyle tentang perilaku materi pada tingkat partikel merupakan pendahulu dari teori modern tentang unsur-unsur kimia. Dia juga anggota pendiri Royal Society of London.
Robert Boyle lahir dalam keluarga bangsawan di Irlandia dan bersekolah di sekolah Inggris dan Eropa terbaik. Dari 1656 hingga 1668 ia menjabat sebagai asisten Robert Hooke di Universitas Oxford, berkolaborasi dengannya dalam serangkaian eksperimen yang menentukan sifat fisik udara dan bagaimana ia membakar, bernafas, dan mentransmisikan suara.
Hasil dari kontribusi tersebut dikumpulkan dalam «Eksperimen fisik-mekanik baru tentang elastisitas udara dan efeknya» (1660). Dalam edisi kedua karya ini (1662), ia mengungkapkan sifat terkenal gas, hukum Boyle-Mariotte, yang menyatakan bahwa volume yang ditempati oleh gas pada suhu konstan berbanding terbalik dengan tekanannya. Hari ini diketahui bahwa hukum ini terpenuhi hanya ketika perilaku ideal teoritis gas diterima.
Saya berharap dengan informasi ini Anda dapat mempelajari lebih lanjut tentang hukum Boyle, karakteristiknya dan aplikasinya dalam dunia sains.