
La Boyle törvénye Robert Boyle fedezte fel a XNUMX. században, és megalapozta a gázokban jelenlévő nyomás és térfogat kapcsolatának magyarázatát. Kísérletsorozattal sikerült kimutatnia, hogy ha a hőmérséklet állandó, akkor a gáz térfogata csökken, ha nagyobb nyomásnak van kitéve, és térfogata nő, ha a nyomást csökkentik.
Ebben a cikkben mindent elmondunk, amit a Boyle-törvényről, annak jellemzőiről és fontosságáról tudni kell.
Főbb jellemzők
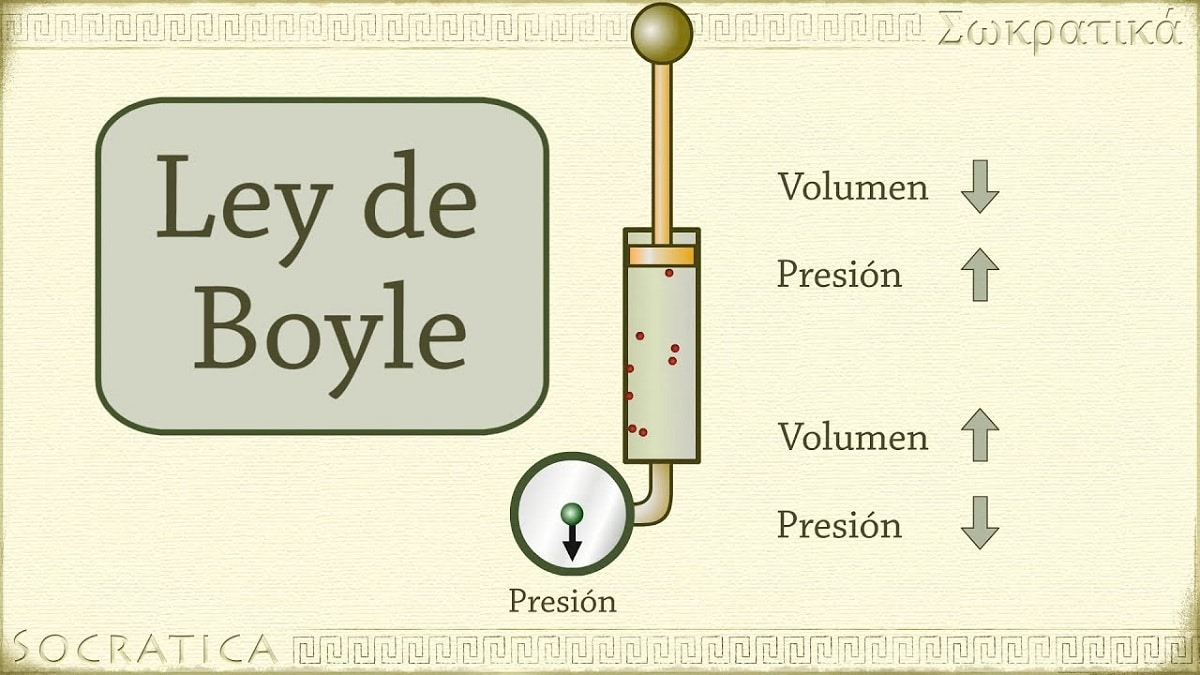
1662-ben Robert Boyle felfedezte, hogy a gázra gyakorolt nyomás fordítottan arányos annak térfogatával és móljainak számával állandó hőmérsékleten. Más szóval, ha a gázra alkalmazott nyomás megkétszereződik, ugyanaz a gáz összenyomódik, és térfogata felére csökken.
A gázt tartalmazó tartály térfogatának növekedésével az a távolság is növekszik, amelyet a részecskéknek meg kell tenniük, mielőtt a tartály falával ütköznének. Ez a távolságnövekedés lehetővé teszi az ütések gyakoriságának csökkentését, így a falra nehezedő nyomás kisebb, mint korábban, amikor a térfogat kisebb volt.
A Boyle-törvényt először Robert Boyle fedezte fel 1662-ben. Edme Mariotte egy másik tudós volt, aki gondolkodott és ugyanazokra a következtetésekre jutott, mint BoyleMariotte azonban csak 1676-ban hozta nyilvánosságra munkáját. Ezért találjuk sok könyvben ezt a Boyle-törvényt és a Boyle-Mariot-törvényt, más néven Mattut törvényét, amelyet Robert brit fizikus és vegyész dolgozott ki. egymástól függetlenül Boyle és Edmé Mattout francia fizikus és botanikus.
Az egyik olyan törvényre utal, amely a gáz térfogatát és nyomását egy bizonyos mennyiségű, állandó hőmérsékleten tartott gázhoz köti. A Boyle-törvény a következőket mondja ki: Az erő által kifejtett nyomás fizikailag fordítottan arányos a gáznemű anyag térfogatával mindaddig, amíg hőmérséklete állandó marad. Vagy egyszerűbben értelmezhetjük így: magasabb állandó hőmérsékleten egy rögzített tömegű gáz térfogata fordítottan arányos az általa kifejtett állandó nyomással.
A Boyle-törvény kísérletei és alkalmazásai

A Boyle-törvény elméletének bizonyítására Mariot feladata volt, hogy egy dugattyúval gázt vezessenek be egy hengerbe, és ellenőrizni tudta a különböző nyomásokat, amelyek a dugattyú leereszkedésekor keletkeztek. Ebből a kísérletből arra következtethetünk, hogy a térfogat növekedésével a nyomás csökken.
A Boyle-törvénynek számos alkalmazása van a modern életben, ezek között említhetjük például a búvárkodást, ennek oka, hogy a búvárnak emelkedéskor ki kell ürítenie a tüdejéből a levegőt, mert a nyomás csökkenésével kitágul, ha nem így tesz, szövetkárosodást okozhat.
Minden olyan berendezésben megtalálható, amely pneumatikus erőt használ, vagy azt hajtja meg, például olyan robotkarokban, amelyek pneumatikus dugattyúkat, működtetőket, nyomásszabályozókat és nyomáscsökkentő szelepeket használnak.
A benzin-, gáz- vagy dízelmotorok a belső égés során is alkalmazzák a Boyle-törvényt, mert az első alkalommal a levegő térfogattal és nyomással kerül a hengerbe, másodszor pedig a nyomás növelésével csökkenti a térfogatot.
Az autók légzsákrendszerei úgy működnek, hogy bizonyos mennyiségű levegőt vagy gázt kiszorítanak a külső légzsákot elérő kamrából, ahol a nyomás csökken és a térfogat növekszik állandó hőmérsékleten tartva.
A Boyle-törvény ma nagyon fontos, mert ez a törvény szól hozzánk és magyarázza meg a gázok viselkedését. Ez határozottan megmagyarázza, hogy a gáz nyomása és térfogata fordítottan arányos egymással. Ezért ha nyomást gyakorolnak egy gázra, annak térfogata csökken, nyomása pedig nő.
ideális gázmodell

A Boyle-Mariotte törvény az úgynevezett ideális gázokra vonatkozik, egy olyan elméleti modell, amely nagymértékben leegyszerűsíti bármely gáz viselkedését, feltételezve:
- gázmolekulák olyan kicsik, hogy nem kell a méretükre gondolni, különösen, ha figyelembe vesszük, hogy ez sokkal kisebb, mint az általuk megtett távolság.
- Ezen túlmenően, a molekulák alig lépnek kölcsönhatásba, kivéve, ha nagyon rövid ideig ütköznek, és amikor mégis, az ütközés rugalmas, így a lendület és a mozgási energia is megmarad.
- Végül tegyük fel, hogy ez a kinetikus energia arányos a gázhalmazállapotú minta hőmérsékletével, azaz minél felkavartabbak a részecskék, annál magasabb a hőmérséklet.
A könnyű gázok, identitásuktól függetlenül, nagyon szigorúan betartják ezeket az irányelveket szabványos hőmérsékleti és nyomási feltételek mellett (pl.: 0ºC és légköri nyomás (1 atmoszféra). Ezeknél a gázoknál a Boyle-Mariotte törvény nagyon pontosan leírja viselkedésüket).
Mivel P∙V egy adott hőmérsékleten állandó, ha a gáz nyomása megváltozik, a térfogat úgy változik, hogy a szorzat változatlan marad, így két különböző, 1-es és 2-es állapotban az egyenlőség a következőképpen fejezhető ki:
P1∙V1 = P2∙V2
Ezután az egyik állapot és a másik állapot változójának ismeretében megtudhatja a hiányzó változót, ha eltávolítja a Boyle-Mariot törvényből.
A Boyle-törvény története
brit vegyész. A kísérletek úttörője a kémia területén, különös tekintettel a gázok tulajdonságaira,
Robert Boyle tézise az anyag részecskeszintű viselkedéséről a kémiai elemek modern elméletének előfutára volt. Alapító tagja volt a Londoni Királyi Társaságnak is.
Robert Boyle nemesi családban született Írországban, és a legjobb angol és európai iskolákba járt. 1656 és 1668 között Robert Hooke asszisztenseként dolgozott az Oxfordi Egyetemen, és együttműködött vele egy sor kísérletben, amelyek meghatározták a levegő fizikai tulajdonságait, valamint azt, hogy hogyan ég, lélegzik és hogyan továbbítja a hangot.
Ezeknek a hozzájárulásoknak az eredményeit összegyűjtötték „Új fizikai-mechanikai kísérletek a levegő rugalmasságáról és hatásairól» (1660). E munka második kiadásában (1662) feltárta a gázok híres tulajdonságát, a Boyle-Mariotte törvényt, amely kimondta, hogy a gáz állandó hőmérsékletű térfogata fordítottan arányos a nyomásával. Ma már tudjuk, hogy ez a törvény csak akkor teljesül, ha elfogadjuk a gázok elméleti ideális viselkedését.
Remélem, hogy ezen információk birtokában többet megtudhat a Boyle-törvényről, annak jellemzőiről és alkalmazásairól a tudomány világában.