
Kemijska promjena je promjena tvari kojom se mijenja njezina kemijska struktura, odnosno mijenjaju se njezina svojstva, a ne samo oblik. To znači da kemijska promjena, također poznata kao kemijska reakcija ili kemijski fenomen, uključuje kidanje i stvaranje kemijskih veza u jednoj tvari ili spoju kako bi nastala nova tvar ili spoj. Postoje brojni kemijske promjene u svijetu.
Iz tog razloga, ovaj ćemo članak posvetiti tome da vam kažemo koje su glavne kemijske promjene koje postoje i njihov primjer.
Što su kemijske promjene?

Kada dvije ili više tvari (koje se nazivaju reaktanti ili reaktanti) prolaze kroz kemijsku reakciju, pri čemu mijenjaju svoju kemijsku strukturu i mogu se konzumirati (endotermne reakcije) ili oslobađanje (egzotermne reakcije) energije, proizvodeći dvije ili više tvari (koje se nazivaju produkt). Neke kemijske reakcije opasne su za ljude jer mogu uključivati ili proizvoditi otrovne ili korozivne spojeve. Ostale reakcije, kao što su određene egzotermne reakcije, mogu uzrokovati eksplozije.
U kemijskoj industriji mnogi materijali koje koristimo u svakodnevnom životu proizvode se kontroliranim kemijskim reakcijama. Neke se reakcije odvijaju spontano, druge moraju proizvesti ljudi u tvornicama ili kemijskim laboratorijima. Za odvijanje kemijske reakcije potrebno je određeno vrijeme. ovisno o prirodi reaktanata i uvjetima u kojima se reakcija odvija.
Stoga čimbenici koji utječu na brzinu kemijskih reakcija općenito uključuju:
- Temperatura raste. Povećanje temperature ima tendenciju povećanja brzine kemijske reakcije.
- povećani pritisak. Povećanje tlaka općenito povećava brzinu kemijske reakcije. To se obično događa kada tvari koje su osjetljive na promjene tlaka, poput plinova, reagiraju. U slučaju tekućina i krutina, promjene tlaka ne uzrokuju značajne promjene u njihovim brzinama reakcije.
- Agregacijsko stanje reagensa. Krutine općenito reagiraju sporije od tekućina ili plinova, iako brzina također ovisi o reaktivnosti svake tvari.
- Upotreba katalizatora. To su tvari koje se koriste za povećanje brzine kemijskih reakcija. Te tvari ne ometaju reakciju, one samo kontroliraju brzinu kojom se reakcija odvija. Postoje i tvari zvane inhibitori, koje se koriste na isti način, ali imaju suprotan učinak, usporavaju reakciju.
- svjetlosna energija. Neke kemijske reakcije se ubrzavaju kada na njih padne svjetlost.
- Koncentracija reagensa. Većina kemijskih reakcija odvija se brže ako su koncentracije reaktanata visoke.
Primjeri kemijskih promjena
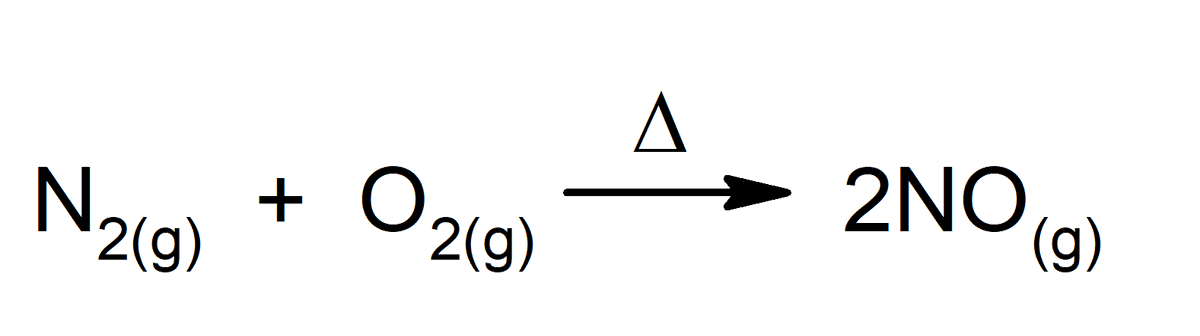
Svaka kemijska reakcija savršen je primjer kemijske promjene, čak i one koje se odvijaju unutar našeg tijela. Neki primjeri su:
- Disanje. Ovo je kemijski izmijenjen biološki proces u kojem se kisik uzima iz zraka i koristi za reakciju s glukozom koju dobivamo iz hrane, proizvodeći visoke razine kemijske energije (ATP) i velike količine otpadnog ugljičnog dioksida (CO2). koji se mora izlučuje se.
- Kisela kiša. Javlja se u okruženjima s velikim onečišćenjem zraka. Obično je rezultat kemijske promjene između vode pohranjene u oblacima i drugih plinova raspršenih u zraku, čiji sadržaj sumpornog oksida ili dušikovog oksida stvara sumpornu kiselinu ili dušičnu kiselinu koja pada s kišnicom i tvori sol. Reakcija koja se odvija unutar baterije je između kiseline i metala. Na primjer, baterija koja koristi olovo i sumpornu kiselinu proizvodi olovo(II) sulfat, bijelu sol. Razgradnja ozona. Molekule ozona pod djelovanjem neke vrste svjetlosti razgrađuju se na molekule kisika.
Kemijska promjena i fizička promjena

Fizikalne promjene tvari ne mijenjaju njezin sastav, odnosno ne mijenjaju kemijsku strukturu tvari, pa se tvari ne mogu razgraditi niti nastati fizikalnim promjenama. Fizička promjena jednostavno mijenja fizikalna svojstva materije, kao što su oblik, gustoća i stanje agregacije (krutina, tekućina, plin). Fizičke promjene, s druge strane, Obično su reverzibilni jer mijenjaju oblik ili stanje tvari, ali ne i njezin sastav.
Na primjer, kada voda proključa, tekućinu možemo pretvoriti u plin, ali nastala para i dalje se sastoji od molekula vode. Nasuprot tome, ako zamrznemo vodu, ona postaje kruta, ali je i dalje kemijski ista tvar.
Drugi je primjer ukapljeni plin koji koristimo u upaljačima za cigarete, obično butan (C4H10) ili propan (C3H8) koji postaje tekući kada se primijeni visoki tlak, ali ne mijenja svoj kemijski sastav.
Kemijska promjena mijenja raspored i vezu atoma u tvari tako da se oni spajaju na drugačiji način, što rezultira drugačijom tvari od izvorne. Kada dođe do kemijske promjene, uvijek završite s istom količinom tvari s kojom ste počeli, čak i ako je u drugačijem omjeru, jer se materija ne može stvoriti ili uništiti, samo transformirati.
Na primjer, ako reagiramo s vodom (H2O) i kalijem (K), dobit ćemo dvije nove tvari: kalijev hidroksid (KOH) i plin vodik (H2). To je reakcija koja općenito oslobađa puno energije i stoga je vrlo opasna.
Primjeri kemijskih promjena u tvarima
Pečenje kolačića ili kolača
Uobičajene stvari kao što su kolačići, kolači, kolači itd. skrivaju kemijsku reakciju zvanu fermentacija, u kojoj tijesto se diže zbog plinova koje proizvodi kvasac. U proizvodnji kruha kvasac pretvara škrob u glukozu.
Digestija
Probava hrane očiti je primjer kemijske promjene tvari hidrolizom (razgradnja organske tvari djelovanjem vode). Hrana koju jedemo u obliku voća, povrća, mesa itd., prolaze kroz proces miješanja sa želučanim sokovima kako bi bolje apsorbirali hranjive tvari te ih prema potrebama organizma pretvaraju u razne tvari.
U istom procesu, višak elemenata ili toksina se eliminira iz organizma na drugačiji način od prvobitnog; u obliku izmeta, urina, znoja itd.
pulque
Fermentacija je katabolički proces u kojem se molekule glukoze razgrađuju zbog nedostatka kisika. Neka od alkoholnih pića dobivenih procesom fermentacije su jabukovača, pivo i bezalkoholno vino, a potonje je jedno od najmanje poznatih pića na svijetu. Pulque se dobiva iz biljke agave obrtničkim postupkoml, kod koje je sazrijevanje tvari ključno za dobivanje konačnog proizvoda, bijelog, kiselkastog i viskoznog, vrlo specifičnog okusa koji ne prija svakom nepcu.
Fermentacija se također događa tijekom izrade kruha, jogurta i sira, između ostalog.
Caramelo
Karamela je osnovni primjer kemijske promjene tvari, budući da se kruti bijeli šećer, zagrijavajući nekoliko minuta, pretvara u jantarnu masu ugodne arome. Drugim riječima, generira se proizvod potpuno drugačiji od originala.
Nadam se da s ovim informacijama možete naučiti više o kemijskim promjenama i njihovim primjerima.