
Atom je osnovna jedinica materije i najmanji je djelić kojim se može identificirati kemijski element. Sastoji se od atomske jezgre koja sadrži neutrone i protone te elektrone koji okružuju jezgru. Pojam atom potječe iz grčkog i znači nedjeljiv. Međutim, mnogi ljudi ne znaju dobro Što je atom niti koje su njegove karakteristike.
Stoga ćemo ovaj članak posvetiti tome da vam kažemo što je atom, njegove karakteristike i važnost.
Što je atom

Atomi se sastoje od središnjeg dijela koji se naziva jezgra, u kojem se nalaze protoni (pozitivno nabijene čestice) i neutroni (električno neutralne čestice). Područje oko jezgre zauzimaju elektroni (negativno nabijene čestice); ovo područje se naziva električni sloj. Električna ljuska (negativno nabijena) i jezgra (pozitivno nabijena) drže se zajedno električnom privlačnošću.
Prosječni promjer atoma je oko 10-10 metara, a prosječni promjer jezgre je oko 10-15 metara; tako, atom ima 10.000 100.000 do XNUMX XNUMX puta veći promjer od svoje jezgre. Na primjer, ako je atom veličine nogometnog igrališta, jezgra će biti iste veličine kao lopta u središtu igrališta. Ako atom ima promjer 100 metara, njegova jezgra ima promjer 1 centimetar.
Povijest

Grčki filozof Aristotel (384. pr. Kr. – 322. pr. Kr.) pokušao je objasniti sastav sve materije od elemenata: zemlje, zraka, vatre i vode. Demokrit (546. pr. Kr. – 460. pr. Kr.) bio je grčki znanstvenik i matematičar koji je predložio ideju da postoji ograničenje veličine čestica. Te čestice postaju toliko male da se više ne mogu podijeliti, rekao je. Takve je čestice nazvao "atomima".
Veći dio XNUMX. stoljeća atomski model britanskog znanstvenika Daltona bio je taj koji je predložio atomsku teoriju, koja je bila daleko izvan razmišljanja starih u to vrijeme.
Ova teorija to kaže Sva materija sastoji se od sićušnih nedjeljivih čestica koje se nazivaju atomi. Nedavna istraživanja otkrila su da se atomi sastoje od drugih malih čestica koje se nazivaju subatomske čestice.
Povijesno gledano, različite atomske teorije o sastavu materije razvijene su prije nego što je stečeno današnje znanje o strukturi atoma. Na temelju atomske teorije, Znanstvenici demonstriraju modele atoma koji se postupno razvijaju.
Prvi model koji je predložio John Dalton razvio se u model atoma Nielsa Bohra. Bohr je predložio model vrlo sličan trenutnom modelu elektrona koji kruže oko jezgre.
struktura atoma
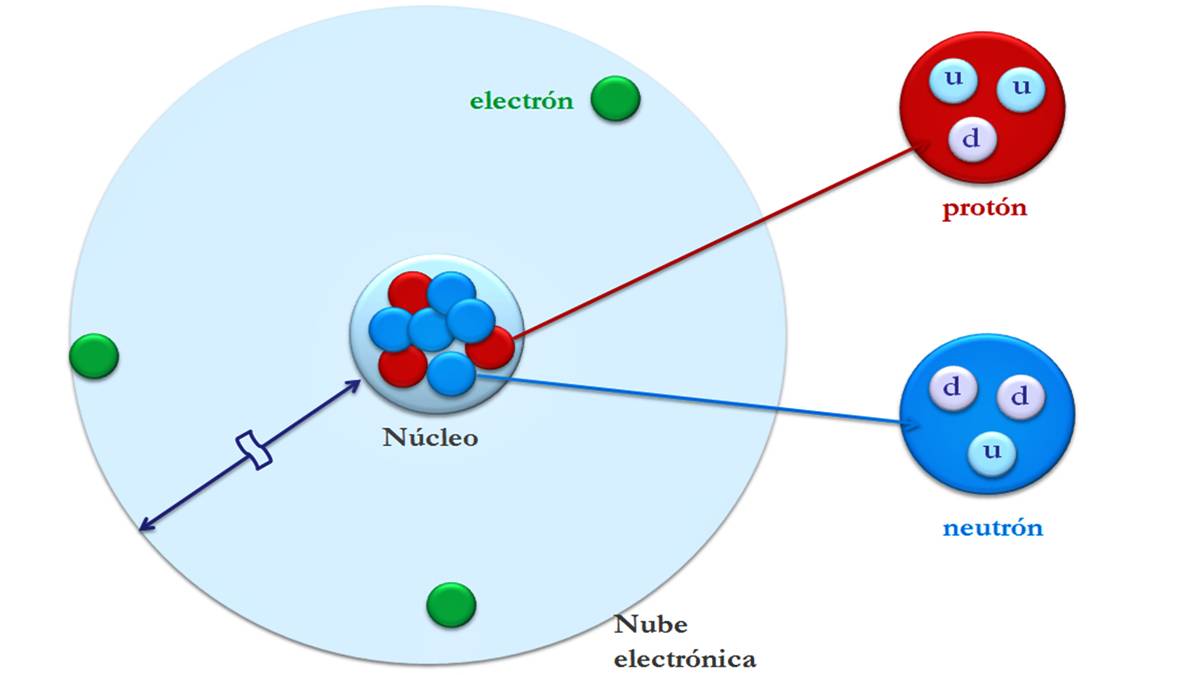
Atomi se sastoje od sićušnih čestica koje se nazivaju subatomske čestice: elektroni, protoni i neutroni. Najveći dio mase atoma koncentriran je u jezgri. A njegov najveći volumen je u električnoj ljusci gdje se nalaze elektroni.
Elektroni, protoni i neutroni
Elektroni su negativno nabijeni i nemaju gotovo nikakvu masu. Njegova masa je oko 1840 puta veća od mase atomske jezgre.. One su sićušne čestice koje se okreću oko središnje jezgre atoma. Osim toga, oni se brzo kreću oko jezgre stvarajući elektromagnetsko polje.
Proton ima isti pozitivan naboj kao naboj elektrona u apsolutnoj vrijednosti, tako da protoni i elektroni imaju tendenciju da se međusobno privlače. Oni čine jedinicu mase i zajedno s neutronima čine jezgru atoma.
Neutroni nemaju naboj, odnosno imaju neutralan naboj. Uz protone, čini jezgru i predstavlja gotovo svu masu (99,9%) atoma. Neutroni daju stabilnost jezgri.
Atomi imaju energetske razine, sedam ljuski oko jezgre u kojima se nalaze elektroni koji kruže oko jezgre. Ljuske se nazivaju K, L, M, N, O, P i Q. Svaka ljuska može sadržavati konačan broj elektrona: osam elektrona po ljusci. Krajnji vanjski sloj uvijek je najdinamičniji. Samo atom vodika nema neutrone i samo jedan elektron kruži oko protona.
kemijske karakteristike
U kemiji su atomi temeljne jedinice koje obično zadržavaju svoja izvorna svojstva u svakoj reakciji. Oni nisu uništeni ili stvoreni, oni su jednostavno raspoređeni na različite načine s različitim vezama među njima.
Atomi se skupljaju i stvaraju molekule i druge vrste materijala. Veze nastale u kemijskim reakcijama imaju određeni sastav koji razlikuje različite kemijske elemente. Ovi elementi su oni koji se pojavljuju u periodnom sustavu elemenata.
Svaki od ovih elemenata ima mnogo protona u jezgri. Taj se broj naziva atomski broj i označava se slovom Z. Svi atomi s istim brojem protona pripadaju istom elementu i imaju ista kemijska svojstva iako su različiti kemijski elementi.
Nadalje, nalazimo maseni broj, označen slovom A. Ovaj broj se odnosi na broj nukleona prisutnih u atomu. Još jedna vrsta atoma koju možemo pronaći i o kojoj najbolje znamo je izotop. Ti atomi imaju isti broj protona, ali različit broj neutrona. Imaju ista kemijska svojstva iako se njihova fizikalna svojstva međusobno razlikuju.
Kao što smo ranije primijetili, izotopi su vrlo važni. A vitalni su za nuklearnu energiju jer obogaćivanje urana uključuje pretvaranje jednog izotopa urana u drugi s nestabilnijom kemijskom strukturom, što nam omogućuje lančanu reakciju.
nekretnine
Svojstva koja definiraju atom su:
- Atomski broj (Z) koji označava broj protona u jezgri. Svi atomi s istim brojem protona pripadaju istom elementu. Na primjer, atom vodika sa samo jednim protonom.
- Maseni broj se odnosi na zbroj protona i neutrona.. Elementi s različitim brojem neutrona različiti su izotopi istog elementa.
- elektronegativnost To je tendencija atoma da privlače elektrone kada stvaraju kemijske veze.
- atomski radijus Odgovara polovici udaljenosti između dvije spojene jezgre istog elementa.
- potencijal ionizacije To je energija potrebna za uklanjanje elektrona iz elementa.
Nadam se da ćete s ovim informacijama saznati više o tome što je atom i njegovim karakteristikama.
VRLO DOBRO
RICARDO