
परमाणु पदार्थ की मूल इकाई है और सबसे छोटा अंश है जो रासायनिक तत्व की पहचान कर सकता है। इसमें एक परमाणु नाभिक होता है जिसमें न्यूट्रॉन और प्रोटॉन होते हैं, और नाभिक के आसपास के इलेक्ट्रॉन होते हैं। परमाणु शब्द ग्रीक से लिया गया है और इसका अर्थ है अविभाज्य। हालाँकि, बहुत से लोग अच्छी तरह से नहीं जानते हैं परमाणु क्या है न ही इसकी विशेषताएं क्या हैं।
इसलिए, हम आपको यह बताने के लिए इस लेख को समर्पित करने जा रहे हैं कि परमाणु क्या है, इसकी विशेषताएं और महत्व क्या है।
परमाणु क्या है

परमाणुओं में एक केंद्रीय भाग होता है जिसे नाभिक कहा जाता है, जिसमें प्रोटॉन (सकारात्मक रूप से आवेशित कण) और न्यूट्रॉन (विद्युत रूप से तटस्थ कण) रहते हैं। नाभिक के आसपास के क्षेत्र में इलेक्ट्रॉनों (नकारात्मक रूप से आवेशित कण) का कब्जा है; इस क्षेत्र को विद्युत परत कहा जाता है। विद्युत खोल (नकारात्मक रूप से आवेशित) और कोर (सकारात्मक रूप से आवेशित) विद्युत आकर्षण द्वारा एक साथ रखे जाते हैं।
एक परमाणु का औसत व्यास लगभग 10-10 मीटर है, और एक नाभिक का औसत व्यास लगभग 10-15 मीटर है; इसलिए, एक परमाणु का व्यास उसके नाभिक से 10.000 से 100.000 गुना बड़ा होता है। उदाहरण के लिए, यदि एक परमाणु एक फुटबॉल मैदान के आकार का है, तो नाभिक मैदान के केंद्र में गेंद के समान आकार का होगा। यदि किसी परमाणु का व्यास 100 मीटर है, तो उसके नाभिक का व्यास 1 सेंटीमीटर है।
कुछ इतिहास

यूनानी दार्शनिक अरस्तू (384 ईसा पूर्व - 322 ईसा पूर्व) ने तत्वों से सभी पदार्थों की संरचना की व्याख्या करने की कोशिश की: पृथ्वी, वायु, अग्नि और जल। डेमोक्रिटस (546 ईसा पूर्व - 460 ईसा पूर्व) एक यूनानी वैज्ञानिक और गणितज्ञ थे जिन्होंने इस विचार का प्रस्ताव रखा कि कणों के आकार की एक सीमा होती है। उन्होंने कहा कि ये कण इतने छोटे हो जाते हैं कि इन्हें विभाजित नहीं किया जा सकता है। उन्होंने ऐसे कणों को "परमाणु" कहा।
XNUMXवीं शताब्दी के अधिकांश समय के लिए, यह ब्रिटिश वैज्ञानिक डाल्टन का परमाणु मॉडल था जिसने परमाणु सिद्धांत का प्रस्ताव रखा था, जो उस समय के पूर्वजों की सोच से बहुत परे था।
यह सिद्धांत कहता है कि सभी पदार्थ सूक्ष्म अविभाज्य कणों से बने होते हैं जिन्हें परमाणु कहा जाता है। हाल के शोध में पाया गया है कि परमाणु अन्य छोटे कणों से बने होते हैं जिन्हें उप-परमाणु कण कहा जाता है।
ऐतिहासिक रूप से, परमाणु संरचना पर वर्तमान ज्ञान प्राप्त करने से पहले पदार्थ की संरचना पर विभिन्न परमाणु सिद्धांत विकसित किए गए हैं। परमाणु सिद्धांत के आधार पर, वैज्ञानिक परमाणुओं के धीरे-धीरे विकसित होने वाले मॉडलों का प्रदर्शन कर रहे हैं।
जॉन डाल्टन द्वारा प्रस्तावित पहला मॉडल परमाणु के नील्स बोह्र के मॉडल में विकसित हुआ। बोह्र ने नाभिक की परिक्रमा करने वाले इलेक्ट्रॉनों के वर्तमान मॉडल के समान एक मॉडल प्रस्तावित किया।
एक परमाणु की संरचना
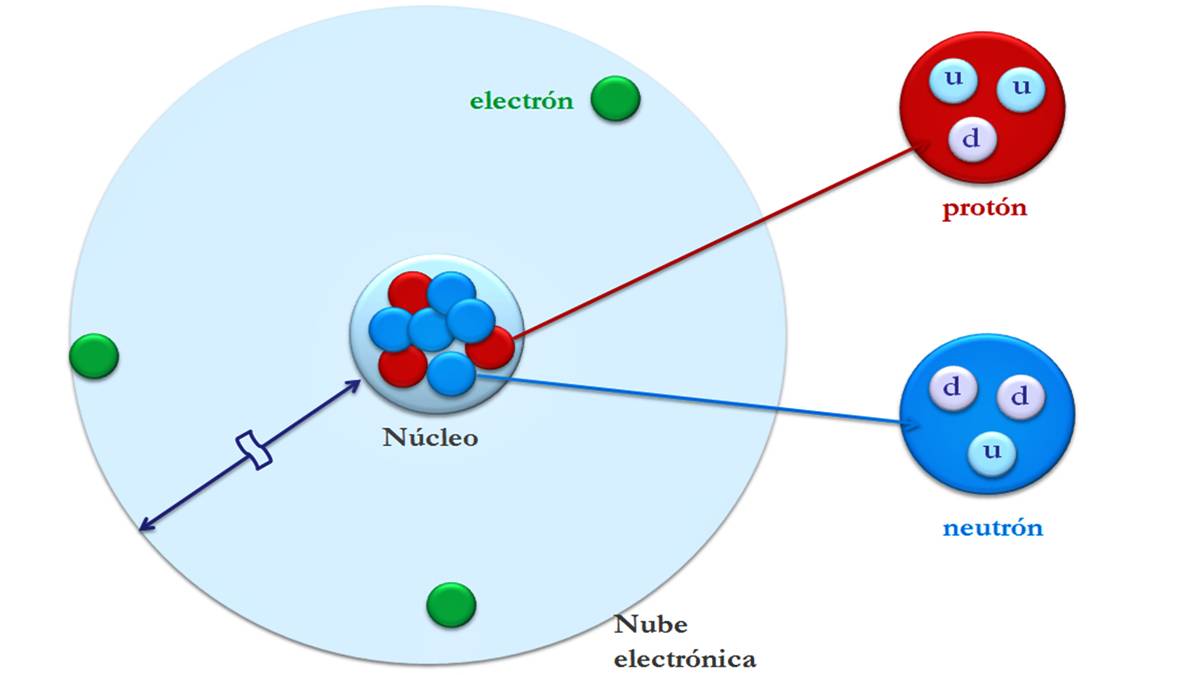
परमाणु सूक्ष्म कणों से बने होते हैं जिन्हें उपपरमाण्विक कण कहा जाता है: इलेक्ट्रॉन, प्रोटॉन और न्यूट्रॉन। परमाणु का अधिकांश द्रव्यमान नाभिक में केंद्रित होता है। और इसकी सबसे बड़ी मात्रा विद्युत खोल में होती है जहां इलेक्ट्रॉन पाए जाते हैं।
इलेक्ट्रॉन, प्रोटॉन और न्यूट्रॉन
इलेक्ट्रॉन ऋणात्मक रूप से आवेशित होते हैं और इनका लगभग कोई द्रव्यमान नहीं होता है। इसका द्रव्यमान परमाणु नाभिक के द्रव्यमान का लगभग 1840 गुना है।. वे छोटे कण होते हैं जो एक परमाणु के केंद्रीय नाभिक के चारों ओर घूमते हैं। इसके अलावा, वे एक विद्युत चुम्बकीय क्षेत्र उत्पन्न करने वाले नाभिक के चारों ओर तेजी से घूमते हैं।
एक प्रोटॉन का निरपेक्ष मूल्य में एक इलेक्ट्रॉन पर आवेश के समान धनात्मक आवेश होता है, इसलिए प्रोटॉन और इलेक्ट्रॉन एक दूसरे को आकर्षित करते हैं। ये द्रव्यमान की इकाई का निर्माण करते हैं और न्यूट्रॉन के साथ मिलकर परमाणु के नाभिक का निर्माण करते हैं।
न्यूट्रॉन के पास कोई चार्ज नहीं होता है, यानी उनके पास तटस्थ चार्ज होता है। प्रोटॉन के साथ-साथ, यह नाभिक बनाता है और परमाणु के लगभग सभी द्रव्यमान (99,9%) का प्रतिनिधित्व करता है। न्यूट्रॉन नाभिक को स्थिरता प्रदान करते हैं।
परमाणुओं में ऊर्जा का स्तर होता है, नाभिक के चारों ओर सात कोश होते हैं जिनमें नाभिक की परिक्रमा करने वाले इलेक्ट्रॉन होते हैं। गोले को K, L, M, N, O, P, और Q नाम दिया गया है। प्रत्येक खोल में इलेक्ट्रॉनों की एक परिमित संख्या हो सकती है: आठ इलेक्ट्रॉन प्रति खोल। सबसे बाहरी परत हमेशा सबसे गतिशील होती है। केवल हाइड्रोजन परमाणु में न्यूट्रॉन नहीं होते हैं और प्रोटॉन के चारों ओर केवल एक इलेक्ट्रॉन परिक्रमा करता है।
रासायनिक विशेषताएं
रसायन विज्ञान में, परमाणु मूलभूत इकाइयाँ हैं जो आमतौर पर हर प्रतिक्रिया में अपने मूल गुणों को बनाए रखती हैं। वे नष्ट या निर्मित नहीं होते हैं, वे बस उनके बीच अलग-अलग कनेक्शन के साथ अलग-अलग तरीकों से व्यवस्थित होते हैं।
अणु और अन्य प्रकार की सामग्री बनाने के लिए परमाणु आपस में टकराते हैं। रासायनिक अभिक्रियाओं में बनने वाले बंधों की एक निश्चित संरचना होती है जो विभिन्न रासायनिक तत्वों को अलग करती है। ये तत्व वे तत्व हैं जो तत्वों की आवर्त सारणी पर दिखाई देते हैं।
इनमें से प्रत्येक तत्व के नाभिक में कई प्रोटॉन होते हैं। इस संख्या को परमाणु संख्या कहा जाता है और अक्षर Z द्वारा निरूपित किया जाता है। समान संख्या में प्रोटॉन वाले सभी परमाणु एक ही तत्व से संबंधित होते हैं और समान रासायनिक गुण होते हैं, भले ही वे विभिन्न रासायनिक तत्व हों।
इसके अलावा, हम द्रव्यमान संख्या पाते हैं, जिसे अक्षर A द्वारा निरूपित किया जाता है। यह संख्या परमाणु में मौजूद न्यूक्लियंस की संख्या को दर्शाती है। एक अन्य प्रकार का परमाणु जिसे हम खोज सकते हैं, और जिसके बारे में हम सबसे अच्छी तरह जानते हैं, एक आइसोटोप है। इन परमाणुओं में प्रोटॉनों की संख्या समान होती है लेकिन न्यूट्रॉनों की संख्या भिन्न होती है। उनके रासायनिक गुण समान होते हैं, हालांकि उनके भौतिक गुण एक दूसरे से भिन्न होते हैं।
जैसा कि हमने पहले उल्लेख किया है, समस्थानिक बहुत महत्वपूर्ण हैं। और वे परमाणु ऊर्जा के लिए महत्वपूर्ण हैं क्योंकि यूरेनियम संवर्धन में एक यूरेनियम समस्थानिक को एक अधिक अस्थिर रासायनिक संरचना के साथ दूसरे में परिवर्तित करना शामिल है, जिससे हमें एक श्रृंखला प्रतिक्रिया की अनुमति मिलती है।
गुण
परमाणु को परिभाषित करने वाले गुण हैं:
- परमाणु क्रमांक (Z) नाभिक में प्रोटॉन की संख्या दर्शाता है। समान संख्या में प्रोटॉन वाले सभी परमाणु एक ही तत्व के होते हैं। उदाहरण के लिए, केवल एक प्रोटॉन वाला एक हाइड्रोजन परमाणु।
- द्रव्यमान संख्या प्रोटॉन और न्यूट्रॉन के योग को दर्शाती है।. विभिन्न संख्या में न्यूट्रॉन वाले तत्व एक ही तत्व के विभिन्न समस्थानिक होते हैं।
- वैद्युतीयऋणात्मकता रासायनिक बंधन बनाते समय इलेक्ट्रॉनों को आकर्षित करने के लिए परमाणुओं की प्रवृत्ति होती है।
- परमाणु का आधा घेरा यह एक ही तत्व के दो सम्मिलित नाभिकों के बीच की आधी दूरी के बराबर होता है।
- आयनीकरण क्षमता यह किसी तत्व से एक इलेक्ट्रॉन को निकालने के लिए आवश्यक ऊर्जा है।
मुझे उम्मीद है कि इस जानकारी से आप परमाणु क्या है और इसकी विशेषताओं के बारे में अधिक जान सकते हैं।
बहुत अच्छा
रिकार्डो