
Tutkimuksen jälkeen Thomsonin atomimalli, joka piti elektroneja positiivisesti varautuneessa väliaineessa, kehittyneempi malli, joka tunnetaan nimellä Rutherfordin atomimalli. Tämän uuden tieteen edistymisen johtaja oli Ernest Rutherford. Hän syntyi 20. elokuuta 1871 ja kuoli 19. lokakuuta 1937. Elämänsä aikana hän antoi suuren panoksen kemiaan ja tiedemaailmaan yleensä.
Siksi aiomme omistaa tämän artikkelin kertomaan sinulle kaiken, mitä sinun tarvitsee tietää Rutherfordin atomimallista.
Kultalehtikokeilu
Vanha thomson-malli sanoi, että elektronit olivat positiivisesti varautuneessa väliaineessa. Vuonna 1909 Ernest Rutherford, kahden avustajan, Geiger ja Marsden, seurassa, teki Gold Leaf -kokeiluna tunnetun tutkimuksen, jossa he pystyivät varmistamaan, että Thomsonin tunnettu "rusinapuuro" oli väärä. Ja että tämä uusi koe pystyi osoittamaan, että atomilla oli rakenne, jolla oli vahva positiivinen varaus. Tämä koe tai voisi auttaa palauttamaan joitain johtopäätöksiä, jotka esitettiin Rutherfordin atomimallina vuonna 1911.
Kullanlehdeksi kutsuttu koe ei ollut ainutlaatuinen, mutta ne tehtiin vuosina 1909–1913. Tätä varten he käyttivät Manchesterin yliopiston fysiikan laboratoriot. Nämä kokeet olivat erittäin tärkeitä, koska niiden tuloksista voitiin tehdä uusia johtopäätöksiä, jotka johtivat vallankumoukselliseen atomimalliin.
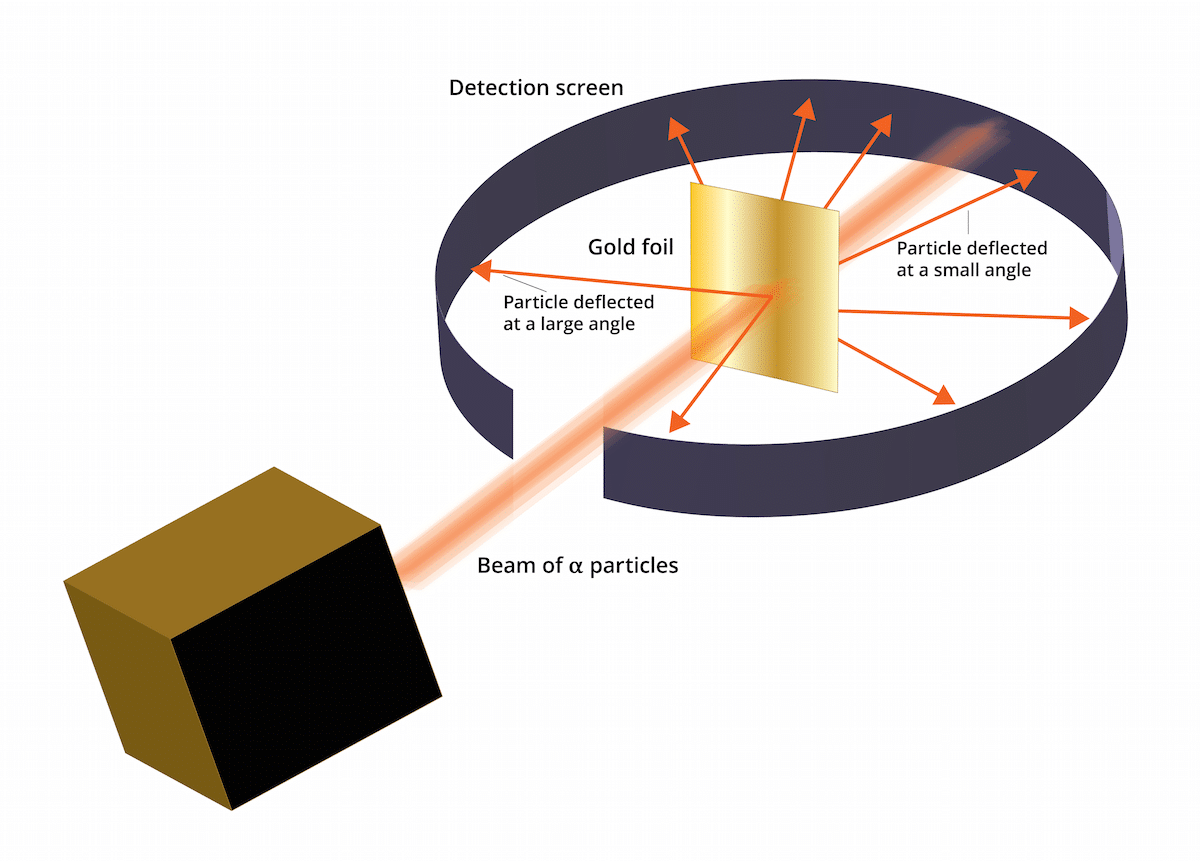
Tämä koe koostui seuraavista: ohut, vain 100 nm: n paksuinen kultalevy pommitettiin suurella määrällä alfa-hiukkasia. Nämä alfa-hiukkaset olivat ja ioneja. Eli atomit, joilla ei ole elektroneja, joten niillä oli vain protoneja ja neutroneja. Ottaen neutronit ja protonit atomin kokonaisvaraus oli positiivinen. Tämän kokeilun tarkoituksena oli pääasiassa vahvistaa Thomson-mallin oikeellisuus. Jos tämä malli oli oikea, alfahiukkasten oli kuljettava kultaatomien läpi suorassa linjassa.
Alfa-hiukkasten aiheuttaman taipuman tutkimiseksi hienon kultakalvon ympärille oli asetettava fluoresoiva sinkkisulfidisuodatin. Tämän kokeen tulos on, että havaittiin, että jotkut hiukkaset pystyivät kulkemaan arkin kultaatomien läpi suorassa linjassa. Jotkut näistä alfahiukkasista taipuivat kuitenkin satunnaisiin suuntiin.
Gold Leaf -kokeilun päätelmät

Tämän tosiasian vuoksi ei ollut mahdollista vahvistaa, mitä edellisiä atomimalleja pidetään. Ja juuri nämä atomimallit huomauttivat, että positiivinen varaus jakautui tasaisesti atomeihin, mikä helpottaisi sen ylittämistä, koska sen varaus ei olisi niin voimakas tietyssä vaiheessa.
Tämän Gold Leaf -kokeilun tulokset olivat täysin odottamattomia. Tämä sai Rutherfordin ajattelemaan, että atomilla oli keskellä voimakas positiivinen varaus, joka syntyi alfa-hiukkasena yritä välittää se keskushallinnon hylkäämänä. Luotettavamman lähteen saamiseksi hiukkasia tarkasteltiin määrinä heijastuneita ja niitä, jotka eivät heijastuneet. Tämän hiukkastevalinnan ansiosta oli mahdollista määrittää ytimen koko verrattuna sen ympärillä olevien elektronien kiertoradalle. Voidaan myös päätellä, että suurin osa atomin tilasta on tyhjä.
Voidaan nähdä, että kultakalvo ohjasi joitain alfahiukkasia. Jotkut heistä poikkesivat vain hyvin pienistä kulmista. Tämä auttoi päättelemään, että atomin positiivinen varaus ei jakaudu tasaisesti. Toisin sanoen positiivinen varaus sijaitsee atomilla keskitetysti hyvin pienessä tilavuudessa.
Hyvin harvat alfahiukkaset ajelehtivat takaisin. Tämä poikkeama osoittaa, että mainitut hiukkaset olisivat voineet palata takaisin. Kaikkien näiden uusien näkökohtien ansiosta Rutherfordin atomimalli voitaisiin luoda uusilla ideoilla.
Rutherfordin atomimalli

Aiomme tutkia, mitkä ovat Rutherfordin atomimallin periaatteet:
- Hiukkaset, joilla on positiivinen varaus atomin sisällä ne on järjestetty hyvin pieneen tilavuuteen, jos verrataan sitä mainitun atomin kokonaistilavuuteen.
- Lähes kaikki atomin massa on siinä mainitussa pienessä tilavuudessa. Tätä sisäistä massaa kutsuttiin ytimeksi.
- Elektronit, joilla on negatiiviset varaukset havaitaan pyörivän ytimen ympäri.
- Elektronit pyörivät suurilla nopeuksilla, kun ne ovat ytimen ympärillä, ja he tekevät sen pyöreillä poluilla. Näitä reittejä kutsuttiin kiertoradoiksi. Myöhemmin teen ne tunnetaan kiertoradoina.
- Sekä negatiivisesti varautuneet elektronit että positiivisesti varautuneen atomin ydin pidetään aina yhdessä sähköstaattisen vetovoiman ansiosta.
Rutherfordin atomimallin hyväksyminen ja rajoitukset
Kuten odotettiin, tämä uusi malli kuvasi aivan uuden panoraaman atomista tiedemaailmassa. Tämän atomimallin ansiosta monet myöhemmät tutkijat voisivat tutkia ja määrittää elektronien määrän, jotka jokaisella jaksollisen järjestelmän elementillä on. Lisäksi voitaisiin tehdä uusia löytöjä, jotka auttavat selittämään atomin toiminnan yksinkertaisimmalla tavalla.
Tällä mallilla on kuitenkin myös joitain rajoituksia ja virheitä. Vaikka se oli läpimurto fysiikan maailmassa, ne eivät olleet täydellinen eikä täydellinen malli. Ja onko se Newtonin lakien ja tärkeän Maxwellin lakien mukaisesti, tämä malli ei voinut selittää tiettyjä asioita:
- Hän ei pystynyt selittämään, kuinka negatiiviset varaukset pystyivät pitämään ytimessä. Elektronisen sääriluun mukaan positiivisten varausten on torjuttava toisiaan.
- Toinen ristiriita oli elektrodynamiikan peruslakeja kohtaan. Jos elektronien, joilla on positiivinen varaus, katsotaan pyörivän ytimen ympäri, niiden tulisi lähettää sähkömagneettista säteilyä. Kun säteily säteilee, energiaa kuluu elektronien romahtamiseen ytimessä. Siksi juovallinen atomimalli ei voi selittää atomin vakautta.
Toivon, että näiden tietojen avulla voit oppia lisää Rutherfordin atomimallista.