
Vesi on inimese ja kõigi planeedi elusolendite kõige väärtuslikum ressurss. See ressurss on element, mis võib loomulikult olla erinevates olekutes. The vee olekud Need on hüdroloogilises tsüklis väga olulised, et luua universaalne pidev vool.
Sel põhjusel pühendame selle artikli teile, millised on vee peamised olekud, millised on nende omadused ja kui tähtis on see.
vee olekud
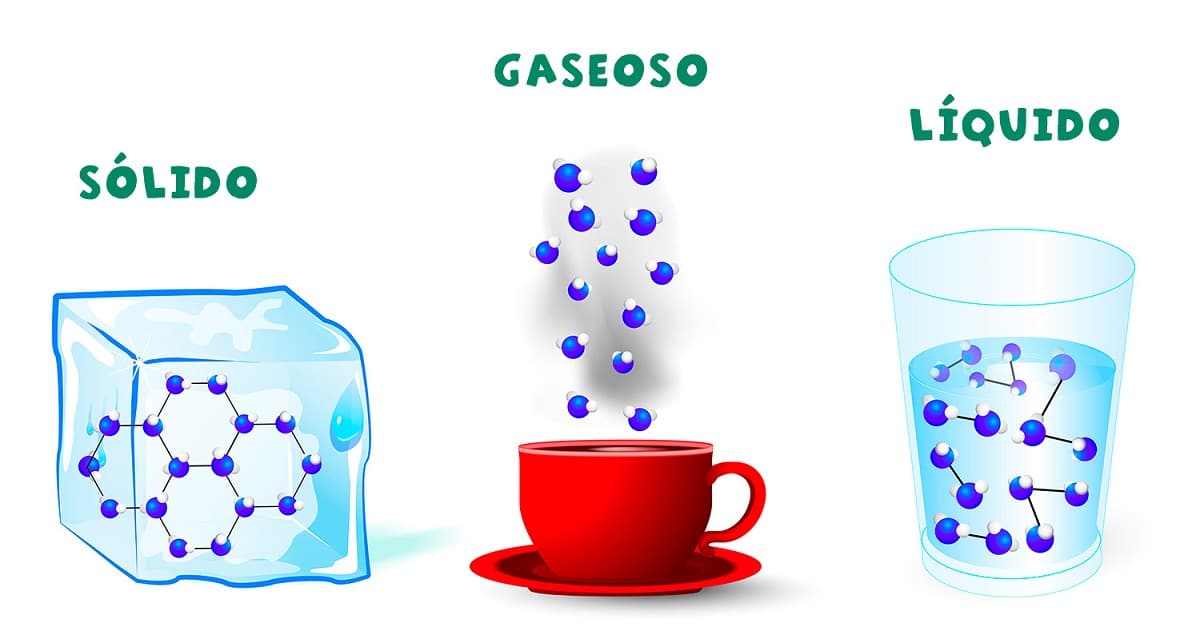
Me kõik teame, mis on vesi ja me teame selle kolme vormi, mida nimetatakse selle füüsikaliseks olekuks: vedel (vesi), tahke (jää) ja gaasiline (aur). Need on kolm vormi, milles vett võib looduses leida ilma selle keemilist koostist üldse muutmata: H2O (vesinik ja hapnik).
Vee olek sõltub seda ümbritsevast rõhust ja temperatuurist, millega see kokku puutub, st keskkonnatingimustest. Seetõttu saab nende tingimustega manipuleerimisel vedela vee muuta tahkeks või gaasiliseks olekuks ja vastupidi.
Arvestades vee tähtsust elule ja selle küllust Maal, teie füüsilist olekut kasutatakse paljudes mõõtesüsteemides võrdlusalusena ja seetõttu saab neid võrrelda teiste materjalide ja ainetega.
vee omadused

Pindpinevuse tõttu võivad putukad ja ämblikud vees liikuda. Vesi on lõhnatu, värvitu ja maitsetu aine, mille pH on neutraalne (7, ei happeline ega aluseline). See koosneb kahest vesinikuaatomist ja ühest hapnikuaatomist igas molekulis.
Selle osakestel on tohutud ühtekuuluvusjõud, mis hoiavad neid koos, seega on sellel märkimisväärne pindpinevus (mida mõned putukad kasutavad vee peal "kõndimiseks") ja selle füüsilise oleku muutmiseks kulub palju energiat.
Vett tuntakse kui "universaalset lahustit" sest see suudab lahustada rohkem aineid kui ükski teine vedelik. Lisaks on see eluks hädavajalik ühend ja seda leidub suurtes kogustes kõigis elusorganismides. Vesi katab kaks kolmandikku meie planeedi kogupindalast.
Vee erinevad olekud ja nende omadused
Vedelik
Vedelas olekus on vesi vedel ja paindlik. Seisund, millega meid kõige rohkem seostatakse, on vedel, mis on meie planeedi kõige tihedam ja arusaamatum ning kõige rikkalikum olek. Vedelas olekus, veeosakesed on lähestikku, kuid mitte liiga lähestikku. Seetõttu on vedel vesi samasugune kui vedelike paindlikkus ja voolavus, kuid kaotab oma kuju, et võtta seda sisaldava anuma kuju.
Seetõttu vajab vedel vesi teatud energia (soojus, temperatuur) ja rõhu tingimusi. Vesi on vedelik, mille temperatuur on vahemikus 0 kuni 100 ° C ja normaalõhurõhk. Kui aga allutada kõrgemale rõhule (ülekuumendatud vesi), võib see ületada keemistemperatuuri ja jõuda vedelas olekus kriitilise temperatuurini 374 °C, mis on kõrgeim temperatuur, mille juures gaas võib veelduda. Vedelat vett leidub tavaliselt ookeanides, järvedes, jõgedes ja maa-alustes setetes, kuid seda leidub ka elusorganismides.
Tahkes olekus
Vee tahke olek, mida sageli nimetatakse jääks, See saavutatakse, vähendades selle temperatuuri 0 °C-ni või alla selle. Külmunud vee üks veidrusi on see, et see lisab vedela vormiga võrreldes mahtu. See tähendab, et jää on vähem tihe kui vesi (sellepärast jää hõljub).
Jää välimus on kõva, rabe ja läbipaistev ning varieerub valgest siniseni, olenevalt kihi puhtusest ja paksusest. Teatud tingimustel võib ajutiselt jääda pooltahkesse olekusse, mida nimetatakse lumeks.
Tahket vett leidub tavaliselt liustikestes, mägede tippudes, igikeltsas (igikeltsas) ja päikesesüsteemi välisplaneetidel ning meie toidukülmikutes.
Gaasiline
Vee gaasiline olek, mida nimetatakse auruks või veeauruks, see on meie atmosfääri tavaline komponent ja esineb isegi igas hingetõmbes. Madala rõhu või kõrge temperatuuri korral vesi aurustub ja kipub tõusma, kuna veeaur on õhust vähem tihe.
Niikaua kui inimene on merepinnal (1 atmosfäär), toimub üleminek gaasilisse olekusse temperatuuril 100 °C. Gaasiline vesi moodustab pilved, mida näeme taevas, on õhus, mida me hingame (eriti väljahingamisel) ja udus, mis ilmub külmadel ja niisketel päevadel. Kui paneme poti vett keema, näeme ka seda.
Muutused vee seisundis
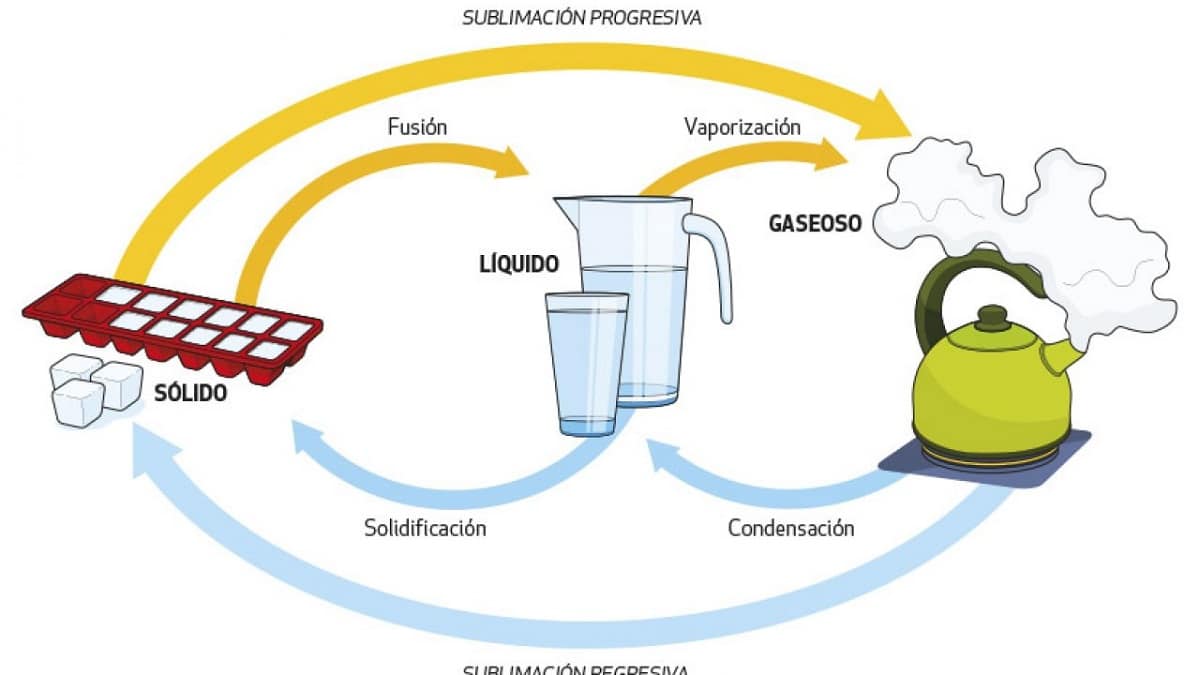
Nagu nägime mõnel eelneval juhul, võib vesi muutuda ühest olekust teise lihtsalt oma temperatuuritingimusi muutes. Seda saab teha ühes või teises suunas ja me anname igale erinevale protsessile oma nime:
- Aurustumine. Üleminek vedelikult gaasile tõstab vee temperatuuri 100°C-ni. Nii juhtub keeva veega, mistõttu sellele on iseloomulik mullitamine.
- Kondensatsioon. Muundamine gaasilisest vedelikuks soojuskao tõttu. Nii juhtub siis, kui veeaur kondenseerub vannitoapeeglile: peeglipind on jahedam ja sellele ladestunud aur muutub vedelaks.
- Külmutamine. Üleminek vedelast tahkeks alandab vee temperatuuri alla 0 °C. Vesi külmub, tekitades jääd, nagu see juhtub meie külmikutes või mäetippudel.
- Sulamine: muudab tahke vee vedelaks, kuumuse jääks. See protsess on tavaline ja seda on näha, kui lisame joogile jääd.
- Sublimatsioon. Gaasilisest olekust tahkeks muutumise protsess, antud juhul veeaurust otse jääle või lumele. Selleks on vaja väga spetsiifilisi temperatuuri ja rõhu tingimusi, mistõttu esineb see nähtus mägede tippudes, näiteks Antarktika põuas, kus vedelat vett pole.
- Pöördsublimatsioon: Tahke aine otsene muundamine gaasiks, st jääst auruks. Näeme seda väga kuivades keskkondades, nagu polaartundra ise või mägede tipud, kus päikesekiirguse suurenedes sublimeerub suurem osa jääst otse gaasiks, läbimata vedelat faasi.
Loodan, et selle teabe abil saate rohkem teada vee olekute ja selle omaduste kohta.