Füüsikamaailmas on haru, mis vastutab soojuse poolt tekitatavate ja süsteemis töötavate transformatsioonide uurimise eest. See on umbes termodünaamika. See on füüsika haru, mis vastutab kõigi transformatsioonide uurimise eest, mis tulenevad ainult protsessidest, mis hõlmavad nii temperatuuri kui ka energia olekumuutujate muutusi makroskoopilisel tasandil.
Selles artiklis räägime teile kõigest, mida peate teadma termodünaamika ja termodünaamika põhimõtete kohta.
põhijooned
Klassikalise termodünaamika analüüsimisel näeme, et see põhineb makroskoopilise süsteemi kontseptsioonil. See süsteem pole midagi muud kui väliskeskkonnast eraldatud osa füüsilisest või kontseptuaalsest massist. Termodünaamiliste süsteemide paremaks uurimiseks eeldatakse alati, et see on füüsiline mass, mida energia vahetus välise ökosüsteemiga ei häiri.
Makroskoopilise süsteemi olek, mis on tasakaalu tingimustes määratakse see suurustega, mida nimetatakse termodünaamilisteks muutujateks. Me teame kõiki neid muutujaid ja need on temperatuur, rõhk, maht ja keemiline koostis. Kõik need muutujad määravad süsteemid ja nende tasakaalu. Keemilise termodünaamika peamised märkused on loodud tänu rakendatud rahvusvahelisele liidule. Nende üksustega on võimalik töötada ja paremini selgitada termodünaamika seadust.
Siiski on termodünaamika haru, mis ei uuri tasakaalu, vaid vastutab termodünaamiliste protsesside analüüsimise eest, mida iseloomustavad peamiselt kellel puudub võime stabiilselt saavutada tasakaalutingimusi.
Seadused
Põhimõtted tauniti XNUMX. sajandi jooksul Isa, kes Nende ülesandeks on reguleerida kõiki teisendusi ja nende edenemist. Nad analüüsivad ka tegelikke kontseptsioone, millised on tegelikud piirid. Need on aksioomid, mida ei saa tõestada, kuid mis on kogemuste põhjal tõendamatud. Iga termodünaamika teooria põhineb neil põhimõtetel. Saame eristada kolme põhiprintsiipi pluss printsiip, kuid see määratleb temperatuuri ja on kaudne ka ülejäänud kolmes põhimõttes.
Null seadus
Kirjeldame, mis on see nullseadus, mis kirjeldab esimesena ülejäänud põhimõtetes kaudset temperatuuri. Kui kaks süsteemi suhtlevad üksteisega ja on termilises tasakaalus, on neil mõned omadused. Neid omadusi, mida nad omavahel jagavad, saab mõõta ja anda neile arvulise väärtuse. Selle tulemusena, kui need kaks süsteemi on kolmandaga tasakaalus, on nad omavahel tasakaalus ja jagatud omadus on temperatuur.
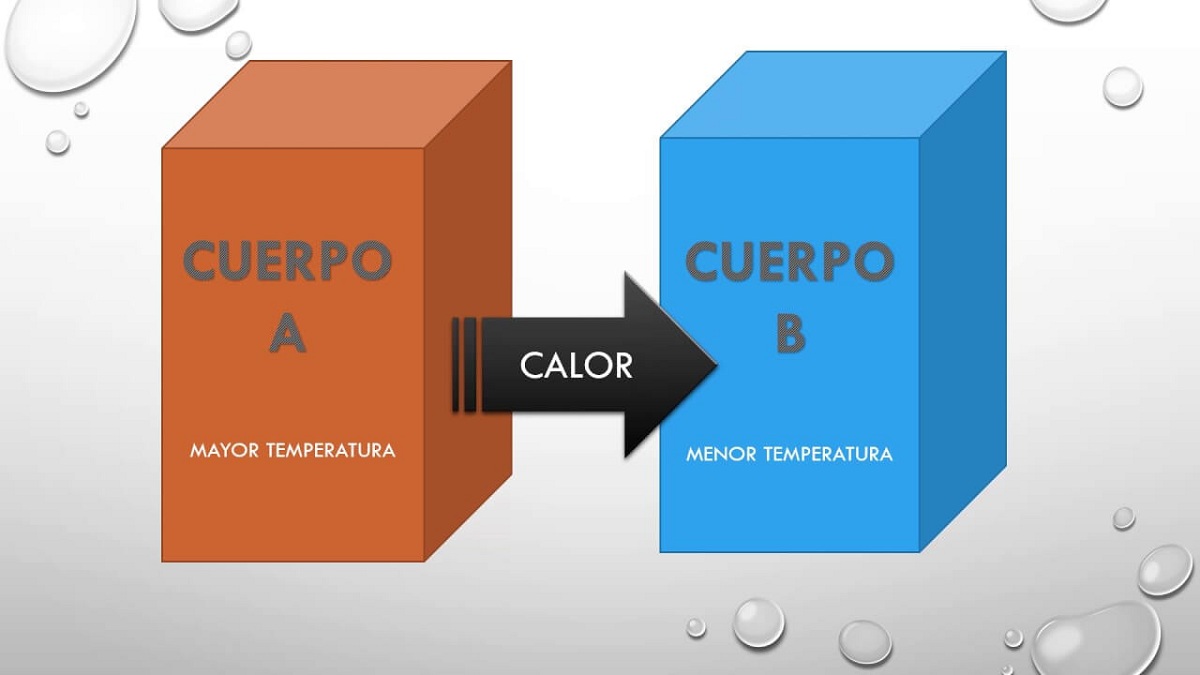
Seetõttu see põhimõte, kuid lihtsalt ütleb, et kui keha A oli kehaga B tasakaalus ja see keha B on kehaga C termilises tasakaalus, siis on ka kehad A ja C tasakaalus soojus. See põhimõte seletab asjaolu, et kaks erineval temperatuuril asuvat keha võivad omavahel soojust vahetada. Varem või hiljem saavutavad mõlemad kehad sama temperatuuri, seega on nad täielikus tasakaalus.
Esimene termodünaamika seadus
Kui keha viiakse kontakti kehaga, mis on külmem, toimub transformatsioon, mis viib tasakaalu seisundisse. See tasakaaluolek põhineb asjaolul, et kahe keha temperatuur on võrdne, kuna külma keha jaoks suureneb energia ülekandmine kuuma keha vahel. Selle nähtuse selgitamiseks eeldasid teadlased, et suurem aine, mida leidub suuremas koguses, möödus külmemast kehast. Mõeldi vedelikust, mis saaks läbi massi liikuda, et oleks võimalik soojust vahetada.
See põhimõte vastutab soojuse kui energiavormi identifitseerimise eest. See ei ole materiaalne aine. Sel viisil saaks näidata, et soojus, mida mõõdetakse kaloritega, ja töö, mida mõõdetakse džaulides, on samaväärsed. Seetõttu teame seda täna 1 kalor on umbes 4,186 džauli.
Võib öelda, et termodünaamika esimene põhimõte on energia säästmise põhimõte. Soojusmootori energiahulk muundatakse tööks ja seda näeb iga masin, mis suudab sellist tööd toota ilma energiat tarbimata. Selle esimese põhimõtte saame kehtestada järgmiselt: suletud termodünaamilise süsteemi siseenergia variatsioon on võrdne süsteemiga tarnitud soojuse ja selle süsteemi keskkonnas tehtud töö vahelise erinevusega.
Termodünaamika teine seadus
See ütleb alguses, et on võimatu teha tsüklilist masinat, mille tulemuseks on ainult soojuse ülekandmine külmast kehast sooja keha. Võime öelda, et on võimatu läbi viia ümberkujundamine, mille tulemus ainult saab olema see on ühest allikast eraldatud soojuse muundamine mehaaniliseks tööks.
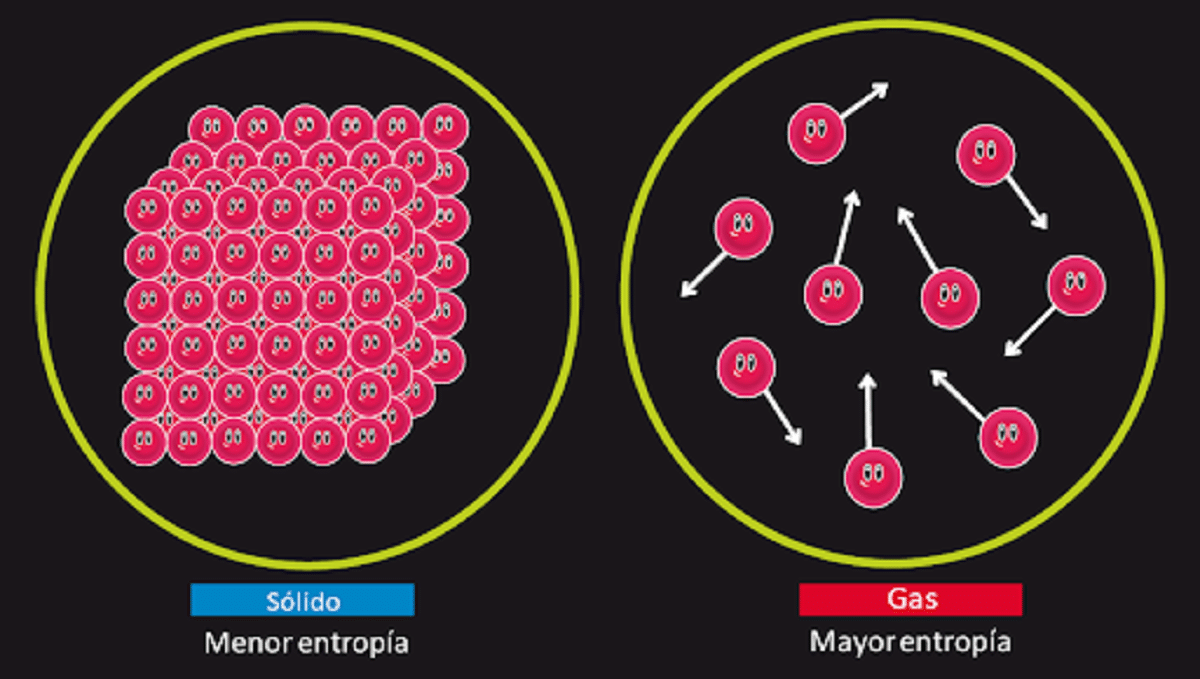
Selle põhimõtte eesmärk on eitada võimalust, et teise liigi teadaolev püsiv liikumine eksisteerib. Me teame, et entroopia süsteemi isoleerub muutumatuna, kui toimub pöörduv muundumine. Samuti teame, et see suureneb, kui toimub pöördumatu muundumine.
Termodünaamika kolmas seadus
See viimane põhimõte on tihedalt seotud teisega ja seda peetakse selle tagajärjeks. See põhimõte kinnitab, et absoluutset olendit ei saa saavutada värvilise hulga teisendustega. Me teame, et absoluutne null ei ole suurem kui minimaalne temperatuur, mida on võimalik saavutada. Ühikutes Kelvini kohta teame, et see on 0, kuid Celsiuse kraadides on selle väärtus -273.15 kraadi.
Samuti on selles öeldud, et ideaalselt kristallilise tahke aine entroopia temperatuuril 0 kelviini on võrdne 0-ga. See tähendab, et entroopiat ei oleks, seega oleks süsteem täiesti stabiilne. Selle moodustavate osakeste vabanemise, translatsiooni ja pöörlemise energia ei oleks 0 kelvini temperatuuril midagi.
Loodan, et selle teabe abil saate rohkem teada saada termodünaamikast ja põhiprintsiipidest.