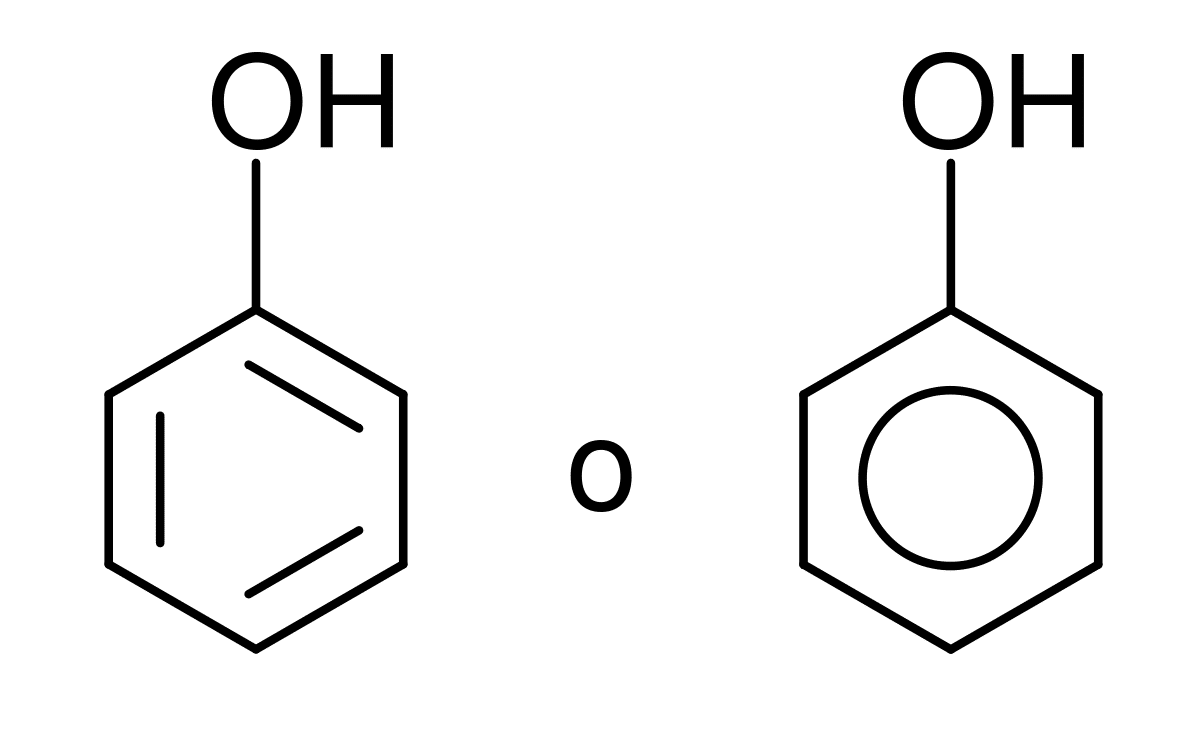
Rühm hüdroksüül See on see, mis koosneb hapnikuaatomist ja vesinikuaatomist ning sarnaneb veemolekuliga. Seda võib leida erinevates keemilistes vormides, nagu rühm, ioon või radikaal. Kõigi nende inimeste jaoks, kes uurivad orgaanilist keemiat, on selle aatomirühma reaktsioonide ja olulisuse tundmine ülioluline. Ja see on võimeline moodustama olulisi sidemeid süsinikuaatomiga, kuigi seda saab teha ka väävli ja fosforiga.
Selles artiklis räägime teile hüdroksüülrühma omadustest ja tähtsusest orgaanilises keemias.
põhijooned
Kui analüüsime hüdroksüülrühma anorgaanilise keemia seisukohalt, näeme, et see osaleb rohkem ioonina. See tähendab, et selle ja metallide vahel eksisteeriv pitsi tüüp ei ole kovalentne, vaid ioonne. Seetõttu on hüdroksüülrühm muutunud oluliseks elemendiks, mis aitab määratleda paljude ühendite omadusi ja muundumisi.
Hüdroksüülrühm on seotud radikaaliga, mis on määratletud ctähega R, kui see on alküül, või tähega Ar, kui see on aromaatne. Teaduse kohta tean kõige rohkem seda, mis aitab hüdroksüülrühma molekulis, milles see seondub. Parima vastuse leiab selle prootonite uurimisel. Ja kas tugevatest alustest saab prootoneid soolade moodustamiseks haarata. See võib suhelda ka teiste ümbritsevate rühmadega, mis on omavahel ühendatud vesiniksidemete abil. Lisaks on hüdroksüülrühma jaoks kõige olulisem see, et kus see ka poleks, võib see kujutada potentsiaalset piirkonda vee tekkeks.
Hüdroksüülrühma struktuur

Hüdroksüülrühm on orgaanilise keemia seisukohast muutunud üsna huvitavaks molekuliks. Veemolekul on nurgelise kujuga ja näeb välja nagu bumerang. Kui lõikame selle ühe otsa, mis tähendab sama, mis prootoni eemaldamine, võib juhtuda mitmesuguseid olukordi. Vee molekul on muundatakse hüdroksüülradikaaliks või hüdroksüüliooniks. Mõlemal on siiski molekulaarne lineaarne geomeetria ja need pole elektroonilised.
Kõik need sidemed on tingitud asjaolust, et nad on orienteeritud kahele aatomile, et olla võimelised alati joonduma. Sama ei ole hübriidorbitaalide puhul. Hüdroksüülrühma võti, mis võimaldab erinevatel molekulidel üksteisega seguneda, vajab vesiniksidemeid. Need vesiniksidemed pole iseenesest tugevad, kuid kui allikate arv suureneb ja hüdroksüülrühmade arv struktuuris suureneb, mõju mitmekordistub. See vesiniksidemete arvu suurenemine kajastub ka ühendi füüsikalistes omadustes.
Vesiniksidemed eeldavad, et aatomid oleksid üksteise vastas. Ühes hüdroksüülrühmas on mõned hapniku aatomid, mis peavad olema paigutatud nii, et see suudaks teise rühma vesinikuga tekitada sirgjoone. See on mõnevõrra keerulisem, kuid seda juhtub sageli. Sel moel tekivad üsna spetsiifilised ruumilised paigutused nagu mis toimub DNA molekuli struktuuris. See juhtub lämmastikaluste vahel, mis moodustavad DNA.
Hüdroksüülrühmade arvu võime nimetada struktuuriks, mis on otseselt proportsionaalne vee afiinsusega molekuli suhtes. Selle paremaks mõistmiseks toome näite. Kuigi suhkrul on hüdrofoobne süsiniku struktuur, on sellel palju hüdroksüülrühmi, muudab selle vees väga hästi lahustuvaks.
Ioonid ja nende funktsioonid
Hüdroksüülrühm ja ioon on väga sarnased, kuid neil on erinevad keemilised omadused. Hüdroksüülioon on äärmiselt tugev alus ja toimib prootonite püüdmisega. Kui me seda sunnime, võib see muutuda veeks. Ja see on mittetäielik veemolekul, mis on negatiivselt laetud ja mille lõpuleviimiseks on vaja prootonit. Teiselt poolt, kuna hüdroksüülrühm selle lõpuleviimiseks pole vaja prootoneid hõivata, see käitub nagu ülinõrk alus. Ta on võimeline loovutama prootoneid, kuigi teeb seda ainult väga tugevate aluste vastu.
Positiivsed tuumad on molekuli aatomid, mis kannatavad oma elektronegatiivse keskkonna tõttu elektroonilise defitsiidi all.
Hüdroksüülrühm ja meteoroloogia

Me teame, et see toimib õhus oleva detergendi tüübina, mis lagundab teisi gaase. Me teame, et metaani kontsentratsiooni peamine kontroll on hüdroksüülrühm. Metaanaas on kasvuhoonegaas, mille kontsentratsioon ületab ainult süsinikdioksiidi osakaal globaalses soojenemises. Kuigi metaangaasi leidub atmosfääris vähemal määral, on see võimeline säilitama suuremat soojushulka kui süsinikdioksiid.
NASA järeldoktorikraadi juhitud uued uuringud on näidanud, et hüdroksüülradikaalid töötlevad ise ja suudavad säilitada püsivat atmosfäärikontsentratsiooni. See kontsentratsioon säilib aja jooksul, isegi kui metaani heide suureneb. Seetõttu on hüdroksüüli rolli mõistmine metaani kasuliku eluea ja atmosfääri mõistmiseks hädavajalik.
Teadlased on välja toonud, et metaangaasi kontsentratsiooni ja heitkoguste suurenemine võib põhjustada hüdroksüülradikaalide hulga globaalses ulatuses ammendumise. Nii pikeneks metaani kasulik eluiga, mis lisaks kliima soojenemist. Metaani eluiga pikendades poleks meil midagi atmosfääri puhastada. On täheldatud hüdroksüül- ja metaanprimaarseid allikaid ja nende reageerimist. Selle rühma ringlussevõtt toimub pärast metaani lagunemist ja seejärel teiste gaaside juuresolekul reformimist. Hüdroksüülkontsentratsioonid on aja jooksul üsna stabiilsed. Need ei peaks tingimata metaaniga reageerides kaduma.
Loodan, et selle teabe abil saate rohkem teada hüdroksüülrühma ja kogu selle olulisuse kohta.