
Efter bekendtskabet Thomsons atommodel, som betragtede elektroner som et positivt ladet medium, en mere avanceret model kendt som Rutherford atommodel. Den videnskabsmand, der var ansvarlig for dette nye fremskridt inden for videnskab, var Ernest Rutherford. Han blev født den 20. august 1871 og døde den 19. oktober 1937. I løbet af sit liv gav han store bidrag til kemi og videnskabens verden generelt.
Derfor vil vi dedikere denne artikel til at fortælle dig alt hvad du behøver at vide om Rutherfords atommodel.
Guldbladeksperiment
Den gamle thomson-model sagde, at elektronerne var i et positivt ladet medium. I 1909 foretog Ernest Rutherford, ledsaget af to assistenter ved navn Geiger og Marsden, en undersøgelse kendt som Gold Leaf-eksperimentet, hvor de kunne kontrollere, at Thomsons velkendte "rosinpudding" var forkert. Og er det, at dette nye eksperiment var i stand til at vise, at atomet havde en struktur med en stærk positiv ladning. Dette eksperiment eller kunne hjælpe med at genskabe nogle konklusioner, der endte med at blive præsenteret som Rutherfords atommodel i 1911.
Eksperimentet kendt som Leaf of Gold var ikke unikt, men de blev udført mellem 1909 og 1913. Til dette brugte de fysiklaboratorierne ved University of Manchester. Disse eksperimenter var af stor betydning, da nye konklusioner kunne etableres ud fra deres resultater, hvilket førte til en revolutionær atommodel.
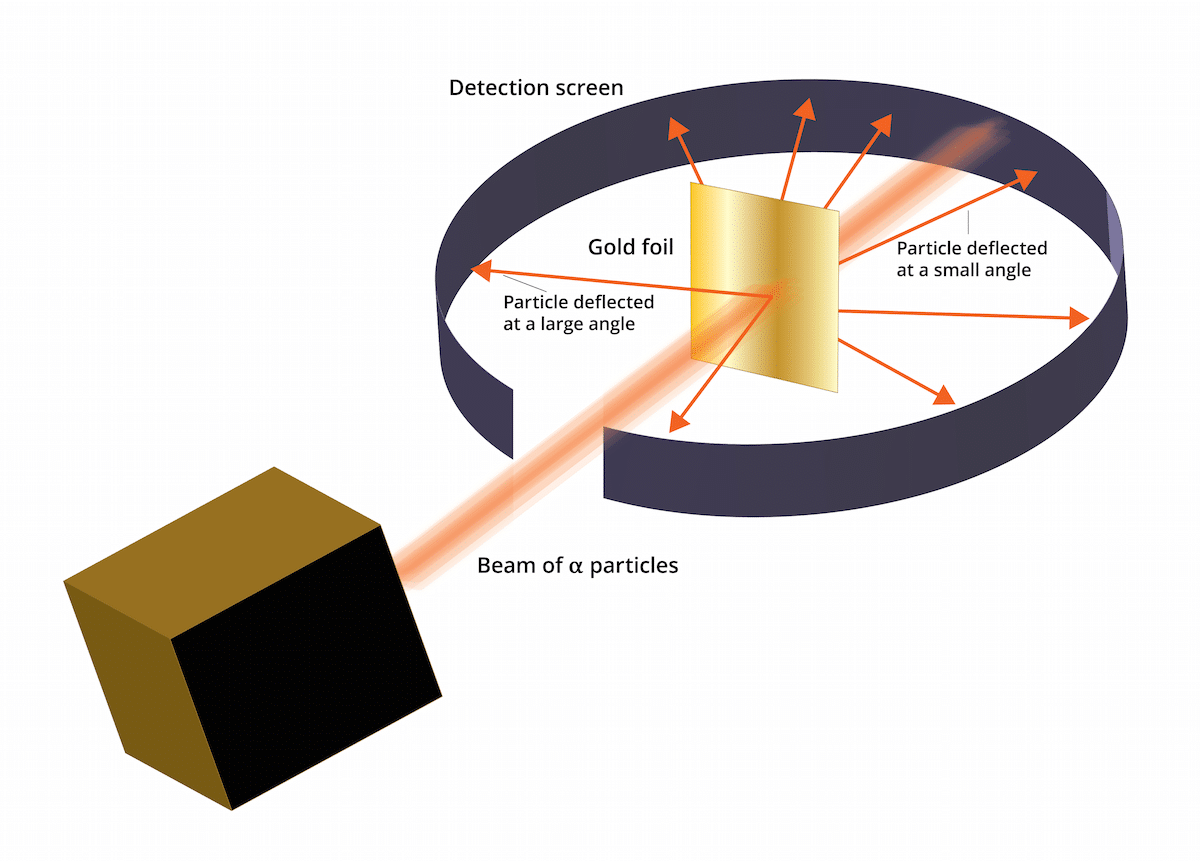
Dette eksperiment bestod af følgende: et tyndt ark guld kun 100 nm tyk måtte bombarderes med en stor mængde alfapartikler. Disse alfapartikler var og ioner. Atomer der ikke har elektroner, så de havde kun protoner og neutroner. Ved at have neutroner og protoner var atomens samlede ladning positiv. Dette eksperiment havde primært til formål at bekræfte, om Thomson-modellen var korrekt. Hvis denne model havde ret, alfapartiklerne måtte passere gennem guldatomer i en lige linje.
For at undersøge afbøjningen forårsaget af alfapartikler, måtte et fluorescerende zinksulfidfilter placeres omkring den fine guldfolie. Resultatet af dette eksperiment er, at det blev observeret, at nogle partikler var i stand til at passere gennem arkets guldatomer i en lige linje. Imidlertid blev nogle af disse alfapartikler afbøjet i tilfældige retninger.
Konklusioner af Gold Leaf eksperimentet

I betragtning af denne kendsgerning var det ikke muligt at bekræfte, hvad de tidligere atommodeller betragtes. Og det er, at disse atommodeller påpegede, at den positive ladning var fordelt ensartet i atomerne, og dette ville gøre det lettere at krydse den, da dens ladning ikke ville være så stærk på et bestemt tidspunkt.
Resultaterne af dette Gold Leaf-eksperiment var helt uventede. Dette fik Rutherford til at tro, at atomet havde et centrum med en stærk positiv ladning, som blev dannet af en alfapartikel prøv at give det afvist af den centrale struktur. For at etablere en mere pålidelig kilde blev partiklerne betragtet i mængder af dem, der blev reflekteret, og dem der ikke var. Takket være dette udvalg af partikler var det muligt at bestemme kernens størrelse sammenlignet med elektronernes bane omkring den. Det kunne også konkluderes, at det meste af rummet i et atom er tomt.
Det kunne ses, nogle alfapartikler blev afbøjet af guldfolien. Nogle af dem afvigede kun i meget små vinkler. Dette hjalp til med at konkludere, at den positive ladning på et atom ikke er jævnt fordelt. Det vil sige, den positive ladning er placeret på et atom på en koncentreret måde i et meget lille rumfang.
Meget få alfapartikler drev tilbage. Denne afvigelse indikerer som følger, at partiklerne kunne have genvundet. Takket være alle disse nye overvejelser kunne Rutherfords atommodel etableres med nye ideer.
Rutherford atommodel

Vi skal undersøge, hvad der er principperne for Rutherfords atommodel:
- Partikler, der har en positiv ladning inde i et atom de er arrangeret i et meget lille volumen, hvis vi sammenligner det med atomets samlede volumen.
- Næsten al den masse, som et atom har, er i det nævnte lille volumen. Denne indre masse blev kaldt kernen.
- Elektroner med negative ladninger findes roterende rundt om kernen.
- Elektronerne roterer ved høje hastigheder, når de er omkring kernen, og de gør det i cirkulære stier. Disse baner blev kaldt baner. Senere vil jeg de er kendt som orbitaler.
- Både de elektroner, der var negativt ladede, og kernen i selve det positivt ladede atom holdes altid sammen takket være den elektrostatiske tiltrækningskraft.
Accept og begrænsninger af Rutherfords atommodel
Som forventet forestillede denne nye model sig et helt nyt panorama af atomet i den videnskabelige verden. Takket være denne atommodel kunne mange senere forskere undersøge og bestemme antallet af elektroner, som hvert element i det periodiske system har. Derudover kunne der foretages nye opdagelser, der hjælper med at forklare et atoms funktion på den enkleste måde.
Denne model har dog også nogle begrænsninger og fejl. Selvom det var et gennembrud i fysikens verden, var de hverken en perfekt eller en komplet model. Og er det af ifølge Newtons love og et vigtigt aspekt af Maxwells love, denne model kunne ikke forklare visse ting:
- Han kunne ikke forklare, hvordan negative ladninger var i stand til at holde sammen i kernen. Ifølge den elektroniske skinneben skal positive ladninger afvise hinanden.
- En anden modsigelse var mod de grundlæggende love i elektrodynamik. Hvis elektroner med en positiv ladning skulle overvejes at rotere rundt om kernen, skulle de udsende elektromagnetisk stråling. Når der udsendes denne stråling, forbruges energi til elektronerne til at kollapse i kernen. Derfor kan den stribede atommodel ikke forklare atomets stabilitet.
Jeg håber, at du med disse oplysninger kan lære mere om Rutherfords atommodel.