Inden for fysik er der en gren, der har ansvaret for at studere de transformationer, der produceres af varme og arbejde i systemet. Det handler om termodynamik. Det er en gren af fysikken, der er ansvarlig for undersøgelsen af alle overgange, som kun er resultatet af en proces, der involverer ændringer i tilstandsvariablerne for temperatur og energi på makroniveau. Der er flere principper for termodynamik som er grundlæggende for mange aspekter af fysikken.
Derfor vil vi fortælle dig i denne artikel, hvad er principperne for termodynamik, og hvad er dens betydning.
Kendetegn ved termodynamik
Hvis vi analyserer klassisk termodynamik, vil vi opdage, at det er baseret på begrebet makroskopiske systemer. Dette system er kun en del af den fysiske eller konceptuelle kvalitet ved adskillelse fra det ydre miljø. For bedre at studere det termodynamiske system antages det altid, at det er en fysisk masse, der det forstyrres ikke af udveksling af energi med det eksterne økosystem.
Tilstanden for et makroskopisk system i ligevægt er angivet ved mængder kaldet termodynamiske variabler. Vi kender alle disse variabler: temperatur, tryk, volumen og kemisk sammensætning. Alle disse variabler definerer systemet og dets ligevægt. Takket være den internationale alliance af applikationer er hovedsymbolerne for kemisk termodynamik blevet etableret. Brug af disse enheder kan fungere bedre og forklare principperne for termodynamik.
Imidlertid der er en gren af termodynamik, der ikke studerer ligevægt, De er snarere ansvarlige for at analysere termodynamiske processer, der hovedsageligt er kendetegnet ved ikke at have evnen til at opnå ligevægtsbetingelser på en stabil måde.
Principper for termodynamik
Der er 4 principper for termodynamik, opført fra nul til tre punkter, disse love hjælper med at forstå alle fysikkens love i vores univers, og det er umuligt at se visse fænomener i vores verden. De er også kendt under navnet termodynamikkens love. Disse love har forskellig oprindelse. Nogle er formuleret ud fra tidligere formler. Den sidste kendte lov for termodynamik er nul -loven. Disse love er permanente i alle undersøgelser og undersøgelser, der udføres i laboratoriet. De er afgørende for at forstå, hvordan vores univers fungerer. Vi vil beskrive principperne for termodynamik en efter en.
Første princip
Denne lov siger, at energi ikke kan skabes eller ødelægges, den kan kun transformeres. Dette er også kendt som loven om bevarelse af energi. Rent faktisk, dette betyder, at i ethvert fysisk system, der er isoleret fra sit miljø, vil al dens energi altid være den samme. Selvom energi kan omdannes til andre energityper i en eller anden form, er summen af alle disse energier altid den samme.
Vi vil give et eksempel for at forstå det bedre. Efter dette princip, hvis vi bidrager med en vis mængde energi til et fysisk system i form af varme, kan vi beregne den samlede energi ved at finde forskellen mellem stigningen i intern energi og det arbejde, der udføres af systemet og dets omgivelser. Det vil sige, at forskellen mellem den energi, som systemet har på det tidspunkt, og det arbejde, det har udført, vil være den termiske energi, der frigives.
Andet princip
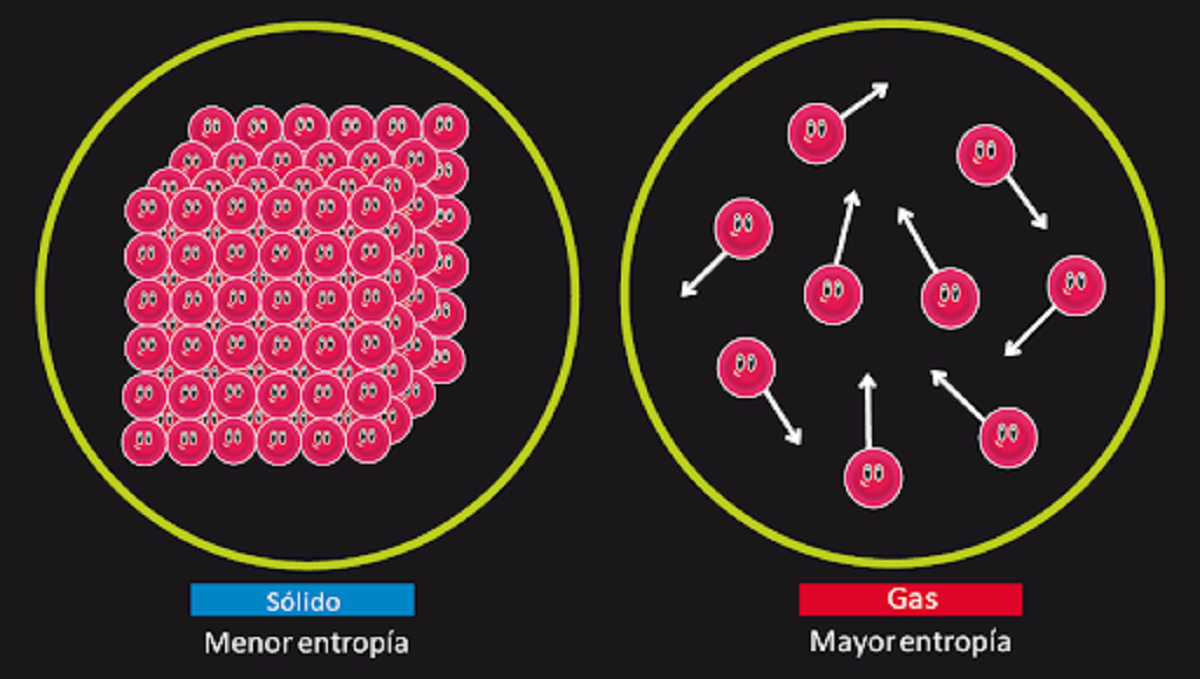
Hvis der er tid nok, mister alle systemer i sidste ende deres balance. Dette princip kaldes også entropiloven. Det kan opsummeres som følger. Mængden af entropi i universet vil stige med tiden. Systemets entropi er et indeks til måling af uorden. Med andre ord, Termodynamikkens andet princip fortæller os, at når systemet når et ligevægtspunkt, det vil øge graden af uorden i systemet. Dette kan betyde, at hvis vi giver et system nok tid, vil det i sidste ende blive ubalanceret.
Dette er den lov, der er ansvarlig for at forklare irreversibiliteten af nogle fysiske fænomener. For eksempel hjælper det os med at forklare, hvorfor et papir et papir er blevet brændt, kan ikke vende tilbage til sin oprindelige form. I dette system kendt som papir og ild er uorden steget i en sådan grad, at det ikke er muligt at vende tilbage til dets oprindelse. Denne lov introducerer entropi-tilstandsfunktionen, som i tilfælde af fysiske systemer er ansvarlig for at repræsentere graden af uorden og dens uundgåelige tab af energi.
For at forstå det andet princip i termodynamik vil vi give et eksempel. Hvis vi brænder en vis mængde stof, og vi sætter bolden sammen med den resulterende aske, kan vi se, at der er mindre stof end i den oprindelige tilstand. Dette skyldes, at stof er blevet til gasser De kan ikke genoprettes, og de skal spredes og rodes. Sådan ser vi, at der i stat et var mindst entropi end i stat to.
Tredje princip
Når absolut nul er nået, stopper den fysiske systemproces. Absolut nul er den laveste temperatur, vi kan nå. I dette tilfælde måler vi temperaturen i grader Kelvin. På denne måde kan det siges, at temperatur og køling bevirker, at systemets entropi er nul. I disse tilfælde ligner det mere en bestemt konstant. Når det når absolut nul, stopper den fysiske systemproces. Derfor vil entropien have en minimum, men konstant værdi.
At nå absolut nul eller ej er en let opgave. Den absolutte nulværdi for Kelvin -graden er nul, men hvis vi bruger den i Celsius temperaturskala måling er -273,15 grader.
Nul lov
Denne lov er sidstnævnte antog og siger, at hvis A = C og B = C, så er A = B. Dette fastlægger de grundlæggende og grundlæggende regler for de andre tre love for termodynamik. Det er et navn, der antager loven om termisk ligevægt. Med andre ord, hvis systemet og andre systemer uafhængigt er i termisk ligevægt, skal de være i termisk ligevægt. Denne lov tillader fastlæggelse af temperaturprincipper. Dette princip bruges til at sammenligne termisk energi fra to forskellige objekter i en tilstand af termisk ligevægt. Hvis disse to objekter er i termisk ligevægt, vil de være unødigt ved den samme temperatur. På den anden side, hvis de begge ændrer den termiske balance i det tredje system, vil de også påvirke hinanden.
Jeg håber, at du med disse oplysninger kan lære mere om principperne for termodynamik af dens egenskaber.