
Voda je nejcennějším zdrojem lidské bytosti a všech živých bytostí na planetě. Tento zdroj je prvek, který může být přirozeně v různých stavech. The vodní stavy Jsou velmi důležité v hydrologickém cyklu pro vytvoření univerzálního nepřetržitého toku.
Z tohoto důvodu věnujeme tento článek tomu, abychom vám řekli, jaké jsou hlavní skupenství vody, jaké jsou jejich vlastnosti a důležitost každého z nich.
vodní stavy
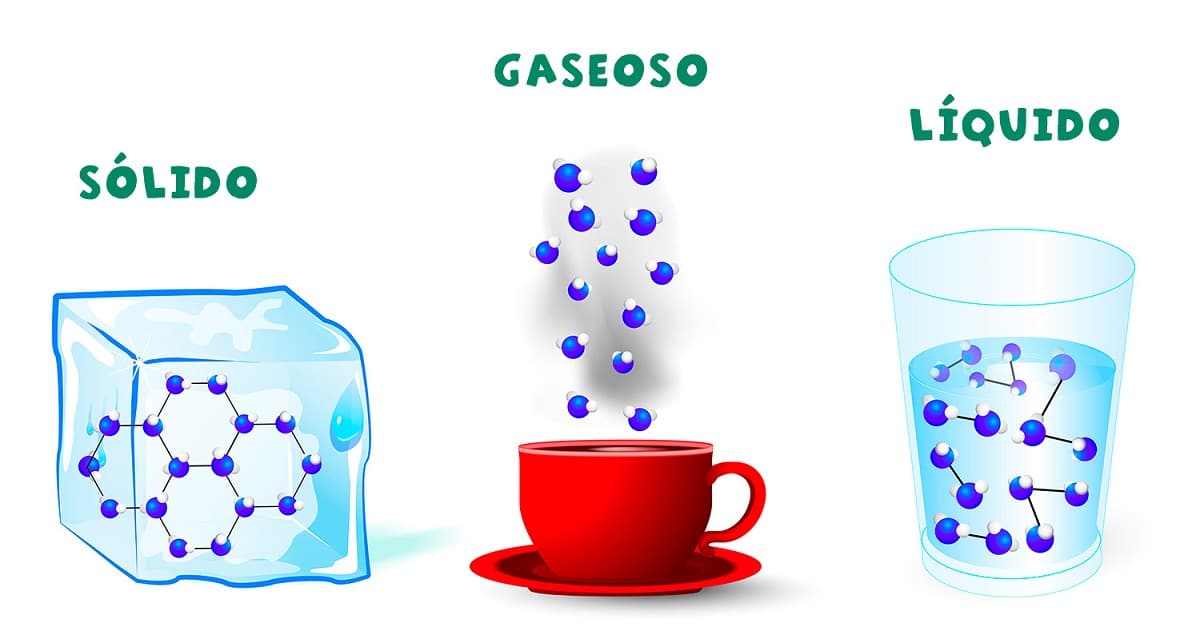
Všichni víme, co je voda a známe její tři formy, známé jako její fyzikální stavy: kapalné (voda), pevné (led) a plynné (pára). Toto jsou tři formy, ve kterých lze vodu v přírodě nalézt, aniž by se změnilo její chemické složení: H2O (vodík a kyslík).
Stav vody závisí na tlaku, který ji obklopuje, a teplotě, které je vystavena, tedy na podmínkách prostředí. Proto se manipulací s těmito podmínkami může kapalná voda přeměnit na pevné nebo plynné skupenství a naopak.
Vzhledem k důležitosti vody pro život a jejímu množství na Zemi, váš fyzický stav se používá jako reference v mnoha měřicích systémech a proto je lze srovnávat s jinými materiály a látkami.
vlastnosti vody

Vlivem povrchového napětí se ve vodě může pohybovat hmyz a pavouci. Voda je látka bez zápachu, barvy a chuti s neutrálním pH (7, není kyselá ani zásaditá). Je tvořen dvěma atomy vodíku a jedním atomem kyslíku v každé molekule.
Jeho částice mají obrovské kohezní síly, které je drží pohromadě, takže má značné povrchové napětí (které některý hmyz využívá k „chůzi“ po vodě) a vyžaduje hodně energie, aby změnil svůj fyzický stav.
Voda je známá jako „univerzální rozpouštědlo“ protože dokáže rozpustit více látek než jakákoli jiná kapalina. Kromě toho je základní sloučeninou života a je přítomen ve velkém množství ve všech živých organismech. Voda pokrývá dvě třetiny celkové plochy naší planety.
Různé skupenství vody a jejich vlastnosti
Kapalina
V kapalném stavu je voda tekutá a pružná. Stav, se kterým jsme nejvíce spojeni, je kapalný, což je nejhustší a nejvíce nepochopitelný stav a nejrozšířenější na naší planetě. V kapalném stavu, částice vody jsou blízko u sebe, ale ne příliš blízko u sebe. Proto má kapalná voda pružnost a tekutost kapalin, ale ztrácí svůj tvar, aby převzala tvar nádoby, která ji obsahuje.
Proto kapalná voda vyžaduje určité podmínky energie (teplo, teplota) a tlaku. Voda je kapalina při teplotách mezi 0 a 100 °C a normálním atmosférickém tlaku. Pokud je však vystaven vyšším tlakům (přehřátá voda), může překročit svůj bod varu a v kapalném stavu může dosáhnout kritické teploty 374 °C, což je nejvyšší teplota, při které může plyn zkapalnit. Kapalná voda se běžně vyskytuje v oceánech, jezerech, řekách a podzemních sedimentech, ale nachází se také uvnitř živých organismů.
Pevné skupenství
Pevné skupenství vody, často označované jako led, Toho je dosaženo snížením jeho teploty na 0 °C nebo méně. Jednou z podivností zmrzlé vody je, že ve srovnání s tekutou formou přidává objem. To znamená, že led je méně hustý než voda (proto led plave).
Vzhled ledu je tvrdý, křehký a průhledný a mění se od bílé po modrou v závislosti na čistotě a tloušťce vrstvy. Za určitých podmínek může dočasně zůstat v polotuhém stavu zvaném sníh.
Pevná voda se běžně vyskytuje v ledovcích, na vrcholcích hor, ve věčně zmrzlé půdě (permafrost) a na vnějších planetách sluneční soustavy a v našich mrazničkách na potraviny.
Plynný
Plynné skupenství vody, známé jako pára nebo vodní pára, je běžnou součástí naší atmosféry a je dokonce přítomen v každém nádechu, který uděláme. Při nízkém tlaku nebo vysoké teplotě se voda vypařuje a má tendenci stoupat, protože vodní pára je méně hustá než vzduch.
Dokud je člověk na hladině moře (1 atmosféra), k přechodu do plynného skupenství dochází při 100 °C. Plynná voda tvoří mraky, které vidíme na obloze, je ve vzduchu, který dýcháme (zejména ve výdechu), a v mlze, která se objevuje za chladných a vlhkých dnů. Pokud dáme vařit hrnec s vodou, vidíme to také.
Změny skupenství vody
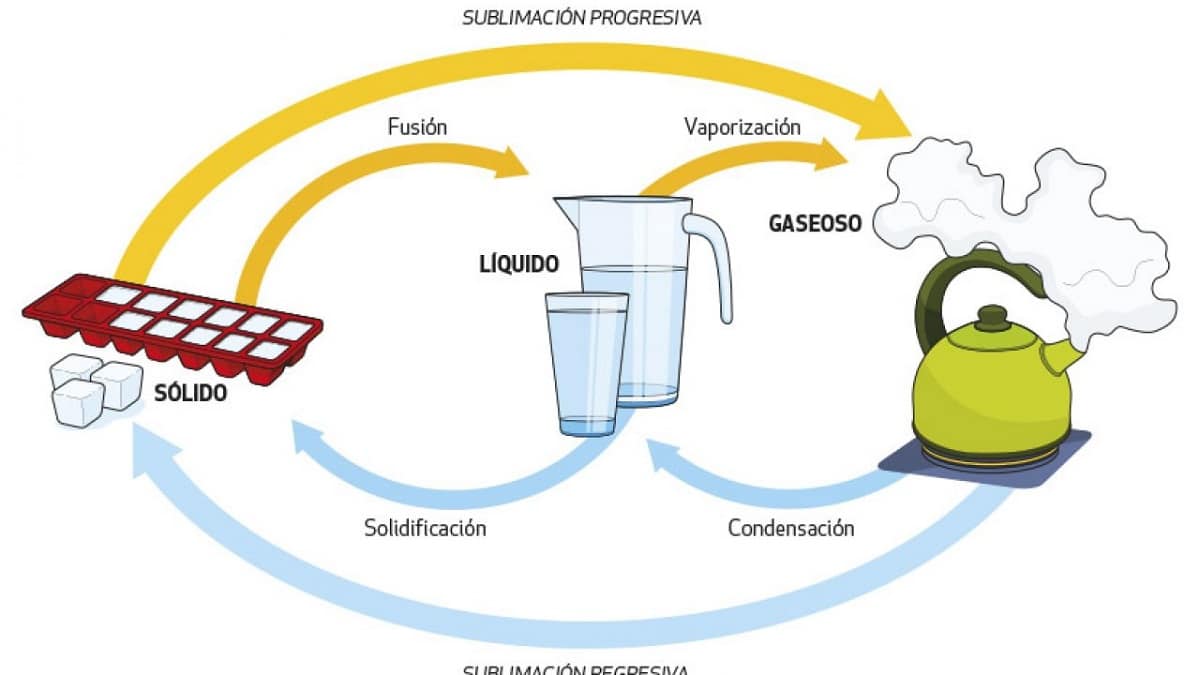
Jak jsme viděli v některých předchozích případech, voda se může změnit z jednoho skupenství do druhého jednoduše změnou teplotních podmínek. To lze provést jedním nebo druhým směrem a každému jinému procesu dáme vlastní název:
- Vypařování. Přechod z kapaliny na plyn zvyšuje teplotu vody na 100°C. To se děje s vařící vodou, proto se vyznačuje bubláním.
- Kondenzace. Přeměna z plynného na kapalné tepelnými ztrátami. To se stane, když vodní pára kondenzuje na zrcadle v koupelně: povrch zrcadla je chladnější a pára na něm usazená se stává tekutou.
- Zmrazení. Přechod z kapaliny na pevnou látku snižuje teplotu vody pod 0°C. Voda zamrzá a vytváří led, jako je tomu v našich ledničkách nebo na vrcholcích hor.
- Tání: mění pevnou vodu na kapalinu, teplo na led. Tento proces je běžný a je vidět, když do nápoje přidáme led.
- Sublimace. Proces přeměny z plynného skupenství do pevného, v tomto případě z vodní páry přímo na led nebo sníh. K tomu jsou potřeba velmi specifické teplotní a tlakové podmínky, proto k tomuto jevu dochází na vrcholcích hor, například za sucha v Antarktidě, kde není kapalná voda.
- Reverzní sublimace: Přímá přeměna pevné látky na plyn, to znamená z ledu na páru. Můžeme ho vidět ve velmi suchých prostředích, jako je samotná polární tundra nebo vrcholky hor, kde se zvyšujícím se slunečním zářením většina ledu sublimuje přímo do plynu, aniž by procházela kapalnou fází.
Doufám, že s těmito informacemi se dozvíte více o skupenstvích vody a jejích vlastnostech.