
Un cambio químico es una alteración de la materia que cambia su estructura química, es decir, cambia sus propiedades, no solo su forma. Esto significa que un cambio químico, también conocido como reacción química o fenómeno químico, implica romper y formar enlaces químicos de una sustancia o compuesto para formar una nueva sustancia o compuesto. Existen numerosos cambios químicos en el mundo.
Por ello, vamos a dedicar este artículo a contarte cuáles son los principales cambios químicos que existen y ejemplo sobre ellos.
Qué es son los cambios químicos

Cuando dos o más sustancias (llamadas reactivos o reactivos) sufren una reacción química, cambiando su estructura química en el proceso y siendo capaces de consumir (reacciones endotérmicas) o liberar (reacciones exotérmicas) energía, produciendo dos o más sustancias (llamada producto ). Algunas reacciones químicas son peligrosas para los humanos porque pueden involucrar o producir compuestos tóxicos o corrosivos. Otras reacciones, como ciertas reacciones exotérmicas, pueden provocar explosiones.
En la industria química, muchos materiales que utilizamos en nuestra vida diaria se producen mediante reacciones químicas controladas. Algunas reacciones ocurren espontáneamente, otras tienen que ser producidas por humanos en fábricas o laboratorios químicos. Una reacción química tarda una cantidad específica de tiempo en ocurrir, dependiendo de la naturaleza de los reactivos y las condiciones bajo las cuales ocurre la reacción.
Por lo tanto, los factores que afectan la velocidad de las reacciones químicas generalmente incluyen:
- La temperatura sube. Un aumento en la temperatura tiende a aumentar la velocidad de una reacción química.
- Aumento de la presión. El aumento de la presión generalmente aumenta la velocidad de una reacción química. Esto suele ocurrir cuando reaccionan sustancias que son sensibles a los cambios de presión, como los gases. En el caso de líquidos y sólidos, los cambios de presión no provocan cambios importantes en sus velocidades de reacción.
- Estado de agregación del reactivo. Los sólidos reaccionan generalmente más lentamente que los líquidos o los gases, aunque la velocidad también depende de la reactividad de cada sustancia.
- Uso de catalizador. Son sustancias que se utilizan para aumentar la velocidad de las reacciones químicas. Estas sustancias no interfieren con la reacción, solo controlan la velocidad a la que ocurre la reacción. También existen sustancias llamadas inhibidores, que se usan de la misma manera pero tienen el efecto contrario, ralentizando la reacción.
- Energía luminosa. Algunas reacciones químicas se aceleran cuando la luz incide sobre ellas.
- Concentración de reactivo. La mayoría de las reacciones químicas ocurren más rápido si las concentraciones de los reactivos son altas.
Ejemplos de cambios químicos
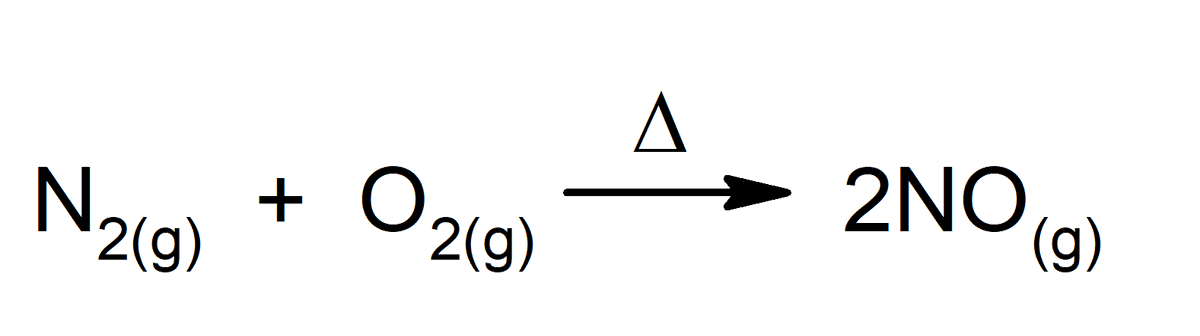
Cualquier reacción química es un ejemplo perfecto de cambio químico, incluso las que tienen lugar dentro de nuestro cuerpo. Algunos ejemplos son:
- Respiración. Este es un proceso biológico alterado químicamente en el que se toma oxígeno del aire y se usa para reaccionar con la glucosa que obtenemos de los alimentos, produciendo altos niveles de energía química (ATP) y grandes cantidades de desechos de dióxido de carbono (CO2) que deben ser excretados .
- Lluvia ácida. Ocurre en ambientes con severa contaminación del aire. Suele ser el resultado de un cambio químico entre el agua almacenada en las nubes y otros gases dispersos en el aire, cuyo contenido de óxido de azufre u óxido de nitrógeno crea ácido sulfúrico o ácido nítrico que cae con el agua de lluvia para formar sal. La reacción que tiene lugar dentro de la batería es entre el ácido y el metal. Por ejemplo, una batería que usa plomo y ácido sulfúrico produce sulfato de plomo (II), una sal blanca. Descomposición del ozono. Las moléculas de ozono se descomponen en moléculas de oxígeno bajo la acción de algún tipo de luz.
Cambio químico y cambio físico

Los cambios físicos de una sustancia no modifican su composición, es decir, no modifican la estructura química de la sustancia, por lo que las sustancias no pueden descomponerse ni formarse mediante cambios físicos. El cambio físico simplemente cambia las propiedades físicas de la materia, como la forma, la densidad y el estado de agregación (sólido, líquido, gas). Los cambios físicos, por otro lado, suelen ser reversibles porque cambian la forma o el estado de la materia, pero no su composición.
Por ejemplo, cuando el agua hierve, podemos convertir un líquido en gas, pero el vapor resultante aún está compuesto de moléculas de agua. Por el contrario, si congelamos el agua, se vuelve sólida, pero sigue siendo químicamente la misma sustancia.
Otro ejemplo es el gas licuado que usamos en nuestros encendedores de cigarrillos, generalmente butano (C4H10) o propano (C3H8) que se vuelve líquido al aplicar alta presión, pero no cambia su composición química.
Un cambio químico cambia la distribución y el enlace de los átomos de una sustancia para que se combinen de una manera diferente, dando como resultado una sustancia diferente a la original. Cuando ocurre un cambio químico, siempre terminas con la misma cantidad de sustancia con la que comenzaste, incluso si está en una proporción diferente, porque la materia no puede crearse ni destruirse, solo transformarse.
Por ejemplo, si hacemos reaccionar agua (H2O) y potasio (K), obtendremos dos nuevas sustancias: hidróxido de potasio (KOH) e hidrógeno gaseoso (H2). Esta es una reacción que generalmente libera mucha energía y, por lo tanto, es muy peligrosa.
Ejemplos de cambios químicos en la materia
Hornear galletas o pasteles
Cosas comunes como galletas, pasteles, cupcakes, etc. esconden una reacción química llamada fermentación, en la cual la masa crece debido a los gases producidos por la levadura. En la elaboración del pan, la levadura convierte el almidón en glucosa.
Digestión
La digestión de los alimentos es un ejemplo obvio del cambio químico de la materia a través de la hidrólisis (la descomposición de la materia orgánica por la acción del agua). Los alimentos que ingerimos en forma de frutas, verduras, carnes, etc., pasan por un proceso de mezcla con los jugos gástricos para absorber mejor los nutrientes y convertirlos en diversas sustancias según las necesidades del organismo.
En el mismo proceso, los elementos sobrantes o toxinas se eliminan del organismo de forma diferente a la original; en forma de heces, orina, sudor, etc.
Pulque
La fermentación es un proceso catabólico en el que las moléculas de glucosa se degradan por falta de oxígeno. Algunas de las bebidas alcohólicas obtenidas a través del proceso de fermentación son la sidra, la cerveza y el vino suave, siendo este último una de las bebidas menos conocidas en el mundo. El pulque se obtiene de la planta del agave a través de un proceso artesanal, en el que la maduración de la sustancia es clave para obtener el producto final, que es blanco, agrio y viscoso, con un sabor muy específico que no conviene a ningún paladar.
La fermentación también ocurre durante la elaboración del pan, el yogur y el queso, entre otros.
Caramelo
El caramelo es un ejemplo básico de un cambio químico en la sustancia, ya que el azúcar blanco y sólido, calentado durante unos minutos, se convierte en una sustancia viscosa de color ámbar con un aroma agradable. En otras palabras, se genera un producto completamente diferente al original.
Espero que con esta información puedan conocer más sobre los cambios químicos y sus ejemplos.