Segurament quan sents parlar de el forat de la capa d'ozó que compten els gasos responsables d'això. La principal substància química que ha provocat la disminució en la concentració d'ozó atmosfèric són els clorofluorocarbonis. Es tracta de substàncies químiques gasoses que es van emprar des dels seus inicis l'any 1928. També són coneguts per les sigles CFC. Es van investigar en detall i van demostrar que les seves propietats posaven en perill no només a la salut pública sinó a la capa d'ozó. Per això, el seu ús va ser prohibit.
En aquest article anem a explicar què són els clorofluorocarbonis, quines són les seves característiques i perquè destrueixen la capa d'ozó.
Què són els clorofluorocarbonis

Es tracta de substàncies químiques que estan formades per àtoms de carboni, fluor i clor. D'aquí el seu nom. Aquests àtoms pertanyen a el grup de els halocarbons que són el grup dels gasos no són tòxics ni inflamables. Van ser originats per primera vegada l'any 1928 com una alternativa a diverses substàncies químiques que es feien servir en els frigorífics. Més tard es van emprar com propulsors dels insecticides, pintures, condicionadors per a cabell i altres productes d'atenció mèdica.
Entre la dècada dels 50 i 60 van ser utilitzats en els aires condicionats de les cases, automòbils i oficines. Tots aquests usos van fer que els clorofluorocarbonis es expandieran de forma mundial. En aquell moment l'ús d'aquests químics es va incrementar comes d'un milió de tones mètriques que es produïen anualment de tan sols als Estats Units. Més tard va augmentar encara més el seu ús. Va arribar a tal extensió que es va utilitzar com a aerosol, refrigerant és, agent expansor per a les escumes, material d'embalatge i en solvents.
Productes amb clorofluorocarbonis més freqüents

Aquests químics no tenen una font natural de què surtin. Són productes químics creats per l'ésser humà per nombrosos usos. Van ser utilitzats com a refrigerants, propel·lents i solvents industrials per a la fabricació d'escumes. També servia com a agent de neteja a la fabricació de productes electrònics. Va ser tal el seu ús l'impacte en la capa d'ozó es va incrementar enormement en poc temps. Es va saber que aquests gasos destrueixin l'ozó estratosfèric a tal nivell que feia que la radiació ultraviolada solar nociva pogués arribar a superfície.
Entre els productes amb clorofluorocarbonis més coneguts tenim els següents:
- Refrigerant és en aires condicionats.
- Frigorífics.
- Propel·lents en aerosols.
- Inhaladors per controlar l'asma. Més tard això va ser prohibit per reduir l'impacte en l'estratosfera.
- Haloalcanos en aeronaus.
- Solvents desitgin greix abans.
Efectes negatius dels clorofluorocarbonis en l'atmosfera
Com hem esmentat abans es va saber que aquests químics danyaven la capa d'ozó. Això fa que gran part de la radiació ultraviolada de el sol pugui travessar l'estratosfera i arribar fins a la superfície terrestre. Es va veure que tenia nombrosos efectes negatius sobre la nostra pròpia salut. I és que, a l'tractar de diversos compostos que són químicament inerts es va pensar que serien innocus a l'atmosfera. No obstant això, amb el pas el temps es va poder comprovar que reaccionaven amb la radiació ultraviolada en l'atmosfera, concretament a l'estratosfera.
En aquesta capa de l'atmosfera es troba una gran concentració d'ozó que ens ajuda a reduir la radiació ultraviolada que ens arriba de el sol. A aquesta gran concentració d'ozó se li coneix com a capa d'ozó. Quan els clorofluorocarbonis interaccionen amb la radiació pateixen una descomposició fotolítica que ens converteix en fonts de clor inorgànic. Quan el clor és alliberat en forma d'àtoms són capaços de catalitzar la conversió de les molècules d'ozó en oxigen. Això vol dir que accelera la reacció química que es produeix de forma natural de la conversió de l'ozó en oxigen.
Recordem que una molècula d'ozó està compost per 3 àtoms d'oxigen. L'oxigen atmosfèric està compost per dos àtoms d'oxigen. D'aquesta manera, el clor actua com un catalitzador per augmentar la velocitat i quantitat de reaccions químiques que converteix en l'ozó en oxigen. D'aquesta manera s'aconsegueix destruir fins a 100.000 molècules d'ozó per cada àtom de clor que és alliberat. Totes aquestes raons són per les que els clorofluorocarbonis estar relacionats amb la destrucció de la capa d'ozó.
No és que aquests químics destrueixin directament l'ozó que es troba a l'estratosfera, sinó que es requereixen diverses reaccions químiques perquè es doni. No obstant això, la velocitat a la qual els clorofluorocarbonis s'emetran a l'atmosfera provocava que gran quantitat d'ozó estratosfèric estigués desapareixent. La desaparició de la capa d'ozó té conseqüències molt perjudicials i augmenta encara més la contaminació química. I és que l'ozó és l'encarregat de absorbir gran part de la radiació ultraviolada de el sol que està comprès entre longituds d'ona de 280 i 320 nm i que resulta nociva per als organismes tant animals com vegetals i l'ésser humà, és clar.
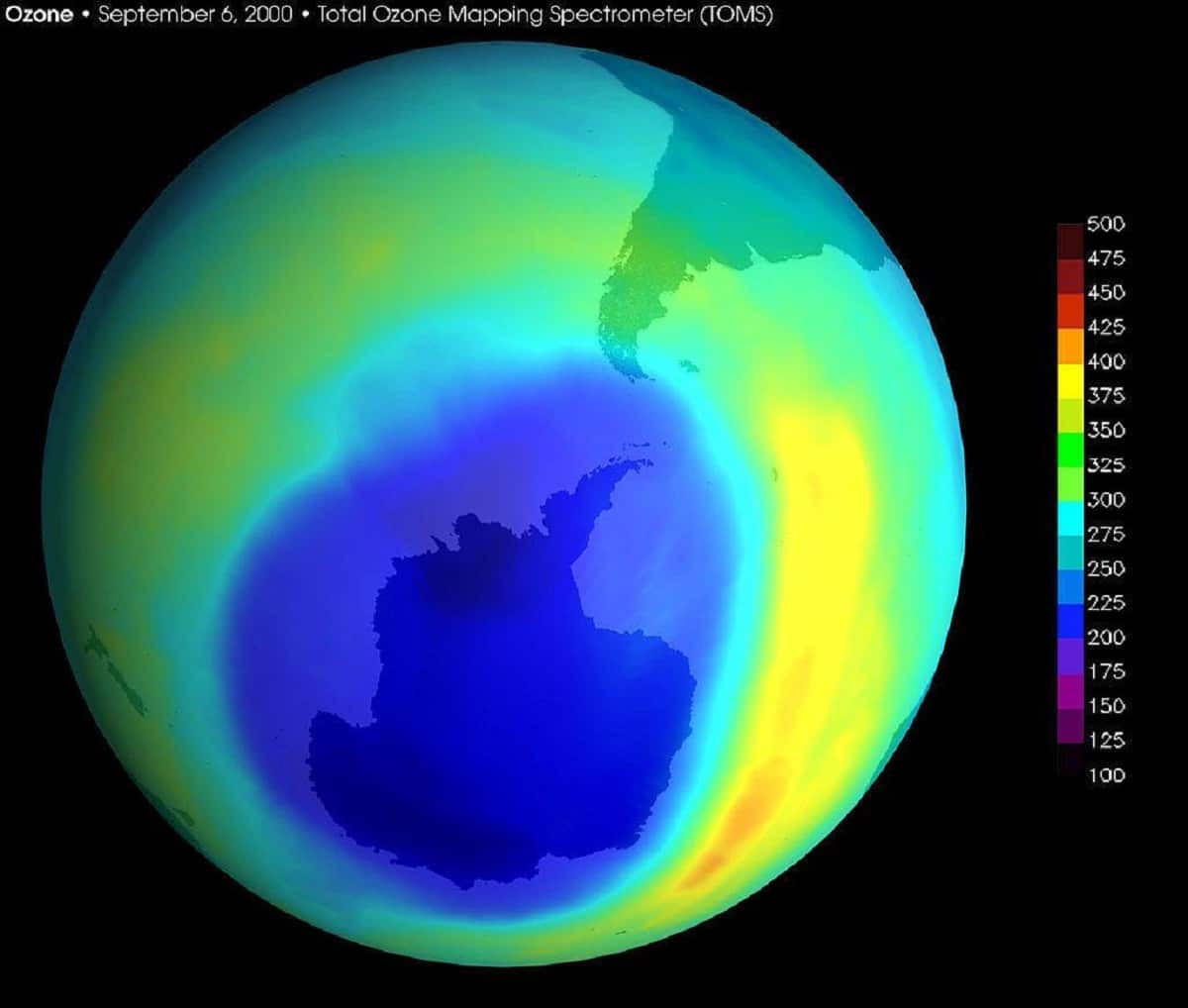
Forat d'ozó
La utilització d'aquests químics en gran proporció ha resultat en la creació de forats a la capa d'ozó. No és que hi hagi un forat pròpiament dit en què no hi hagi cap tipus de concentració d'ozó. Simplement són zones en què la concentració d'ozó està molt per sota del que és normal. Aquesta concentració és prou baixa com per no permetre què la radiació ultraviolada es quedi a la tractes serà i penetrar a la superfície terrestre.
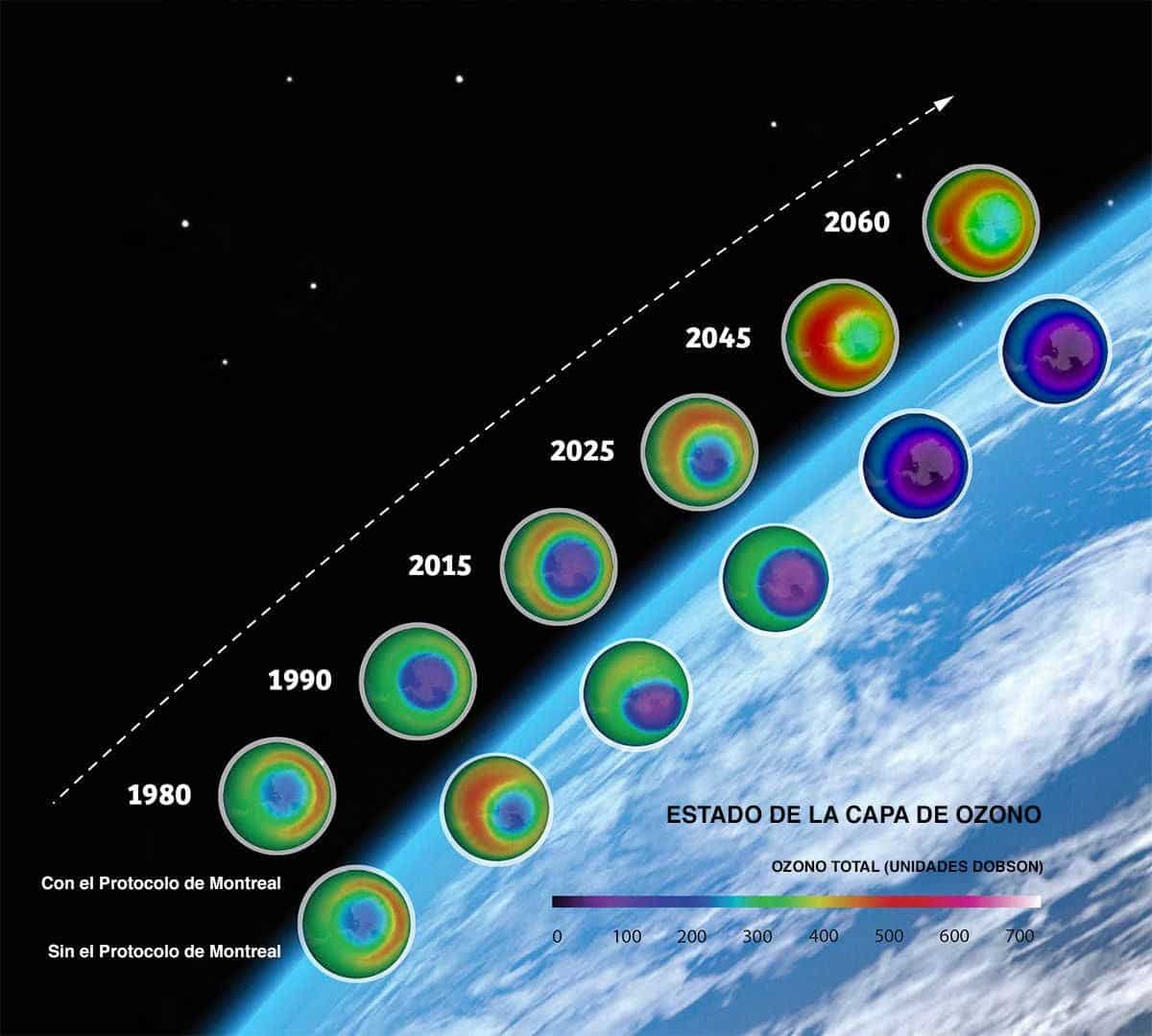
Tot i que els clorofluorocarbonis estan prohibits, pel fet que tenen gran inèrcia química i són insolubles, encara a dia d'avui, es troben gran part dels químics emesos durant els anys anteriors. Això és degut a que tenen gran esperança de vida a l'atmosfera. Des de l'any 1987 el protocol de Mont-real va reconèixer aquests compostos químics com nocius i es van unir altres acords internacionals que va provocar o la prohibició d'aquests químics, ja que també actuen com a gasos d'efecte hivernacle.
Com poden veure, els clorofluorocarbonis tenen grans efectes negatius tant en l'atmosfera, com en els animals, plantes i en l'ésser humà. Espero que amb aquesta informació puguin conèixer més sobre els clorofluorocarbonis.